Влияние способа отварочного затирания на состав молодого светлого пива
Автор: Оселедцева И.В., Назаренко М.А., Палагин К.А., Ханин Д.К., Чусова А.Е., Киселев А.С.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 1 (99) т.86, 2024 года.
Бесплатный доступ
В настоящее время производители пива сталкиваются с проблемой соотношения цена/качество при работе с отечественным солодом и хмелем. Поэтому актуальным становится изучение технологических приемов, влияющих на сырье, с целью регулирования качественных показателей готовой продукции. Произведен сравнительный анализ аминокислотного состава и ароматических профилей молодого светлого пива из ячменного солода, полученного путем сбраживания низовыми и верховыми дрожжами с использованием различных способов отварочного затирания. Объектами исследования являлись следующие образцы: 1 - затирание отварочным способом с дополнительной β-амилазной паузой, сбраживание низовыми дрожжами расы SafLagerW34/70; 2 - затирание классическим отварочным способом, сбраживание на низовых дрожжах, расы SafLagerW34/70 (контроль 1); 3 - затирание классическим отварочным способом, сбраживание на верховых дрожжах, расы SafAleT58 (контроль 2); 4 - затирание отварочным способом с дополнительной β-амилазной паузой, сбраживание верховыми дрожжами расы SafAleT58. В полученных образцах были определены массовые концентрации аминокислот, сложных эфиров и высших спиртов, оказывающих влияние на формирование ароматического профиля. В образцах, молодого пива, сброженных лагерными дрожжами расы SafLagerW34/70, наблюдали, что в образце 1 содержание этилацетата составило 20 мг/дм3, что в 2 раза больше, чем в образце 2. В тоже время, при исследовании образцов молодого пива, полученного сбраживанием на элевых дрожжах SafAleT58, в образце 4 содержание этилацетата составило 49,1 мг/дм3, что в 2 раза выше контрольного образца 3. На основе полученных результатов были сделаны выводы о возможности применения одноотварочного затирания с дополнительной β-амилазной паузой в технологии светлого пива из ячменного солода.
Затирание, дрожжи, пиво, солод, качественные показатели
Короткий адрес: https://sciup.org/140305661
IDR: 140305661 | УДК: 640 | DOI: 10.20914/2310-1202-2024-1-144-154
Effect of the cooking method on the composition of young light beer
Currently, beer producers are faced with the problem of price/quality ratio when working with domestic malt and hops. Therefore, it becomes relevant to study technological methods that affect raw materials in order to regulate the quality indicators of finished products. A comparative analysis of the amino acid composition and aromatic profiles of young light beer from barley malt, obtained by fermentation with bottom and top yeast using various methods of decoction mashing, was carried out. The objects of the study were the following samples: 1 - mashing by decoction with an additional β-amylase pause, fermentation with grassroots yeast of the SafLagerW 34/70 race; 2 - mashing using the classic decoction method, fermentation with bottom yeast, race SafLagerW 34/70 (control 1); 3 - mashing using the classic decoction method, fermentation with top yeast, race SafAleT 58 (control 2); 4 - mashing by decoction with an additional β-amylase pause, fermentation with top yeast of the SafAleT 58 race. In the resulting samples, the mass concentrations of amino acids, esters and higher alcohols that influence the formation of the aromatic profile were determined. In samples of young beer fermented with lager yeast of the SafLagerW 34/70 race, it was observed that in sample 1 the ethyl acetate content was 20 mg/dm3, which is 2 times more than in sample 2. At the same time, when studying samples of young beer, obtained by fermentation with SafAleT 58 ale yeast, in sample 4 the ethyl acetate content was 49.1 mg/dm3, which is 2 times higher than control sample 3. Based on the results obtained, conclusions were drawn about the possibility of using single-decoction mashing with an additional β-amylase pause in the technology light beer made from barley malt.
Текст научной статьи Влияние способа отварочного затирания на состав молодого светлого пива
В настоящее время, в условиях ограниченного импорта сырья для производства пива отрасль стала испытывать определенные трудности. Безусловно, в Российской Федерации, выращивают ячмень и производят солод. Государство уделяет внимание выведению новых сортов ячменя для пивоварения, освоению новых площадей для его выращивания, строительству солодовен и осуществляет субсидирования таких программ. Однако, производители пива, так или иначе, сталкиваются с проблемой соотношения цена/качество при работе с отечественным солодом и хмелем. Поэтому актуальным становится изучение технологических приемов, влияющих на сырье, с целью регулирования качественных показателей готовой продукции.
Затирание при производстве пива является одним из ключевых этапов в технологии. Правильное проведение этого процесса позволяет избежать проблемы с брожением и коллоидной стабильностью напитка, получить продукцию высокого качества [1].
Затирание может проводится настойным и отварочным способами. В настоящее время, инфузионные способы более востребованы, так как программирование процесса при этом является наиболее реализуемым по сравнению с декок-ционными. В то же время, многие иностранные пивоварни настаивают на установке дополнительного процесса отваривания чтобы иметь возможность решать проблемы с процессом затирания в случаях, когда качество солода не соответствует стандартам. Процесс отваривания по-прежнему используется примерно на 40% всех пивоварен Европы [1].
Классический одноотварочный декокцион-ный процесс отварки пива происходит следующим образом: начинают затирание при температуре 35°С медленно нагревают до 52°С и выдерживают белковую паузу при этой температуре, после этого весь затор нагревают до 63°С и выдерживают мальтозную паузу. Затем отделяют отварку и кипятят её 15–30 мин, после чего добавляют к остатку затора и происходит повышение температуры до 72°С с последующим осахариванием. На следующем этапе затор нагревается до 78°С – «маш аут» (для деактивации ферментов) и перекачивается на фильтрацию [6].
Известен отварочный способ, предложенный Маркусом Херрманном, для пшеничного пива. Его особенность заключается в том, что часть затора нагревается до температуры осахаривания с соблюдением всех пауз, а другая часть затирается с холодной водой и на стадии осахаривания добавляется к основной части, тем самым снижается температура затора до 63°С – мальтозная
На наш взгляд, представляет научный и практический интерес исследование влияния дополнительной β-амилазной паузы в процессе отварочного затирания при производстве светлого ячменного пива.
Следует учитывать тот факт, что пшеничное пиво обычно производят при верховом брожении. Известно, что в зависимости от выбора рас верховых или низовых дрожжей в процессе брожения, получают пивоваренную продукцию отличающуюся между собой по физико-химическим и органолептическим свойствам. Поэтому нами, был проведен сравнительный анализ аминокислотного состава и ароматических профилей молодого светлого пива из ячменного солода, полученного путем сбраживания низовыми и верховыми дрожжами с использованием классического одноотварочного и одноотварочного с дополнительной β-амилазной паузой способов затирания.
Материалы и методы
В лабораторных условиях были получены образцы молодого светлого пива из ячменного солода. Затирание проводили следующим образом: часть затора нагревали до 35°С – кислотная пауза, затем до 52°С – белковая пауза, потом до 63°С – мальтозная пауза, затем добавляли часть затора (отварку) температура которой составляет 95°С, благодаря которой температура повышалась до 72°С выдерживали паузу осахаривания, добавляли другую часть затора с холодной водой, тем самым возвращаясь к мальтозной паузе 63°С (дополнительная β-амилазная пауза), нагревали весь затор до 72°С выдерживали при этой температуре, и доводили до 78°С (маш-аут). Контрольные образцы подвергали классическому одноотварочному способу. Фильтрация затора, охмеление и осветление пивоваренного сусла проводилась в одинаковых условиях. Полученные образцы пивоваренного сусла сбраживали на расах дрожжей компании «Fermentis» – «Saflager W34/70» и «SafAle T-58» при температуре брожения 12°С и температуре дображивания 2°С.
Образцы обозначали следующим образом:
Образец 1 – затирание отварочным способом с дополнительной β-амилазной паузой, сбраживание низовыми дрожжами расы SafLagerW-34/70.
Образец 2 – затирание классическим от-варочным способом, сбраживание на низовых дрожжах, расы SafLagerW-34/70 (контроль № 1).
Образец 3 – затирание классическим от-варочным способом, сбраживание на верховых дрожжах, расы SafAleT-58 (контроль № 2).
Образец 4 – затирание отварочным способом с дополнительной β-амилазной паузой, сбраживание верховыми дрожжами расы SafAleT-58.
Определение аминокислот проводили методом капиллярного электрофореза на анализаторе «Капель 105-М». Ввод пробы происходит при давлении 30 мбар·с. Напряжение электрического поля составляет + 13 кВ. Детектирование осуществляется при длине волны 254 нм.
Определение массовой концентрации высших спиртов и сложных эфиров проводили методом газожидкостной хроматографии на анализаторе «Кристалл 2000М», согласно ГОСТ Р 5793–2017, метод основан на хроматографическом разделении смеси летучих компонентов в продукте и последующем их детектировании пламенноионизационном детектором.
Результаты и обсуждения
На первом этапе исследования был проведен сравнительный анализ аминокислотного состава полученных образцов молодого светлого
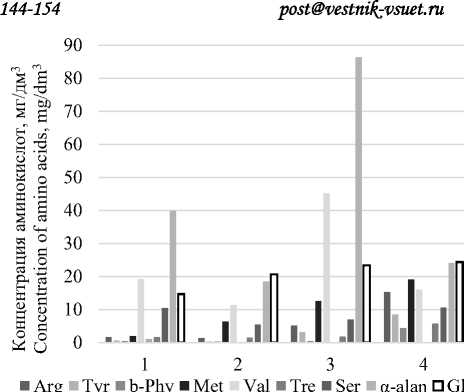
Рисунок 1. Состав аминокислот в молодом светлом пиве, полученном путем сбраживания низовыми и верховыми расами дрожжей, в зависимости от способов затирания
Figure1. Composition of amino acids in young pale beer obtained byfermentation by lower and higher yeast races, depending on the methods ofmashing
Аргинин – алифатическая основная α-ами-нокислота, является одним из предшественников
ячменного пива.
Аминокислоты являются основными структурными компонентами белков. Процесс формирования этих веществ начинается с расщепления белков на составные части. Состав аминокислот в пиве зависит от многих факторов, включая вид солода, его способность к высвобождению аминокислот, технологические режимы при затирании, процессы, протекающие при ферментации пивоваренного сусла.
Аминокислоты в процессе брожения используются дрожжами в разной степени. Так, например, к легкоусвояемым аминокислотам относятся: аспарагин, глютамин, серин, треонин, лизин, аргинин, метионин, изолейцин, лейцин; промежуточное усвояемость – валин, гистидин, триптофан, тирозин, финилаланин, медленная усвояемость – аланин и глицин; практически не усваивается – пролин. От степени использования аминокислот дрожжами в процессе ферментации, зависит их концентрация в готовом пиве [3].
Помимо метаболизма аминокислот, дрожжи способны производить аминокислоты из различных химических веществ-предшественников. Это происходит посредством переаминирования, но обычно, лишь в средах с крайне ограниченными концентрациями аминокислот. Таким путем могут быть получены – валин, изолейцин, фенилаланин, глицин, тирозин, лейцин, гистидин, лизин и аргенин [3].
На рисунке 1 представлен аминокислотый состав образцов молодого пива в зависимости от способа отварочного затирания и расы дрожжей.
аминокислоты гостидина, которая отвечает за обогащение пива ароматическими компонентами. Аргинин может служить источником питательных веществ для дрожжей, тем самым влияя на активность их работы.
Эта аминокислота способствует образованию аминов, участвующих в сложении аромата и вкуса пива. В тоже время, аминовые соединения в больших концентрациях в пиве могут быть причиной горечи и неприятного запаха. При концентрации ниже 50 мг/дм3 аргинин не оказывает негативного влияния на органолептические свойства пива [2].
В образцах молодого пива, полученного сбраживанием лагерными дрожжами расы SafLagerW-34/70 в образце 1 содержание аргинина, составило 1,7 мг/дм3, что на 18% ниже, чем в контрольном образце 2.
При сбраживании пивоваренного сусла элевыми дрожжами расы SafAleT-58 в образце 4 концентрация аргинина составила – 15,26 мг/дм3, что в 3 раза выше, чем в контроле 3.
Экспериментальный способ затирания значительно повлиял на рост концентрации аргинина в молодом пиве, сброженном на элевых дрожжах. При этом его содержание в исследуемых образцах не превышало пороговых значений.
Тирозин – это аминокислота, которая обычно присутствует в зерновых культурах, таких как ячмень и пшеница, которые используются при изготовлении пива. Тирозин активно влияет на процесс брожения, являясь одной из аминокислот, необходимых для роста дрожжей.
Низкое содержание тирозина в пивоваренном сусле может привести к дальнейшим проблемам во время ферментации.
Экспериментально установлено (рисунок 1) что, в образце 1 концентрация тирозина составила – 0,63 мг/дм3, что в 2 раза выше контроля 2.
В молодом пиве, полученном путем верхового брожения (образец 4) концентрация тирозина составила 8,6 мг/дм3, что в 2,6 раза выше, чем в контрольном образце 3.
Бета-фенилаланин, как правило, в пиве содержится в достаточно малых количествах и его влияние на качество готовой продукции несущественно [4].
Исследование опытных образцов показало, что при сбраживании лагерными дрожжами SafLagerW-34/70, в экспериментальном образце 1, концентрация бета-фенилаланина составила – 0,43 мг/дм3, что на 19% выше, чем в контрольном образце 2.
В молодом пиве, полученном путем сбраживания верховыми дрожжами расы SafAleT-58, содержание бета-фенилаланина было равно 4,5 мг/дм3, что равно концентрации в контрольном образце 3.
Метионин – аминокислота, влияющая на аромат пива. Так при брожении, она способствует образованию сульфидов, тиолов и альдегидов.
В образце 1, полученном путем сбраживания лагерными дрожжами расы SafLagerW-34/70, концентрация метионина составила – 2 мг/дм3, что в 3 раза меньше чем в контроле 2.
В молодом пиве верхового брожения при экспериментальном способе затирания содержание метионина равнялось 19,1 мг/дм3, что в 3 раза больше, чем в контрольном образце 3.
Можно предположить, что повышение концентрации метионина в экспериментальных образцах, возможно, будет способствовать образованию ароматических веществ и улучшению аромата пива.
Валин – аминокислота, оказывающая влияние на вкус и аромат пива. В небольших концентрациях может придавать пиву аромат фруктов и цветочные ноты, а при повышенном содержании – горечь.
При сбраживании лагерными дрожжами SafLagerW-34/70, в образце 1 концентрация валина составила – 19,3 мг/дм3, что на 41% выше, чем в контрольном образце 2.
При проведении верхового брожения с дрожжами расы SafAleT-58, в экспериментальном образце 4 концентрация валина была в 3 раза выше контроля 3 и составила – 16 мг/дм3.
Пролин – это аминокислота, образующаяся при гидролизе ячменного гордеина. Содержание пролина в пиве оказывает влияние на его вкус. При высоких концентрациях эта аминокислота может придавать пиву более горький и пряный вкус [3].
В образце, полученном при сбраживании лагерными дрожжами SafLagerW-34/70 содержание пролина составило 884 мг/дм3, что на 13% больше чем в контрольном образце 2.
В образце 4, полученном при верховом брожении, концентрация пролина составила 2275 мг/дм3, что на 47% выше, чем в контрольном образце 3.
Достаточно высокие значения этого показателя в молодом пиве можно объяснить тем, что пролин практически не используется дрожжами.
Треонин – влияет на сахаропреобразующую активность дрожжей, являясь прекурсором фермента, который способствует разложению сложных сахаров на простые. Используется дрожжами для синтеза этилового эфира.
Согласно полученным данным в образце 1 концентрация треонина идентифицирована на уровне 1,73 мг/дм3, что на 15% выше концентрации данной аминокислоты в контрольном образце.
При исследовании образцов пива верхового брожения наблюдали более высокие концентрации треонина: в экспериментальном образце 4 концентрация составила 5,8 мг/дм3, что более чем в 3 раза выше концентрации, установленной в контрольном образце 2.
Серин – является незаменимой аминокислотой, которая играет важную роль в организме человека. Серин не оказывает значительного влияния на качество пива. Синтезируется из глюкозы, в процессе брожения.
При исследовании образцов пива, полученного низовым способом, концентрация серина в экспериментальном образце 1 идентифицирована на уровне 10,54 мг/дм3, что в 2 раза превышает уровень, установленный в контрольном образце.
В то же время, в образцах, полученных верховым брожением, концентрация серина в экспериментальном образце 4 составила 10,6 мг/дм3, что на 30% больше, чем в контроле 3.
Известно, что α-аланин – является важным аминокислотным источником для дрожжей во время брожения. Она образуется в процессе разложения белка во время затирания и способствует формированию фруктовых нот и ароматов специй. Аланин играет роль в регулировании pH и цвета пива. Может быть использован для контроля уровня кислотности во время брожения. Является одним из компонентов, улучающих стабильность и плотность пены [5].
В образцах пива, полученного низовым способом, концентрация α-аланина в экспериментальном образце 1 составила 39,8 мг/дм3, что в 2 раза выше, чем в контрольном образце 2.
В то же время, при исследовании молодого пива, полученного верховым брожением, концентрация α-аланина в опытном образце 4 составила 24,12 мг/дм3, что в 3,3 раза превышает уровень α-аланина в контрольном образце.
Глицин – это аминокислота, которая благоприятно влияет на показатели пива. Глицин обладает сладким вкусом, который может смягчить горечь, делая пиво более приятным для потребления, повышает вязкость и стабильность пены [6].
При исследовании образцов пива, полученного низовым способом, установлено, что концентрация глицина в экспериментальном образце 1 составила 14,6 мг/дм3, что на 30% ниже, по сравнению с контрольным образцом 2.
В образцах, полученных верховым брожением, концентрация глицина в экспериментальном образце 4 составила 24,34 мг/дм3, что сопоставимо с концентрацией, идентифицированной в контрольном образце 3.
Таким образом, согласно полученным экспериментальным данным способ затирания способствует повышению концентрации тирозина, метеонина, валина, треонина, α-аланина в продукции. При чем эта тенденция более характерна для пива верхового брожения. При этом следует отметить тот факт, что полученные результаты согласуются с литературными данными [3]. Из чего следует, что аминокислотный профиль исследуемых образцов является вполне типичным и анализируемый способ затирания не приводит к экстремальному повышению уровня аминокислот.
На следующем этапе исследования был проведен сравнительный анализ ароматических профилей полученных образцов молодого светлого ячменного пива.
Ароматический профиль пива формируется благодаря различным классам химических веществ, таким как высшие спирты, сложные эфиры, жирные кислоты, карбонильные соединения, соединения серы, фурановые соединения, монотер-пенолы, C 13 -ноизопреноиды и летучие фенолы [7].
Ключевыми факторами в технологии пивоварения, влияющими на образование ароматических веществ, являются: выбор сырья – качество хмеля и солода, образование побочных продуктов метаболизма дрожжей, присутствие загрязняющей микрофлоры и трансформации вкусо – ароматических соединений при хранении продукта [8].
При различном качестве солода важным аспектом является правильный выбор технологических режимов затирания. Путем регулирования параметров данного процесса возможно оказывать влияние на физико-химические свойства пива, в том числе на формирование его ароматического профиля.
Согласно исследованиям, проведенным Маркусом Херманном, при производстве пшеничного пива благодаря введению дополнительной β-амилазной паузы происходят следующие процессы: мальтоза, необходимая для реакции, производится первым затором, который осахаривают; фермент мальтаза уже инактивирован в этом заторе, при добавлении части затора с холодным наливом, добавляется и начинает действовать мальтаза, когда затор остывает, происходит мальтазная реакция. Это приводит к сдвигу соотношения сахаров мальтоза: глюкоза в пивоваренном сусле в сторону глюкозы [9].
При этом параллельные исследования процесса брожения искусственных сред показали что, дефицит глюкозы в растворе приводит к экспрессии ацетилалкоголтрансфераз. Увеличение же концентрации глюкозы, отодвигает момент времени возникновение дефицита этого сахара. При такой же или ускоренной пролиферации дрожжевых клеток, основанной на глюкозе, значительная доля дрожжей испытывает эту стрессовую ситуацию, и поэтому может образовываться больше ацетилспирттрансфераз. А клетки дрожжей, образовавшиеся после перехода на мальтозное брожение, не испытывают этой стрессовой ситуации. Поэтому образование сложных эфиров в пиве идет интенсивнее при сдвиге сахаров в пивоваренном сусле в сторону глюкозы [9].
Сложные эфиры являются побочным продуктом алкогольного брожения. Поэтому их качественный и количественный состав во многом зависит от условий проведения процесса брожения и расы дрожжей. Известно, что при использовании рас верховых дрожжей содержание сложных эфиров в пиве выше [9].
В умеренных количествах сложные эфиры способны придать приятный, насыщенный вкус и тонкий аромат готовому продукту. Однако, их избыток может вызывать в пиве чрезмерный фруктовый запах [10].
В основном выделяют две группы эфиров в сброженных напитках. Первая группа представлена ацетатными эфирами (в которых кислотная группа ацетат, а спиртовая группа представляет собой этанол или сложный спирт, полученный в результате метаболизма аминокислот), например этилацетат, изоамилацетат и фенилэтилацетат. Вторая группа – этиловые эфиры (в которых спиртовая группа представляет собой этанол, а кислотная группа представляет собой жирные кислоты), например, этилгексаноат, этилоктонат и этилдеканоат. Этилацетат обычно присутствует в наибольшей степени, и его концентрация составляет примерно треть всех сложных эфиров в пиве [11].
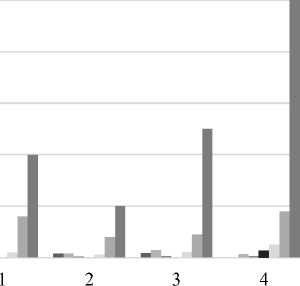
На рисунке 2 представлено изменение концентрации сложных эфиров в молодом светлом ячменном пиве, обусловленное выбором способа затирания и расы дрожжей.
■ Этиллактат
Ethyl lactate ■ Метилацетат
Этилвалериат
Этилкапринат Ethylcaprinate Этилацетат
Ethyl acetate
■ Этилкапроат Ethylcaproate Этилкаприлат Ethylcaprylate
Methyl acetate
Рисунок 2. Состав сложных эфиров в молодом светлом пиве из ячменного солода в зависимости от расы дрожжей и способов затирания
Figure 2. Composition of esters in young pale barley malt beer depending on yeast race and mashing methods
Экспериментально установлено, что номинальная концентрация эфиров в молодом ячменном пиве, зависит от способа затирания и расы дрожжей.
Этилацетат и метилацетат, идентифицированные в исследуемых образцах, относятся к ацетатным эфирам пива. Концентрации ацетатных эфиров всегда выше в напитках в сравнении с другими летучими эфирами. Образование этих веществ происходит за счет действия ферментов дрожжей и во многом зависит от выбранной расы. Наряду с этим следует учитывать влияние состава сахаров пивоваренного сусла. Так более высокий уровень глюкозы в сусле повышает содержание ацетил-КоА, который является основным субстратом для синтеза ацетатных эфиров [8].
Пороговым значением по аромату для этилацетата в лагерном пиве является 25–30 мг/дм3 [12], в элевом – 50 мг/дм3 [3]. В небольших концентрациях этот сложный эфир придает готовому продукту умеренные фруктовые ноты, легкий аромат леденцов [13]. При содержании этилацетата в пиве выше указанных значений может появиться неприятный запах растворителя, а при многогократном превышении – резкий яблочный или уксусный вкус, что считается дефектом качества [14].
В образцах, молодого пива, сброженных лагерными дрожжами расы SafLagerW-34/70, наблюдали, что в экспериментальном образце 1 содержание этилацетата составило 20 мг/дм3, что в 2 раза больше, чем в контрольном образце 2.
В тоже время, при исследовании образцов молодого пива, полученного сбраживанием на элевых дрожжах SafAleT-58, в экспериментальном образце 4 содержание этилацетата составило 49,1 мг/дм3, что в 2 раза выше контрольного образца 3.
Метилацетат в зависимости от концентрации придает пиву фруктовый вкус и аромат. Его пороговая концентрация по аромату составляет 10 мг/дм3 [9].
В молодом пиве низового брожения при экспериментальном способе затирания, в образце 1 содержание метилацетата составило 4 мг/ дм3, что в 2 раза больше, чем в контрольном образце 2.
При исследовании образцов пива верхового брожения, в экспериментальном образце 4, концентрация метилацетата составила 9 мг/дм3, что в 2 раза выше, чем в контрольном образце 3.
Увеличение этилацетата и метилацетата в экспериментальных образцах, можно объяснить тем, что вероятнее всего дополнительная β-амилазная пауза, привела к увеличению содержания глюкозы в пивоваренном сусле, что повысило содержание ацетил-КоА и способствовало увеличению их синтеза.
В исследуемых образцах также были идентифицированы сложные эфиры этиловой группы – этилкаприлат, этилкапринат, этилвале-риат, этилкапроат и этиллактат. Их содержание всегда значительно ниже в сравнении с эфирами ацетатной группы, однако качественный и количественный состав имеет значение для формирования ароматного профиля пива.
Образование сложных эфиров этиловой группы во многом зависит от генома дрожжей, их способности вырабатывать ферменты способствующие синтезу этих веществ. В то же время, с точки зрения качественного состава сложных эфиров, имеют значения реакции этерификации и переэтирификации [12].
К снижению уровня этиловых эфиров в пиве приводит увеличение концентрации жирных кислот в ферментационной среде [12].
При концентрации ниже 5 мг/дм3 этилка-прилат может придать пиву аромат яблок. Так же это вещество способно оказывать влияние на стабильность и сохранность пива [9].
В молодом пиве низового брожения при экспериментальном способе затирания, в образце 1 содержание этилкаприлата составило 1 мг/дм3, что почти в 2 раза выше, чем в контрольном образце 2.
При исследовании образцов пива верхового брожения, в экспериментальном образце 4, концентрация этилкаприлата составила 2,49 мг/дм3, это в 2,5 раза выше, чем в контрольном образце 3.
Этилкапринат – эфир этилового спирта и капроновой кислоты, при содержании в пиве способен придавать ему аромат сливок и привкус сиропа, что является желательным для некоторых стилей пива. Пороговым значением по аромату для этого вещества является 0,5 мг/дм3 [14].
Этилкапринат был идентифицирован только в экспериментальном образце 4 в количестве – 1,4 мг/дм3. Так как концентрация этого вещества превышает пороговое значение по аромату почти в 3 раза, можно заключить, что это окажет значительное влияние на органолептику данного образца.
При содержании этилвалериата в пиве до 5 мг/дм3, данный эфир способствует появлению фруктовых, цветочных и сладких ароматов, добавляет сложности и глубины вкуса готовой продукции. Также присутствие этого вещества, может увеличить длительность послевкусия, делая пиво более сложным и насыщенным [4].
В образцах молодого пива, сброженных низовыми дрожжами расы SafLagerW-34/70, наблюдали следующее: в образце 1 – концентрация этилвалериата составила 0,8 мг/дм3, что равняется концентрации в контрольном образце 2.
В то же время, в молодом пиве сброженном верховыми дрожжами расы SafAleT-58, в образце 4 этилвалириат находился на уровне менее 0,1 мг/дм3, а в контроле 3 его концентрация составила 0,85 мг/дм3.
Этилкапроат – это эфир капроновой кислоты, образующийся в результате брожения, который имеет аромат анисовых семян, при повышении концентрации проявляются яблочные ноты во вкусе и аромате. Пороговое значение по аромату составляет 0,3 мг/дм3 [4, 15].
При исследовании образцов, полученных низовым способом с применением дрожжей расы SafLagerW-34/70, концентрация этилкапроата в образце 1 составила 1,4 мг/дм3, что более чем наполовину выше по сравнению с контролем 2.
В образцах молодого пива, полученных верховым брожением с применением дрожжей расы SafAleT-58, концентрация этилкапроата в образце 4 составила 1,54 мг/дм3, что так же более, чем на половину выше по сравнению с контрольным образцом 3.
Этиллактат – сложный эфир, который в небольших количествах, может вносить в аромат пива тона сливок и участвовать в сложении вкуса. Пороговое значение по аромату составляет 0,9 мг/дм3 [14].
В молодом пиве, полученным сбраживанием низовыми дрожжами расы SafLagerW-34/70, концентрация этиллактата составила 0,35 мг/ дм3, что на 50% выше, чем в контроле 2.
В молодом пиве верхового брожения, с применением дрожжей расы SafAleT-58, в образце 4 содержание этиллактата составило 0,26 мг/ дм3, что соответствует концентрации в контрольном образце 3.
Таким образом, при исследовании качественного и количественного состава этиловой группы сложных эфиров, можно заключить, что в элевых образцах данные компоненты накапливаются в более высоких концентрациях, это согласуется с литературными данными [15]. В то же время при сравнении контрольных и опытных образцов, было выявлено, что на концентрации этиловых сложных эфиров способ затирания оказывал незначительное влияние, за исключением этилкапроата, этилка-прилата и этилкаприната.
Известно, что высшие спирты являются компонентами, оказывающими значительное влияние на ароматический профиль пива. Их образование может происходить двумя путями: катаболическим и анаболическим. Первый путь, также называемый «путь Эрлиха» предусматривает, что пивные дрожжи, поглощают аминокислоты, присутствующие в пивоваренном сусле, отщепляют аминогруппу для включения ее в собственную структуру, при этом оставшаяся часть молекулы трансаминируется с образованием α-кетокислоты с последующим декарбоксилированием и восстановлением, в результате чего образуется спирт, содержащий на один атом углерода меньше, чем потребленная аминокислота. Таким образом, например, из изолейцина образуется изоамиловый спирт [12]. Анаболический путь связан с биосинтезом аминокислот. При этом предпоследней реакцией является образование соответствующей α-кетокислоты из пирувата и ацетил-КоА. Затем, происходит декарбоксилирование и восстановление этих α-кето-кислот с образованием высших спиртов [12, 16].
На содержание в пиве высших спиртов влияет ряд факторов: раса дрожжей; температура брожения, так как при ее повышении ускоряется поглощение аминокислот дрожжевыми клетками и усиливается синтез высших спиртов; содержание свободного аминного азота в сусле.
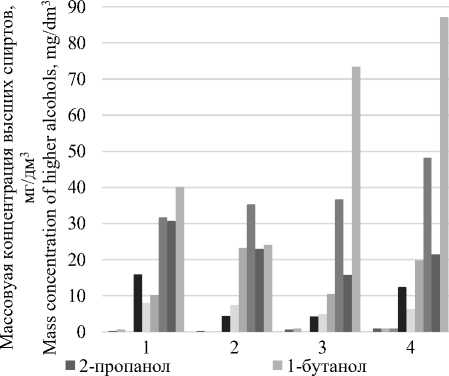
На рисунке 3 представлено изменение концентрации высших спиртов в молодом светлом ячменном пиве, обусловленное выбором способа затирания и расы дрожжей.
Изоамиловый спирт образуется в результате метаболизма дрожжевых клеток в процессе брожения. Поэтому его содержание в пиве во многом зависит от аминокислотного состава сусла, расы дрожжей, температуры брожения [16]. Он имеет специфический аромат, который может влиять на органолептические свойства пива. Пороговое значение по аромату для данного вещества составляет 50–60 мг/дм3. В тоже время в зависимости от стиля пива его содержание может колебаться в пределах от 25 до 120 мг/дм3, последнее более характерно для элей. При небольших концентрациях изоамиловый спирт придает готовому пиву фруктовые ноты, в частности аромат банана [12, 16, 17]. Однако в количествах значительно превышающих вышеуказанные значения, может придать пиву спиртовой и винный запах [16].
2-propanol 1-butanol
■ Бензиловый спирт ■ 1-гексанол
Benzyl alcohol 1-hexanol
Октанол ■ 1-пропанол
Octanol 1-propanol
Рисунок 3. Состав высших спиртов в молодом светлом пиве из ячменного солода в зависимости от расы дрожжей и способов затирания
Figure3. Composition of higher alcohols in young light beer from barley malt depending on yeast race and mashing methods
В образцах молодого пива, полученного низовым способом брожения с применением дрожжей расы SafLager W-34/70, концентрация изоамилового спирта в образце 1 составила 40,2 мг/дм3, существенно выше контрольного образца 2.
В образцах, полученных верховым способом брожения с применением дрожжей расы SafAle T-58, концентрация изоамилового спирта составила 87 мг/дм3, что несколько превышает уровень концентрации образца 3.
Изобутанол производится дрожжами первоначально в цитоплазме по пути Эрлиха или путем анаболического синтеза внутри митохондрий. Этот высший спирт способен придавать пиву запах растворителя. Пороговое значение по аромату изобутанола составляет 100 мг/дм3 [16].
Согласно проведенным исследованиям при низовом брожении концентрация изобутанола в образце 1 составила 30,7 мг/дм3, что на 30% выше, контроля.
При использовании расы дрожжей SafAle T-58 в образце 4 изобутанол содержался в количестве 21,5 мг/дм3, что на 36% больше, чем в образце 3.
Исходя из полученных данных можно заключить, что содержание изоамилового и изобутилового спиртов в экспериментальных образцах повысилось, что вероятнее всего может быть связано с изменением аминокислотного состава сусла при введении дополнительной β-амилазной паузы, в результате которой увеличилось количество аминокислот – прекурсоров.
Известно, что β-фенилэтанол – это ароматический спирт, содержание которого может влиять на качество пива. В небольших количествах β-фенилэтанол придает пиву медовый аромат или лёгкий аромат розы. Однако слишком высокие концентрации данного компонента могут привести к появлению аромата гвоздики, что является нетипичным для лагерного пива, однако может иметь место при производстве верхового пива. Предельно допустимая концентрация, не оказывающая негативного действия на аромат, для лагерей составляет порядка 25 мг/дм3 [5].
В образцах, полученных низовым брожением, с применением дрожжей расы SafLager W-34/70, содержание β-фенилэтанола (в образце 1) составило 31,7 мг/ дм3, что несколько превышает уровень концентрации в контрольном образце 2.
В образцах пива, полученного верховым способом брожения (в образце 4) концентрация β-фенилэтанола составила 48,2 мг/дм3, что уже существенно выше, чем в контрольном образце 3.
Опираясь на полученные экспериментальные данные можно предположить, что опытные образцы 1 и 4 имеют потенциал формирования выраженных медовых оттенков в готовом продукте, что приветствуется для элевого пива, но нежелательно для лагерных стилей.
Известно, что 1-пропанол является одним из многочисленных соединений, которые также могут быть образованы в процессе брожения, он является побочным продуктом метаболизма дрожжей. Содержание 1-пропанола в пиве может придать ему слегка сладковатые тона в аромате. В элях 1-пропанол может содержаться в больших количествах, чем в лагерах. Предельно допустимая концентрация, не влияющая отрицательно на вкусовые характеристики пива, составляет до 100 мг/дм3 [18].
В образцах молодого пива, сброженных низовыми дрожжами расы SafLager W-34/70 наблюдали следующее: в образце 1 концентрация 1-пропанола составила – 10,2 мг/дм3, что в 2 раза выше контрольного образца 2. При этом пороговое значение по аромату для низового пива составляет 50 мг/дм3.
В то же время, в молодом пиве сброженном верховыми дрожжами расы SafAle T-58, концентрация 1-пропанола в образце 4 составила 19,8 мг/дм3, что в 2 раза выше контрольного образца 3.
Согласно приведенным данным, можно констатировать, что применение при затирании дополнительной β-амилазной паузы приводит к увеличению концентраций 1-пропанола, что, возможно, связано с трансформацией аминокислотного состава пивоваренного сусла экспериментальных образцов.
Октанол – органическое вещество, относящееся к классу жирных спиртов. В зависимости от концентрации, он может придавать пиву свежий фруктовый аромат, сладковатый, слегка ореховый вкус. Октанол также способен выполнять роль антиоксиданта и консерванта – предотвращать окисление пива и продлять срок его годности [4].
При исследовании образцов, полученных низовым способом с применением дрожжей расы SafLagerW-34/70, концентрация октанола в образце 1 составила 8 мг/дм3, что несколько выше по сравнению с контролем 2.
В то же время, в образцах молодого пива, полученных верховым брожением с применением дрожжей расы SafAleT-58, концентрация октанола в образце 4 составила 6,4 мг/дм3, что более чем на 20% выше по сравнению с контрольным образцом 3.
Таким образом, полученные данные свидетельствуют о том, что экспериментальный способ затирания не оказывает существенного влияния на изменение концентрации октанола в пиве.
Содержание 1-гексанола в пиве в большей степени зависит от качества сырья, в том числе сорта хмеля. Могут оказывать влияния и режимы кипячения сусла с хмелем. При концентрации более 75 мг/дм3 гексанол может оказывать негативное влияние на качественные свойства пива: придавать запах и привкус муки, горечь во вкусе, снижать стабильность пены и сроки хранения продукта [4.16]. При более низких концентрациях 1-гексанол может придавать напитку легкие фруктовые ноты, аромат свежескошенной травы [19].
При исследовании образцов пива, полученного низовым брожением с применением дрожжей расы SafLagerW-34/70, концентрация 1-гексанола в образце 1 составила 15,9 мг/дм3, что в 3,5 раза выше, чем в контрольном образце 2.
В образцах, полученных с помощью верхового брожения и с применением дрожжей расы SafAleT-58, концентрация в образце 4 составила 12,4 мг/дм3, что в 3 раза выше, чем в контрольном образце 3.
Количество 1-гексанола в исследуемых образцах значительно увеличилось, однако не превысило порогового значения (75 мг/дм3), что может свидетельствовать о его положительном влиянии на ароматический профиль молодого пива.
Бензиловый спирт – простейший ароматический спирт, в пиве имеет сладковатый цветочный аромат, похожий на жасмин. Предельно допустимая концентрация составляет 10 мг/дм3[18].
Бензиловый спирт был идентифицирован на уровне выше 0,1 мг/дм3 только в экспериментальном образце 4, и его концентрация составила 0,9 мг/ дм3.
1-бутанол – высший спирт, в малых количествах придает глубину и сложность аромату пива, но в больших концентрациях, может давать готовому продукту неприятные запахи, напоминающие резину или растворитель [18–20].
В образцах молодого пива, сброженном низовыми дрожжами расы SafLagerW-34/70, в экспериментальном образце 1 концентрация 1-бутанола составила 0,7 мг/дм3, в контрольном образце 1-бутанол не был идентифицирован.
При брожении верховыми дрожжами расы SafAleT-58, концентрация 1-бутанола в образцах 3 и 4 была одинаковой и составила 0,9 мг/ дм3.
2-Пропанол (изопропиловый спирт) – побочный продукт ферментации дрожжей, может оказывать влияние на вкус пива, придавая аромат алкоголя, вызывая чувство жжения на языке. Пороговое значение по аромату изопорпило-вого спирта составляет 0,5 мг/дм3 для низовых дрожжей и 1 мг/дм3 для верхового брожения [18].
В молодом пиве, полученном сбраживанием низовыми дрожжами расы SafLagerW-34/70, концентрация 2-пропанола составило 0,3 мг/дм3, что немного выше, чем в контроле 2.
В молодом пиве верхового брожения, с применением дрожжей расы SafAleT-58, в образце 4 содержание 2-пропанола составило 0,9 мг/ дм3, что несколько превышает его концентрацию в контрольном образце 3.
Заключение
На основании результатов проведенных экспериментальных исследований можно сделать следующие выводы:
-
1) Экспериментально, установлено, что применение дополнительной β-амилазной паузы в процессе одноотварочного затирания способствует увеличению содержания ряда аминокислот, являющихся прекурсорами аро-матобразующих компонентов, это в свою очередь оказывает влияние на формирование ароматического профиля.
-
2) Показано, что дополнительная β-ами-лазная пауза приводит к увеличению концентрации сложных эфиров и высших спиртов
Оселедцева И.В. и др.Вестник ВГУИТ, 2024, Т. 86, №. 1, С. в молодом пиве, полученном путем сбраживания как верховыми так и низовыми дрожжами.
-
3) Экспериментально доказано, что оптимальное соотношение концентраций сложных эфиров и высших спиртов формируется при реализации в исследуемых условиях варианта верхового брожения.
-
5) Установлено, что применение отвароч-ного затирания с дополнительной β-амилазной паузой при производстве светлого пива оказывает существенное влияние на состав ароматических компонентов, что в свою очередь позволяет регулировать и корректировать при необходимости ароматический профиль пива.
Список литературы Влияние способа отварочного затирания на состав молодого светлого пива
- Bettenhausen H.M. et al. Influence of malt source on beer chemistry, flavor, and flavor stability // Food research international. 2018. V. 113. P. 487-504.
- Кобелев К.В., Гернет М.В., Грибкова И.Н., Лазарева И.В. Исследование влияния состава сырья на качество и безопасность готового пива. Часть III. Влияние состава зернового и сахаросодержащего сырья на содержание органических кислот и углеводов в пиве // Пиво и напитки. № 4. 2015. URL: https://cyberleninka.ru/article/n/issledovanie-vliyaniya-sostava-ishodnogo-syrya-na-kachestvo-i-bezopasnost-gotovogo-piva-chast-iii-vliyanie-sostava-zernovogo-i/viewer
- Koller H., B. Perkins L. Brewing and the Chemical Composition of Amine-Containing Compounds in Beer // Foods 2022. V. 11. № 3. doi: 10.3390/foods11030257
- Меледина Т.В., Дедегкаев А.Т., Афонин Д.В. Качество пива: стабильность вкуса и аромата, коллоидная стойкость, дегустация. Санкт-Петербург: Профессия, 2011. 220 с.
- Нарцисс Л. Краткий курс пивоварения. СПб.: Профессия, 2007. 640 с.
- Кунце В., Мит Г. Технология солода и пива. СПб.: Профессия, 2001. 912 с.
- Rodrigues F., Caldeira M., Câmara J.S. Development of a dynamic headspace solid-phase microextraction procedure coupled to GC–qMSD for evaluation the chemical profile in alcoholic beverages // Analytica Chimica Acta. 2008. V. 609. №. 1. P. 82-104.
- Olaniran A.O., Hiralal L., Mokoena M.P., Pillay B. et al. Flavour‐active volatile compounds in beer: production, regulation and control // Journal of the Institute of Brewing. 2017. V. 123. №. 1. P. 13-23.. doi: 10.1002/jib.389
- Baiano A. Craft beer: An overview // Comprehensive reviews in food science and food safety. 2021. V. 20. №. 2. P. 1829-1856. doi: 10.1111/1541-4337.12693
- Rodrigues F., Caldeira M., Camara J.S. Development of a dynamic headspace solid-phase microextraction procedure coupled to GC–qMSD for evaluation the chemical profile in alcoholic beverages // Anal. Chim. Acta. 2008. V. 609. P. 82–104.
- Saerens S.M.G., Delvaux F., Verstrepen K.J., van Dijck P. et al. Parameters affecting ethyl ester production by Saccharomyces cerevisiae during fermentation // Appl. Environ. Microbiol. 2008. V. 74. P. 454–461.
- Pires E.J., Teixeira J.A., Brányik T., Vicente A.A. Yeast: The soul of beer’s aroma—A review of flavour-active esters and higher alcohols produced by the brewing yeast // Applied microbiology and biotechnology. 2014. V. 98. P. 1937-1949. URL: esearchgate.net/publication/259566009
- Betancur M.I., Motoki K., Spence C., Velasco C. Factors influencing the choice of beer: A review // Food Research International. 2020. V. 137. P. 109367.
- Ferreira I.M., Guido L.F. Impact of wort amino acids on beer flavour: A review // Fermentation. 2018. V. 4. №. 2. P. 23. doi: 10.3390/fermentation4020023
- Humia B.V., Santos K.S., Barbosa A.M., Sawata M. et al. Beer molecules and its sensory and biological properties: A review // Molecules. 2019. V. 24. №. 8. P. 1568. URL: https://pubmed.ncbi.nlm.nih.gov/31009997/
- Зипаев Д.В., Никитченко Н.В., Кашаев А.Г., Платонов И.А. и др. Исследование показателей качества светлого пива, полученного с использованием солода из тритикале // Известия высших учебных заведений. Пищевая технология. 2015. №. 5-6. С. 77-79.
- Харламова Л.Н., Волкова Т.Н., Лазарева И.В., Селина И.В. и др. Исследование содержания летучих компонентов и глицерина в пиве и пивных напитках // Пищевая промышленность. 2020. № 8. С. 48–51.
- Пономарева О.И., Борисова Е.В., Прохорчик И.П. Молочнокислые бактерии рода Lactobacillus в формировании вкусоароматического профиля кислых элей // Техника и технология пищевых производств. 2018. Т. 48. №. 2. С. 100-108. URL: https://cyberleninka.ru/article/n/molochnokislye-bakterii-roda-lactobacillus-v-formirovanii-vkusoaromaticheskogo-profilya-kislyh-eley/viewer
- Сайфуллина Р.Ф., Матушкина Е.В. Исследование качества светлого пива отечественного и импортного производства // Молодежь и наука. 2015. №. 1. С. 21-21.
- Жуков Р.Б. Физико-химические показатели качества пива // Инновационные технологии пищевых производств. 2020. С. 172-175.


