Выбор хирургического доступа при остеосинтезе переломов дистального метаэпифиза большеберцовой кости
Автор: Кошкин А.Б., Паршиков М.В., Ярыгин Н.В., Говоров М.В.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Новые технологии
Статья в выпуске: 1 т.32, 2026 года.
Бесплатный доступ
Введение. Выбор оптимального хирургического доступа при остеосинтезе внутрисуставных переломов дистального метаэпифиза большеберцовой кости (переломов пилона) остается сложной задачей. Ни один из существующих доступов не обеспечивает полной визуализации суставной поверхности, что увеличивает риск осложнений и неудовлетворительной репозиции. Цель работы — оптимизировать выбор хирургического доступа при предоперационном планировании погружного остеосинтеза внутрисуставных переломов дистального метаэпифиза большеберцовой кости (пилона) на основе 3D-прототипирования и стандартизированной разметки суставной поверхности. Материалы и методы. Разработан алгоритм, основанный на создании полноразмерного 3D-прототипа по данным КТ. Суставную поверхность большеберцовой кости разделяли на девять стандартных зон. Хирургический доступ выбирали в зависимости от локализации ключевого фрагмента (занимающего > 2/3 зоны) или точки выхода линии перелома. Метод применили у 12 пациентов с переломами пилона AO/OTA 43-C. Оценивали время операции, объем кровопотери, качество репозиции (по Burwell – Charnley), функциональные исходы (по шкалам AOFAS и VAS FA) и консолидацию (по mRUST) через шесть месяцев. Результаты и обсуждение. Среднее время операции составило (65,08 ± 7,03) мин, кровопотеря — (119,3 ± 18,51) мл. Раны зажили первично без инфекционных осложнений. Качество репозиции: анатомичное — у восьми, приемлемое — у четырех пациентов. Средние баллы по AOFAS (78,67 ± 8,68) и по VAS FA (41,08 ± 5,05) свидетельствуют о хорошем функциональном восстановлении. Средний балл по mRUST (13,5 ± 1,43) подтверждает полную консолидацию. Предложенный метод объективизирует выбор доступа, устраняя субъективность, позволяет персонализировать вмешательство, комбинируя доступы для оптимальной визуализации всех фрагментов, включая труднодоступные (например, фрагмент Tillaux – Chaput). Заключение. Метод, интегрирующий 3D-планирование и стандартизированную координатную систему, повышает точность репозиции, снижает травматичность и улучшает функциональные исходы лечения пациентов со сложными переломами пилона.
Внутрисуставные переломы, дистальный метаэпифиз большеберцовой кости, перелом пилона, 3D-моделирование, хирургический доступ, остеосинтез, алгоритм выбора
Короткий адрес: https://sciup.org/142247055
IDR: 142247055 | УДК: 616.718.56-001.5-089.227.84-035 | DOI: 10.18019/1028-4427-2026-32-1-107-115
The surgical approach for osteosynthesis of metaepiphyseal fractures of the distal tibia
Introduction The optimal surgical approach is essential for osteosynthesis of intra-articular fractures of the distal tibial metaphysis (pilon fractures). None of the existing approaches provides complete visualization of the articular surface, increasing the risk of complications and inadequate reduction. The objective was to optimize the choice of surgical approach in preoperative planning of internal osteosynthesis of intra-articular fractures of the distal metaepiphysis of the tibia (pilon) based on 3D prototyping and standardized marking of the articular surface. Material and methods An algorithm developed was based on a full-size 3D prototype and CT data. The articular surface of the tibia was divided into nine standard zones. The surgical approach was selected depending on the location of the key fragment (occupying > 2/3 of the zone) or the fracture line exit point. The method was used in 12 patients with AO/OTA 43-C pilon fractures. Surgical time, blood loss, the quality of postoperative fracture reduction categorized according to the Burwell-Charnley criteria, functional outcomes measured with AOFAS and VAS FA grading scales, and radiographic union determined with the mRUST scale were assessed at six months. Results and discussion The mean operating time was (65.08 ± 7.03) min, blood loss was (119.3 ± 18.51) ml. The wounds healed by primary intention without infectious complications. The quality of reduction was anatomical in eight patients and acceptable in four patients. The mean AOFAS (78.67 ± 8.68) and VAS FA (41.08 ± 5.05) scores indicated good functional recovery. The mean mRUST score (13.5 ± 1.43) suggested complete consolidation. The method objectified the surgical approach avoiding subjectivity and allowed for personalized intervention by combining approaches for optimal visualization of all fragments, including hard-to-reach ones (e.g., Tillaux – Chaput fragment). Conclusion The method integrating 3D planning and a standardized coordinate system improves reposition accuracy, reduces morbidity, and improves functional outcomes in patients with complex pilon fractures.
Текст научной статьи Выбор хирургического доступа при остеосинтезе переломов дистального метаэпифиза большеберцовой кости
Остеосинтез переломов дистального метаэпифиза большеберцовой кости (ББК) является операцией с высокими требованиями к квалификации хирурга и оснащению клиники. Для успешного выполнения этой операции необходимо учитывать множество факторов, включая выбор хирургического доступа, технику операции, срок выполнения вмешательства и послеоперационную реабилитацию. Переломы пилона чаще возникают в результате высокоэнергетической травмы, сопровождаются массивным, требующим восстановления разрушением суставной поверхности ББК и тяжелым повреждением мягко-тканного футляра. Поэтому бережное обращение с мягкими тканями в ходе выполнения хирургического доступа является залогом успешного их заживления.
В настоящее время описано большое количество хирургических доступов к дистальному отделу ББК, среди которых выделяют медиальный, переднемедиальный, переднелатеральный, латеральный, заднелатеральный и заднемедиальный. Каждый из этих доступов позволяет визуализировать лишь часть пилона и выполнить репозицию соответствующего фрагмента его суставной поверхности [1]. Концепция стабильности остеосинтеза легла в основу теории колонн. Согласно этой теории, дистальный отдел ББК делится на три колонны (латеральную, медиальную и заднюю), каждая из которых требует отдельной фиксации. Это зачастую диктует необходимость комбинации разных доступов. Основная проблема заключается в том, что увеличение их числа при хирургическом вмешательстве позволяет повысить стабильность создаваемой конструкции, но в то же время существенно увеличивает риск осложнений (инфекции, некрозов мягких тканей, несросшихся переломов), что ставит перед хирургом сложную задачу, — найти оптимальный баланс между надёжностью фиксации и минимальной операционной травмой [2]. Б.А. Майоров с соавт. разработали концепцию «дооперационной визуализации на 360°», которая основана на комплексном анализе рентгенологических и КТ-данных [3]. Эта концепция позволяет детально изучить индивидуальные особенности архитектоники перелома, точно визуализировать все элементы повреждения, определить наиболее рациональные хирургические доступы, а также подобрать и оптимально расположить имплантаты. Подобный подход обеспечивает проведение тщательного и обоснованного предоперационного планирования, что существенно повышает точность хирургического вмешательства. При этом четкого пошагового алгоритма выбора хирургического доступа это исследование не предлагает.
Ключевым моментом при выборе доступа является анализ морфологии перелома. P.A. Cole et al. исследовали распределение линий перелома и расположение основных фрагментов кости в 38 случаях многооскольчатых переломов AO/OTA 43-C3 дистального метаэпифиза ББК и пришли к выводу, что хорошее понимание морфологии перелома должно определять выбор хирургического доступа [4]. Однако в этом исследовании не дано детального объяснения того, как следует выбирать хирургический доступ в зависимости от конкретного распределения линий перелома и костных фрагментов.
H. Kleinetz et al. изучили эффективность четырех хирургических доступов к дистальному отделу ББК (переднемедиального, переднелатерального, заднемедиального и заднелатерального) и влияние инструментальной дистракции на визуализацию суставной поверхности на кадаверном материале [5]. В исследовании авторы использовали стандартизированную методику разметки суставной поверхности для объективной оценки доступности различных анатомических зон через хирургические доступы: суставную поверхность разделяли на сегменты, чтобы можно было количественно оценить, какая часть доступна и соответствует каждому из них. Разметку выполняли в координатной системой на основе анатомических ориентиров (например, переднего и заднего краев суставной поверхности). Каждой зоне присвоен уникальный номер-идентификатор, что позволяло сравнивать доступность областей между разными хирургическими доступами. Для каждого доступа оценивали, какой процент суставной поверхности визуализирован с дистракцией и без неё. Видимые зоны маркировали, затем вычисляли процент доступной поверхности при помощи специального программного обеспечения. Исследователи пришли к выводу о том, что без дистракции большинство доступов обеспечивали крайне ограниченную видимость, при этом максимальную видимость достигали при задне-латеральном доступе (30 %), а минимальную — при переднемедиальном. С дистракцией видимость суставной поверхности значительно увеличивалась, особенно при переднелатеральном (до 72 %) и переднемедиальном (до 63 %) доступах. При этом ни один из них не обеспечивал полной визуализации суставной поверхности.
Результаты применения 3D-планирования хирургического лечения пациентов с переломами дистального метаэпифиза ББК нами подробно изложены в статье М.В. Паршикова с соавт. [6]. По сравнению с традиционными методами, применение 3D-технологий планирования остеосинтеза переломов пилона, включая выбор хирургического доступа, позволило добиться значительного сокращения времени операции, уменьшения интраоперационной кровопотери и снижения лучевой нагрузки. Качество репозиции отломков и функциональные исходы лечения оказались заметно лучше в группе с 3D-моделированием.
Однако при дальнейшем анализе исходов выявлены некоторые ошибки и осложнения, которые можно разделить на три группы:
-
1 — ошибки подготовки и печати 3D-моделей. На начальном этапе возникали проблемы с сегментацией КТ-данных (включение артефактов, пропуск мелких фрагментов), дефекты печати из-за некачественного филамента и некорректной калибровки принтера. Их устраняли ручной коррекцией STL-файлов и использованием более качественных материалов;
-
2 — собственно ошибки планирования хирургического доступа. В 4 % случаев в группе с 3D-моделированием возникала необходимость продления разреза, в то время как в контрольной группе такая необходимость возникла в 7 % случаев;
-
3 — послеоперационные осложнения. У одного пациента группы с 3D-моделированием и двух пациентов контрольной группы наблюдали расхождение краев раны после снятия швов. Во всех случаях ширина расхождения не превышала 3 мм, а протяженность — 2 см. Для лечения использовали кожные стерильные стрипы, повторного наложения швов не потребовалось. Глубоких нагноений ни в одной группе не зарегистрировано.
Если для предупреждения осложнений первой группы (ошибки подготовки и печати 3D-моделей) существуют понятные и эффективные методы, то для профилактики осложнений второй и третьей групп необходимо оптимизировать доступ/ы при хирургическом вмешательстве, выбор которых пока нередко вызывает трудности.
Таким образом, ни один хирургический доступ не является универсальным. Для создания оптимального алгоритма выбора хирургического доступа требуется компромисс между визуализацией и риском осложнений с учётом состояния мягких тканей.
Цель работы — оптимизировать способ выбора хирургического доступа при предоперационном планировании погружного остеосинтеза внутрисуставных переломов дистального метаэпифиза большеберцовой кости (пилона) на основе 3D-прототипирования и стандартизированной разметки суставной поверхности.
МАТЕРИАЛЫ И МЕТОДЫ
Описание метода
В рамках предоперационного планирования на основе данных компьютерной томографии (КТ) изготавливали 3D-прототип по следующей методике: файлы dicom переводили в формат STL, после чего их подавали на печать на 3D-принтер. Далее, используя результаты кадаверного исследования H. Kleinertz et al. [5], на суставной поверхности производили разметку, соединяя крайнюю переднюю точку и крайнюю заднюю точки на дистальной поверхности ББК, прилежащей к внутренней лодыж- ке, и этот отрезок принимали за внутреннюю сторону квадрата. Соответственно внутренней стороне достраивали заднюю, латеральную и переднюю стороны. Полученный большой квадрат делили на девять равных внутренних квадратов, меньших по размерам: переднемедиальный, передне-центральный, переднелатеральный, средне-медиальный, средне-центральный, средне-латеральный, задне-медиальный, задний центральный и задне-латеральный (рис. 1), соответствующих девяти зонам, расположенным на суставной поверхности.
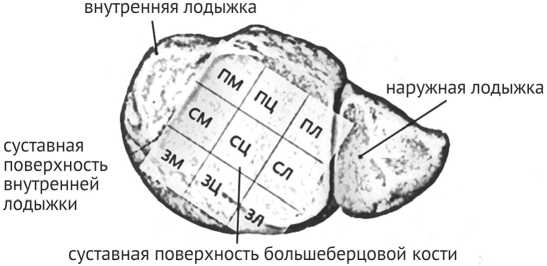
Рис. 1. Разметка суставной поверхности пилона: переднемедиальный (ПМ), передне-центральный (ПЦ), переднелатеральный (ПЛ), средне-медиальный (СМ), средне-центральный (СЦ), средне-латеральный (СЛ), задне-медиальный (ЗМ), задний центральный (ЗЦ), задне-латеральный (ЗЛ)
Выбирали самый крупный фрагмент на суставной поверхности 3D-прототипа (далее — ключевой фрагмент), который ре-понировали в первую очередь и определяли его координаты на разметке. Если более 2/3 фрагмента соответствовали определен- ному квадрату, то его координаты закрепляли за ним. При наличии двух фрагментов одинаковой величины, выбирали два доступа таким же образом. При расположении фрагмента в зоне двух и более квадратов определяли координаты не фрагмента, а точки выхода линии перелома на переднюю или заднюю поверхность. При отсутствии фрагментов площадью, покрывающей более 2/3 фрагментов, применение метода оказалось нецелесообразным, так как в этих случаях показано лечение в компрес- сионно-дистракционном аппарате.
В зависимости от локализации фрагмента и точки выхода линии перелома в определенном квадрате, выбирали доступ из описанных классических доступов АО:
Квадрат
Доступ
Передне-медиальный Передне-центральный Передне-латеральный Средне-медиальный Средне-центральный Средне-латеральный Задне-медиальный Задне-центральный Задне-латеральный
Передне-медиальный
Передне-латеральный
Передне-латеральный
Задне-медиальный
Передне-латеральный, задне-латеральный
Передне-латеральный, задне-латеральный
Задне-медиальный
Задне-латеральный
Задне-латеральный
Исследование проводили на базе отделения травматологии Университетской клиники научно-образовательного института клинической медицины им. Н.А. Семашко Российского Университета Медицины в период с 01.01.2024 по 31.12.2024.
Исследование одобрено Этическим комитетом Российского Университета Медицины (протокол от 15.12.2023 № 12-23).
В исследование включено 12 пациентов с внутрисуставными переломами дистального метаэпифиза ББК (10 пациентов с типом 43С2 и два пациента с типом 43С3). Всем пациентам при поступлении выполнен остеосинтез аппаратом наружной фиксации. Данные КТ после наложения аппарата наружной фиксации использовали для создания 3D-модели, по которой определяли хирургический доступ по указанной методике. Погружной остеосинтез выполняли после спадания отека. Период между датами госпитализации и операции составил (8,2 ± 3,2) дня. Интраоперационно оценивали продолжительность вмешательства и объём кровопотери по гравиметрическому методу. Время операции составило (65,08 ± 7,03) минут, кровопотеря — (119,3 ± 18,51) мл.
Послеоперационные раны зажили в срок, гнойно-воспалительных осложнений не зарегистрировано. Эффективность репозиции оценивали по критериям Burwell – Charnley [7]: у восьми пациентов результат оценен как anatomical (анатомичный), у четырех — как fair (приемлемый). Неудовлетворительных результатов не выявлено.
Функциональные результаты оценивали через шесть месяцев после операции по шкале AOFAS AHS [8] и визуально-аналоговой шкале VAS FA [9]. Значения (78,67 ± 8,68) баллов по AOFAS и (41,08 ± 5,05) балл по VAS FA соответствуют хорошему функциональному восстановлению голеностопного сустава и высокой степени удовлетворённости пациентов. Показатель консолидации перелома по модифицированной шкале mRUST [10] (13,5 ± 1,43) указывает на завершённую консолидацию перелома.
Клинический пример
Пациент 52 лет поступил с диагнозом «закрытый многооскольчатый внутрисуставной перелом дистального метаэпифиза левой ББК со смещением отломков». Травма получена в результате падения с высоты четыре метра на прямые ноги. Через шесть часов после поступления в стационар осуществили фиксацию левой голени и стопы аппаратом наружной фиксации, после чего выполнили компьютерную томографию, на основании которой изготовили полноразмерный 3D-прототип (рис. 2). Произвели разметку суставной поверхности прототипа (рис. 3) и определили ключевые фрагменты, — задне-латеральный и передне-латеральный, точки выхода перелома — в передне-центральном и задне-медиальном квадратах.
На основании полученных данных выбрали хирургические доступы: заднемедиальный и передне-латеральный. Осуществлён остеосинтез из этих доступов с установкой передне-латеральной пластины и 1/3 трубчатой пластины сзади (рис. 4). Задне-медиальный доступ позволил полностью визуализировать перелом заднего края ББК, осуществить репозицию отломков ad occulus и уложить ранее пре-моделированную при помощи 3D-прототипа 1/3 трубчатую пластину. Далее пациента перевернули на спину, выполнили передне-латеральный доступ. Метадиафизарный компонент перелома фиксировали передне-латеральной премоделированной L-образной пластиной, передне-латеральный фрагмент (Chaput) — винтом. Применённый доступ позволил визуализировать передней край вырезки малоберцовой кости для прецизионной репозиции фрагмента Chaput.
Послеоперационный период протекал без осложнений, раны зажили первичным натяжением. Больной разрабатывал движения в оперированном голеностопном суставе в течение восьми недель. Через шесть месяцев после операции на контрольном осмотре результат лечения оценён как удовлетворительный.
По шкале AOFAS AHS сумма баллов составила 82 балла, по шкале VAS-FA — 41 балл, в обоих случаях сумма баллов соответствовала отличным результатам. При оценке рентгенограмм (рис. 5) по критериям mRUST получено 13 баллов, что соответствует перелому в стадии консолидации. Миграции фиксаторов, вторичного смещения не выявлено.
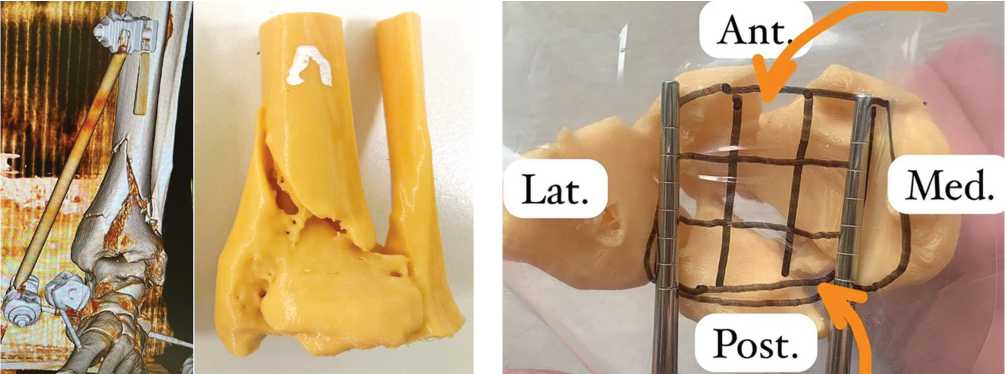
Рис. 2. 3D-реконструкция данных компьютерной томографии перелома и его 3D-прототип
Рис. 3. Разметка суставной поверхности 3D-прототипа с указанием точки выхода линий перелома на переднюю и заднюю поверхность ББК
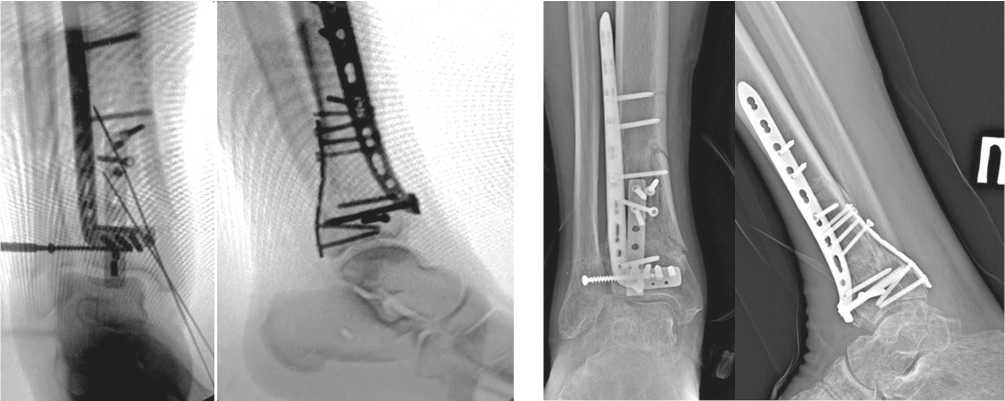
Рис. 4. Интраоперационные рентгенограммы пациента в прямой и боковой проекциях
Рис. 5. Рентгенограммы через шесть месяцев после операции
ОБСУЖДЕНИЕ
Знание точных морфологических характеристик перелома дистального метаэпифиза ББК является ключевым слагаемым успеха лечения. На сегодняшний день классические принципы лечения пациентов с переломами пилона и классические хирургические доступы, предложенные T. Ruedi и M. Allgower, по-прежнему широко применяют. Однако морфологические варианты этих переломов очень разнообразны, вследствие чего механическое копирование принципов и хирургических доступов может привести к неожиданным исходам и в некоторых тяжелых случаях даже к неудаче лечения.
M. Assal et al. при выборе хирургического доступа рекомендуют ориентироваться на биомеханику повреждения с целью установки опорной пластины на сторону компрессии [11]. Эксперты группы АО R. Buckley и A. Sands при выборе доступа предлагают учитывать размер передне-латерального фрагмента [12]. При больших размерах и близости плоскости перелома к медиальной лодыжке рекомендован передне-медиальный доступ, при меньших размерах передне-латерального фрагмента и более латеральном расположении плоскости перелома, переднелатеральный доступ. Недостатком этого способа является отсутствие определения передне-латерального фрагмента, четких критериев «большего» и «меньшего» его размера и «близости линии перелома к медиальной лодыжке».
-
J. Liu et al. в мета-анализе 19 статей (733 пациента) о хирургических доступах и исходах лечения при открытой репозиции и внутренней фиксации переломов пилона отметили, что 30 % операций были выполнены из передне-латерального доступа. Средняя частота осложнений составила 16 %, наименьшую частоту наблюдали при медиальном (11,7 %) и переднем (11,8 %) хирургических доступах, наибольшую — при заднебоковом (23 %) и переднемедиальном (22,8 %) доступах. Максимально тяжелые осложнения зарегистрированы при переднелатеральном доступе (12 случаев). Наиболее распространенными осложнениями были несостоятельность раны (21 %), замедленное сращение или несращение (19 %), инфекция мягких тканей (17 %). Различие в частоте осложнений могло быть связано не только с самим доступом, но и с типом перелома или другими факторами (например, техникой хирургического вмешательства, временем операции, использованием антибиотиков). Однако в исследовании отсутствовало непосредственное сравнение разных хирургических доступов [13].
В.Г. Бабовников с соавт. при фрагментации заднего и внутреннего отделов метаэпифиза ББК выбирали дугообразный задне-внутренний доступ с продолжением разреза на переднюю поверхность в случае необходимости [14]. Этот доступ, по мнению авторов, обеспечивает хороший визуальный контроль всей суставной поверхности. При разрушении переднего и центрального отделов суставной площадки метаэпифиза применяли передний доступ по внутреннему краю сухожилия передней большеберцовой мышцы с дугообразным продолжением по передней суставной поверхности кнаружи. Данное исследование, систематизирующее большой клинический опыт в лечении пациентов с внутрисуставными переломами дистального метаэпифиза ББК имело ограничения. Выбор только между двумя доступами снижает возможности визуализации и фиксации всех фрагментов, ни один подход не обеспечивает полноценного обзора передне-латеральных фрагментов (Chaput), что может ухудшить точность репозиции и отдалённые результаты. Кроме того, задне-внутренний доступ требует работы вблизи сосудисто-нервного пучка, создавая риск его повреждения.
T. Urrutia et al. при сравнении классических хирургических доступов к пилону ББК на кадаверном материале выявили, что антеромедиальный доступ обеспечивает наибольшую площадь экспозиции (18,36 см²), а антеролатеральный — наибольший сегмент по окружности (72°). Авторы подчеркивают, что при выборе доступа должна быть учтена стратегия репозиции, например, постеромедиальный доступ оптимален для заднего фрагмента Фолькмана, а передне-латеральный — для передне-латерального фрагмента Tillaux – Chaput [15].
-
B. Puha et al. предлагают оценивать суставную поверхность ББК по данным КТ, выполненной после установки аппарата наружной фиксации. Авторы выделяют медиальный, центральный, передний и латеральный фрагменты, для фиксации медиальных и центральных фрагментов выбирают медиальный доступ, для переломов с преимущественно передними фрагментами — передний доступ, а для переломов с большим латеральным компонентом или для одновременной фиксации малоберцовой кости — антеролатеральный доступ [16].
А.В. Миронов с соавт. при выборе хирургического доступа предлагают ориентироваться на четырехколонную классификацию Tang: при наибольшем повреждении медиальной колонны использовать передний медиальный доступ, при повреждении латеральной колонны — передне-латеральный, при повреждении задней колонны — задний [17]. Но данный метод не учитывает возможность одновременного повреждения нескольких колонн, а в случае повреждения задней колонны не конкретизирует доступ.
P.A. Cole et al. при изучении на КТ распределения линий переломов и положения основных фрагментов у 38 пациентов с оскольчатыми внутрисуставными переломами дистального метаэпифиза ББК отмечают три основных фрагмента в переднелатеральной, медиальной и заднелатеральной зонах. Авторы подчеркивают, что рациональный выбор хирургического доступа может быть основан на понимании морфологии перелома [4]. При этом конкретного алгоритма выбора доступа авторы не предлагают. Многие авторы исследований, посвященных стратегии лечения этих переломов, также рекомендуют учитывать данные КТ при выборе доступа [18–20].
-
Y. Zhao et al. утверждают, что выбор хирургического доступа, основанный на анализе КТ перелома, позволяет точно восстановить суставную поверхность и достичь стабильной фиксации, что в свою очередь обеспечивает хорошие функциональные результаты и снижает количество осложнений. Так, при наличии крупных задних фрагментов с распространением на тарзальный канал или медиальную лодыжку используют заднемедиальный доступ, а переднюю часть ББК и переломы малоберцовой кости визуализируют через переднелатеральный доступ. При небольших задних маллеолярных фрагментах без распространения на тарзальный канал для репозиции заднего фрагмента ББК и латеральной лодыжки применяют заднелатеральный доступ, а передние фрагменты визуализируют через переднемедиальный доступ с коррекцией положения разреза в зависимости от локализации центрального импрессионного фрагмента [21]. Преимуществом данного метода можно считать то, что он базируется
на данных КТ. Однако фокус внимания авторов этой публикации сосредоточен на задних отделах голеностопного сустава, что не позволяет считать выбор доступа универсальным для всего множества морфологических вариантов переломов пилона.
В отличие от предыдущих исследований разработанный метод предлагает объективную количественную оценку локализации ключевых фрагментов с помощью стандартизированной разметки суставной поверхности. Это исключает субъективность в выборе доступа и позволяет точно определить, какой фрагмент требует первичной репозиции.
Метод позволяет комбинировать классические доступы в зависимости от конкретной морфологии перелома, что обеспечивает лучшую визуализацию всех фрагментов, включая переднелатеральные (Chaput), и снижает риск некорректной репозиции. Кроме того, он учитывает одновременное повреждение нескольких колонн и предлагает конкретные доступы для каждого случая, включая задние фрагменты (например, заднелатеральный или заднемедиальный доступы).
Основа метода — 3D-прототипирование, позволяющее точно смоделировать перелом и заранее определить оптимальные доступы, снизить риск некроза мягких тканей, оптимизировать визуализацию фрагментов, уменьшить частоту инфекционных осложнений и расхождения ран.
ЗАКЛЮЧЕНИЕ
Разработанный метод представляет собой синтез современных технологий 3D-планирования, стандартизированного топографического анализа и персонализированного подхода. Его внедрение в клиническую практику позволит не только оптимизировать выбор хирургического доступа при остеосинтезе переломов пилона, но и существенно повысить точность репозиции, стабильность фиксации и безопасность вмешательства в целом. Применение данного подхода открывает новые возможности для совершенствования хирургического лечения пациентов со сложными внутрисуставными переломами дистального метаэпифиза большеберцовой кости.


