Выбор источника фукоидана и оптимизация его ферментативного гидролиза
Автор: Новикова Ю.С., Анохина Е.П., Корнеева О.С.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Биотехнология, бионанотехнология и технология сахаристых продуктов
Статья в выпуске: 2 (64), 2015 года.
Бесплатный доступ
Разработка биотехнологии фукозы и фукоолигосахаридов из растительного сырья вызывает особый интерес, что обусловлено широким спектром биологических активностей фукозы. Фукоза является незаменимым углеводным компонентом иммуноглобулинов и выполняет важные биологические функции в процессах онтогенеза, клеточной дифференциации и формирования иммунитета, а также в репродуктивных процессах позвоночных. Фукоза и ее полимеры обладают пребиотическим действием, а фукоолигосахариды проявляют также антиоксидантную активность. Одним из перспективных способов получения фукозы и фукоолигосахаридов является ферментативный гидролиз фукоиданов растительного сырья. Наиболее доступным и недорогим растительным сырьем для выделения фукоидана являются бурые водоросли. Литературный анализ показал, что водоросли Fucus vesiculosis характеризуются наибольшим содержанием фукоидана, который по химической структуре является гомополимером фукозы с преобладанием 1,3 - гликозидных связей. Был исследован гидролиз фукоидана водорослей Fucus vesiculosis иммобилизованным ферментным препаратом α-L-фукозидазы для определения оптимальных условий проведения ферментативного процесса. Эффективность ферментативной деструкции фукоидана зависит от ряда факторов, важными из которых являются дозировка ферментного препарата, рН реакционной среды и температура, при которых протекает процесс гидролиза, а также его продолжительность. В результате проведенных исследований установлены оптимальные параметры процесса ферментативного гидролиза фукоидана водорослей Fucus vesiculosis : дозировка ферментного препарата 6 ед/г, температура 50 ºС, рН 7,0, продолжительность процесса 5 ч. При таких условиях степень гидролиза фукоидана составляла 83-85%, что показывает перспективность ферментативного гидролиза для получения фукозы из растительного сырья.
Фукоидан, бурые водоросли, α-l-фукозидаза, фукоза, фукоолигосахариды, гидролиз, субстрат
Короткий адрес: https://sciup.org/14040421
IDR: 14040421 | УДК: 577.15
Selection the source of fucoidan and optimization of its enzymatic hydrolysis
The development of biotechnology fucose and fucooligosaccharides from vegetable raw materials is of particular interest, due to the wide range of biological activity fucose. The fucose is an important carbohydrate component of immunoglobulins and performs important functions in the biological processes of ontogenesis, cell differentiation as well as in the reproductive processes in vertebrates and in the formation of immunity. The fucose and its polymers have prebiotic effects, fucooligosaccharides have also exhibit antioxidant activity. One of the promising methods of obtaining fucose and fucooligosaccharides is an enzymatic hydrolysis of fucoidan vegetable raw materials. The most accessible and inexpensive plant raw materials to extract fucoidan are the brown algae. Literary analysis showed that the algae Fucus vesiculosis are characterized by the highest content of fucoidan, the chemical structure of which is a homopolymer of fucose with a predominance of 1,3 - glycoside bonds. It was investigated the hydrolysis of fucoidan algae Fucus vesiculosis by immobilized enzyme preparation α-L-fucosidase for determine the optimal conditions of the enzymatic process. The efficiency of enzymatic degradation of fucoidan depends on several factors, the most important of which are the amount of the enzyme preparation, the pH of the reaction medium and the temperature at which the hydrolysis takes place, as well as its duration. Were determined the optimal process parameters of the enzymatic hydrolysis of fucoidan algal Fucus vesiculosis: the amount of the enzyme preparation of 6 U / g, the temperature 50 ° C, pH 7.0, the hydrolysis time 5 hours. Under these conditions, the degree of hydrolysis of fucoidan was 83-85%, which shows prospects of the enzymatic hydrolysis for obtaining of fucose from vegetable raw materials.
Текст научной статьи Выбор источника фукоидана и оптимизация его ферментативного гидролиза
Актуальной в настоящее время является разработка биотехнологий продуктов функционального назначения. Особый интерес привлекает «минорный» сахар – фукоза, который является незаменимым углеводным компонен- том иммуноглобулинов и других биологически активных веществ [1].
Фукоза выполняет важные биологические функции в процессах онтогенеза, клеточной дифференциации, а также установлена важная роль
фукозы в формировании иммунитета [2, 3] и в репродуктивных процессах позвоночных [4]. Фукоза и ее полимеры обладают пребиотическим действием [5], а фукоолигосахариды проявляют также антиоксидантную активность [6].
В чистом виде фукоза практически не встречается в природе, а входит в состав фукоиданов - полисахаридов бурых водорослей, некоторых морских беспозвоночных и бактерий.
Одним из перспективных способов получения фукозы и фукоолигосахаридов является биодеструкция фукоиданов бурых водорослей.
Ранее получен иммобилизованный ферментный препарат α-L-фукозидазы [7], способный расщеплять гликозидные связи в фукоиданах, использование которого позволит повысить рентабельность получения фукозы и фукоолигосахаридов из растительного сырья.
Цель данного исследования состояла в подборе перспективного источника фукоидана среди бурых водорослей и определении оптимальных условий ферментативного гидролиза фукоидана.
Объектами исследования служили иммобилизованная α-L-фукозидаза с каталитической активностью 2310 ед./г и фукоидан бурых водорослей.
Выделение фукоидана из бурых водорослей проводили по методу, позволяющему разделять водорастворимые полисахариды водорослей [8].
Определение оптимальных условий ферментативного гидролиза субстрата проводили в интервале рН 6,0–8,0, температур 30–70 °С и при разной дозировке ферментного препарата.
Для определения степени гидролиза фукоидана 1 мл 10 % водного раствора фукоидана, 1 мл 0,1 М фосфатного буфера и 100 мкл раствора фермента выдерживали при заданной температуре в течение 6 часов. Затем определяли количество фукозы по методу Дише [9]. По количеству образовавшейся фукозы в результате гидролиза рассчитывали степень гидролиза фукоидана.
Наиболее доступным и недорогим растительным сырьем для выделения фукоидана являются бурые водоросли.
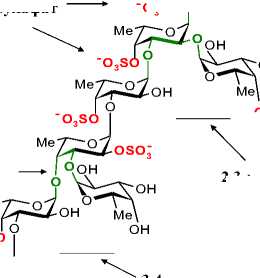
Фукоидан бурых водорослей представляет собой сложный сульфатированный полисахарид, основным звеном которого является L-фукоза [10]. Химическая структура фукоидана бурых водорослей представлена на рисунке 1.
Фукоиданы разных видов водорослей различаются по молекулярной массе (от 10 до
1000 кДа), моносахаридному составу (помимо фукозы в состав могут входить галактоза, манноза, ксилоза, арабиноза, рамноза, рибоза), степени сульфатирования молекул фукозы и типу связи между ними [11].
Me
4-сульфат
O SO
OSO -
(1 ^ 4)-связь
Me
- O SO
(1 ^ 3)-связь
OSO -
O
2-сульфат
2,3-разветвление
з,4-разветвление
Рисунок 1. Химическое строение фукоидана бурых водорослей
Содержание фукоидана в бурых водорослях варьирует от 0,6 до 7,9 % на сухое вещество. Наибольшее количество фукоидана содержат водоросли порядков Laminariales и Fucales , сравнительный химический состав которых представлен в таблице 1. Как видно из таблицы, наибольшее содержание фукоидана отмечено в водорослях Fucus vesiculosis .
Фукоидан водоросли Fucus vesiculosis является частично сульфатированным гомополимером фукозы с преобладанием 1,3 – гликозидных связей, что облегчает очистку фукозосодержащих гидролизатов из-за отсутствия в продуктах гидролиза других сахаров [10].
Проведенный анализ содержания фукоиданов в бурых водорослях и их структуры показал, что наилучшим источником фукоидана являются водоросли Fucus vesiculosis . Кроме того эти водоросли являются дешевым и доступным сырьем в Северном и Дальневосточном регионах России.
На фукоидане, выделенном из водорослей Fucus vesiculosis, исследовали действие иммобилизованной α-L-фукозидазы в процессе гидролиза.
Эффективность ферментативного гидролиза зависит от ряда факторов, важными из которых являются дозировка ферментного препарата, температура и рН реакционной среды, при которых протекает гидролиз, а также время гидролиза.
Т а б л и ц а 1
Химический состав бурых водорослей порядков Laminariales и Fucales , % на сухую массу [12]
|
Водоросли |
Минеральные вещества |
Белок |
Йод |
Маннит |
Альгиновая кислота |
Фукоидан |
Липиды |
|
Порядок Laminariales - ламинариевые |
|||||||
|
Laminaria japonica |
20,7 |
9,7 |
0,22 |
12,8 |
26,3 |
2,54 |
2,10 |
|
L. bongardiana |
10,5 |
8,3 |
0,12 |
15,3 |
34,1 |
3,6 |
0,88 |
|
L. cichorioides |
19,4 |
3,6 |
0,21 |
9,4 |
15,7 |
2,88 |
0,64 |
|
L. gurjanovae |
14,4 |
2,9 |
0,25 |
9,7 |
21,3 |
3,8 |
1,29 |
|
Kjellmanella crassifolia |
26,6 |
10,4 |
0,11 |
12,3 |
27,7 |
3,32 |
0,98 |
|
Agarum cribrosum |
23,1 |
16,8 |
0,04 |
4,3 |
23,5 |
2,1 |
0,56 |
|
Alaria fistulosa |
24,9 |
10,4 |
0,07 |
8,5 |
24,4 |
0,70 |
1,40 |
|
A. angustata |
25,4 |
11,7 |
0,14 |
6,4 |
30,5 |
2,10 |
1,40 |
|
Порядок Fucales - фукусовые |
|||||||
|
Fucus evanescens |
18,6 |
10,0 |
0,007 |
5,5 |
36,4 |
6,04 |
1,12 |
|
Cystoseira crassipes |
12,9 |
10,9 |
0,002 |
5,6 |
34,6 |
5,4 |
0,6 |
|
Fucus vesiculosis |
17,9 |
9,4 |
0,006 |
5,4 |
34,9 |
7,2 |
1,15 |
|
Sargassum pallidum |
10,7 |
5,6 |
0,011 |
10,3 |
26,7 |
4,0 |
0,82 |
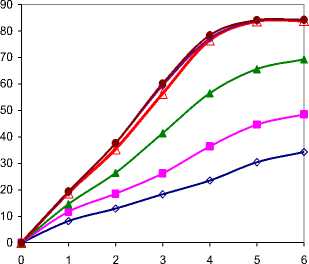
На рисунке 2 представлена зависимость степени гидролиза фукоидана от дозировки ферментного препарата. Фермент вносили в количестве 1-10 ед./г фукоидана. Внесение фермента в количестве 1 ед./г обеспечивало степень гидролиза менее чем на 30 % за 5 ч. При увеличении концентрации ферментного препарата до 4 ед./г степень гидролиза за то же время составила около 60 %. Максимальный выход фукозы 85 % обеспечивало внесение фермента в количестве 6 ед./г фукоидана. Повышение концентрации фермента до 10 ед./г не способствовало значительному увеличению степени гидролиза. Следовательно, оптимальной дозировкой фермента следует считать дозировку 6 ед./г фукоидана.
-■- 2 ед/г
-*- 4 ед/г
6 ед/г
-♦- 8 ед/г
-•- 10 ед/г
Продолжительность гидролиза, ч
Рисунок 2. Влияние дозировки ферментного препарата на степень гидролиза фукоидана
1 ед/г
Далее исследовали влияние температуры на степень гидролиза фукоидана в интервале 30-70 °С при дозировке 6 ед./г и рН 7,0. Данные таблицы 2 показывают, что максимальная степень гидролиза 84 % наблюдалась при температуре 50 оС. Дальнейшее увеличение температуры приводило к снижению степени гидролиза, что обусловлено термической инактивацией фермента.
Т а б л и ц а 2
Степень гидролиза фукоидана при разных температурах (СГ, %)
|
Температура ºС |
Степень гидролиза (СГ), % при продолжительности гидролиза, ч |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
30 |
16 |
29 |
42 |
55 |
60 |
61 |
|
40 |
14 |
34 |
47 |
62 |
77 |
78 |
|
50 |
18 |
36 |
58 |
66 |
84 |
86 |
|
60 |
13 |
29 |
48 |
55 |
60 |
64 |
|
70 |
9 |
22 |
27 |
34 |
48 |
51 |
Влияние рН реакционной среды на эффективность гидролиза фукоидана изучали при дозировке фермента 6 ед/г и температуре 50 оС. Из таблицы 3 видно, что рН среды оказывает сильное влияние на действие фермента. Максимальная степень гидролиза фукоидана наблюдалась при рН 7,0. Смещение рН среды в кислую или щелочную область приводило к значительному снижению выхода фукозы. В щелочной среде, например, при рН 8,0 за 5 часов гидролиза выход фукозы составил около 30 %, а при рН 7,0 за то же время - 84%.
Рациональным временем гидролиза следует считать 5 часов, при которых степень гидролиза достигает 84 %, Дальнейшее увеличение продолжительности гидролиза не приводит к значительному увеличению выхода фукозы.
Т а б л и ц а 3
Степень гидролиза фукоидана в зависимости от рН среды (СГ, %)
|
рН |
Степень гидролиза (СГ), % при продолжительности гидролиза, ч |
|||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
6,0 |
13 |
25 |
40 |
44 |
48 |
50 |
|
6,5 |
17 |
34 |
58 |
62 |
79 |
79 |
|
7,0 |
18 |
35 |
59 |
66 |
84 |
85 |
|
7,5 |
11 |
16 |
26 |
39 |
52 |
53 |
|
8,0 |
7 |
13 |
19 |
24 |
30 |
31 |
Список литературы Выбор источника фукоидана и оптимизация его ферментативного гидролиза
- Ройт, А., Бростофф Дж., Мейл Д. Иммунология. М.: Мир, 2000. 592 с.
- Luther K.B., Haltiwanger R.S. Role of unusual O-glycans in intercellular signaling//The International Journal of Biochemistry & Cell Biology. 2009. V. 41. P. 1011-1024.
- Becker D. J., Lowe J. B. Fucose: biosynthesis and biological function in mammals//Glycobiology. 2003. V. 13. P. 41-53.
- Intra J., Cenni F., Perotti M.-E. An α-L-fucosidase potentially involved in fertilization is present on drosophila spermatozoa surface//Molecular reproduction and development. 2006. V. 73. P. 1149-1158.
- Санина Т.В. и др. Исследование бифидогенной активности фукозы и ее полимеров//Вестник Воронежского государственного университета. Серия: Химия. Биология. Фармация. 2011. № 1. С. 141-143.
- Черенков Д.А., Анохина Е.П., Кирьянова С.В., Корнеева О.С. Антиоксидантная активность продуктов гидролиза природных полимеров (маннана и фукоидана)//Вестник Воронежского государственного университета инженерных технологий. 2012. №1. С. 151-153.
- Мещерякова О.Л., Новикова Ю.С., Анохина Е.П., Корнеева О.С. Получение и характеристика биокатализаторов на основе иммобилизованных гликозидаз//Вестник Воронежского государственного университета инженерных технологий. 2014. №4. С. 206-212.
- Пат. № 2003123744, RU МПК A61K35/80, A61K31/715. Способ комплексной переработки бурых водорослей с получением препаратов для медицины и косметологии/Шевченко Н.М., Имбс Т.И., Урванцева А.М., Кусайкин М.И., Корниенко В.Г., Звягинцева Т.Н., Елякова Л.А. № 2003123744/15; Заявл. 28.07.2003; Опубл. 27.01.2005, Бюлл. № 3.
- Dische Z., Shettles L. B. A specific color reaction of methylpentoses and a spectrophotometric micromethod for their determination//J. Biol. Chem. 1948. V. 175. № 2. P. 595-603.
- Усов А.И., Кирьянов А.В. Полисахариды водорослей. Выделение фракций фукоидана из бурых водорослей//Биоорганическая химия. 1998. № 24. С. 437-445.
- Кузнецова Т. В. и др. Сравнительное исследование биологической активности фукоиданов из бурых водорослей//Вестник Дальневосточного отделения Российской академии наук. 2006. № 6. С. 105-110.
- Аминина Н. М. и др. Состав и возможности использования бурых водорослей дальневосточных морей//Вестник Дальневосточного отделения Российской академии наук. 2007. № 7. С. 123-130.


