Выделение и идентификация вируса эпизоотической диареи свиней при вспышке в крупном свиноводческом хозяйстве
Автор: Стрижакова О.М.
Журнал: Сельскохозяйственная биология @agrobiology
Статья в выпуске: 4 т.48, 2013 года.
Бесплатный доступ
Эпизоотическая диарея свиней (ЭДС) характеризуется острым энтеритом и сильным поносом. Ее возбудитель относится к той же группе рода Сoronavirus семейства Сoronaviridae, что и вирусы трансмиссивного гастроэнтерита свиней (ТГС), коронавирус кошек, собак и человека 229Е. Начиная с 2005 года, на территории Российской Федерации регистрировали вспышки болезни, клинически схожей с трансмиссивным гастроэнтеритом свиней (ТГС) и вызывающей массовый падеж подсосных поросят (в некоторых случаях до 80 %). При этом свиноматки в неблагополучных хозяйствах были привиты против ТГС. Целью нашей работы было выделение в культуре клеток и идентификация инфекционного агента, ставшего причиной вспышек болезни с диарейным синдромом у свиней. Из патологического материала от больных поросят 3-5-суточного возраста выделен РНК-содержащий вирус, идентифицированный как вирус эпизоотической болезни свиней. Титр инфекционности вируса 5-го пассажа в культуре клеток Vero составлял 10 3,50 ТЦД 50/см 3. Выделенный вирус обозначили как изолят БС-08. К настоящему времени проведено 25 последовательных пассажей вируса в культуре клеток; срок проявления цитопатического действия составляет 24-48 ч, инфекционный титр — 10 4,75-10 5,50 ТЦД 50/см 3.
Эпизоотическая диарея свиней (эдс), патологический материал, выделение вируса, культуры клеток, цитопатический эффект
Короткий адрес: https://sciup.org/142133429
IDR: 142133429 | УДК: 636.4:619:616.98:578:57.083
Isolation and identification of epizootic diarrhea virus in pigs under outbreak at a large farm
Epizootic diarrhea fever (EDF), characterized by acute enteritis and hard intestinal disorders, is caused by the virus of the same group of С oronavirus ( Coronaviridae ) as the virus of transmissible gastroenteritis of pigs, coronavirus of cats and dogs, and human 229E strain. From 2005, at the territory of the Russian Federation the outbreaks of the disease were recorded, clinically similar to pig transmissible gastroenteritis. The infections caused a loss of piglets, in some cases up to 80 %. However, the sows in such farms have been vaccinated against the transmissible gastroenteritis of pigs. The aim of our study was to isolate in cell culture and identify an infectious agent that causes the outbreaks with diarrheal syndrome in pigs. From the pathological material of 3-5-day-old piglets with the pathology a RNA virus was isolated and identified as the virus of epizootic diseases of pigs. Virus infectivity in the fifth passage in Vero cell culture was 10 3,50 ТCID 50/sm 3. The isolate was named as BS-08. To date, there are 25 successive passages of the virus in cell culture. A citopatic effect is registered in 24-48 hours, and the infectious titer (titer of citopatic effect — TCE) makes 10 4,75-10 5,50 TCID 50/sm 3.
Текст научной статьи Выделение и идентификация вируса эпизоотической диареи свиней при вспышке в крупном свиноводческом хозяйстве
Целью нашей работы было выделение в культуре клеток и идентификация инфекционного агента, ставшего причиной вспышек болезни с диарейным синдромом у свиней.
Методика. Материалом для исследования служили пробы патологического материала (кишечник, желудок, печень, почки, головной мозг) от вынужденно убитых и павших поросят 3-5-суточного возраста, полученные с сентября по декабрь 2008 года из свиноводческих хозяйств закрытого типа в западном регионе России. Для выделения возбудителя использовали перевиваемые линии культур клеток РК-15, CV-1, MA104 и Vero (предоставлены лабораторией культур клеток Всероссийского НИИ ветеринарной вирусологии и микробиологии — ВНИИВВиМ). В качестве ростовой применяли среду Игла с добавлением 10 % фетальной сы- воротки телят (ФСТ), пенициллина (100 ед/мл), стрептомицина (100 мкг/мл), амфотерицина В (2,5 ед/мл). Поддерживающей служила среда Игла без ФСТ с указанными антибиотиками и трипсином (5 мкг/см3). Для предварительной обработки гомогенатов патологического материала и культуральных материалов, полученных при пассировании, использовали среду Игла с антибиотиками и трипсином в концентрации 5, 10 и 20 и 40 мкг/см3.
Культуры клеток инкубировали при 37 ° С, после формирования монослоя (через 1-2 сут) ростовую среду удаляли, монослой 3-кратно промывали бессывороточной средой Игла и инокулировали суспензиями патологического материала или культуральным материалом, полученным при проведении пассажей. В культуру клеток вносили 5 см3 материала и инкубировали 60 мин при 37 ° С. Затем инокулят удаляли и во флаконы помещали поддерживающую среду Игла с трипсином (в концентрации 5 мкг/см3) или без трипсина. Инокулированные культуры инкубировали при 37 ° С в течение 5-6 сут (при слепых пассажах) либо до проявления цитопатического действия (ЦПД). После этого культуру замораживали, оттаивали, стерильно сливали во флаконы и хранили при - 70 ° С.
Тип нуклеиновой кислоты определяли по методу Майра с соавт. (1974). Чувствительность к воздействию хлороформа анализировали в соответствии с описанием Майра и Бегеля (1961).
Полимеразную цепную реакцию проводили с использованием коммерческой тест-системы «ЭДС» для выявления эпидемической диареи свиней методом ПЦР, кат. № VET-58-FRT-S(RG,iQ) серия 18.08.12 (производитель — ФБУН ЦНИИ эпидемиологии Роспотребнадзора, г. Москва) в соответствии с прилагаемыми рекомендациями.
Реакцию нейтрализации (РН) выполняли в микроварианте с применением 96-луночных культуральных планшетов («Corning», США). В лунки помещали по 100 мкл 2-кратных разведений (с 1:2 до 1:4096) нормальной, специфической и исследуемых сывороток в среде Игла с добавлением пенициллина (100 ед/мл), стрептомицина (100 мкг/мл) и амфотерицина В (2,5 ед/мл), затем по 100 мкл ростовой среды Игла, содержащей вирус в расчетной дозе 100 ЕД. Планшеты выдерживали в течение 1 ч при 37 ° С, после чего переносили образцы (смесь сыворотки с вирусом) в лунки планшетов с монослоем культуры клеток и инкубировали в течение 4-5 сут в атмосфере 5 % СО 2 при 37 ° С. В РН использовали референтные сыворотки к вирусу ТГС, полученные из музея штаммов ВНИИВВиМ.
Статистическую обработку данных выполняли с помощью программы Statistica v. 17.
Результаты. Наблюдавшаяся клиническая картина при развитии патологии была следующей: у поросят с 2-4-суточного возраста проявлялась диарея с выделением серо-зеленых каловых масс, обезвоживание, жажда, анемичность видимых слизистых оболочек, температура тела повышалась или находилась в пределах физиологической нормы (39,4 °C), у некоторых животных отмечали мышечную дрожь. Гибель наступала через 2-5 сут после начала диареи. Клинических и патологоанатомических признаков заболевания органов дыхания выявлено не было. Свиноматок в хозяйствах вакцинировали против ТГС, ротавируса свиней, колибактериоза, анаэробной энтеротоксемии, рожи, классической чумы свиней.
Ветеринарно-санитарное состояние ферм в большинстве случаев соответствовало принятым требованиям. Территория огорожена сплошным забором по периметру, корпуса нового и старого типа. Дезбарьеры и дезковрики имелись в ветсанпропускниках и на местах выезда транспортных средств. Содержание безвыгульное, поголовье — около 2000 свиноматок. Заболеваемость поросят за период регистрируемой вспышки (около 3 мес) составила приблизительно 90 %, летальность — примерно 85 %.
При постановке диагноза были исключены бактериальные инфекции (колибактериоз, анаэробная энтеротоксемия), а также вирусные инфекции — африканская чума свиней (АЧС), репродуктивно-респираторный синдром (РРСС), трансмиссивный гастроэнтерит (ТГС), классическая чума свиней (КЧС), болезнь Ауески, ротавирусная инфекция свиней.
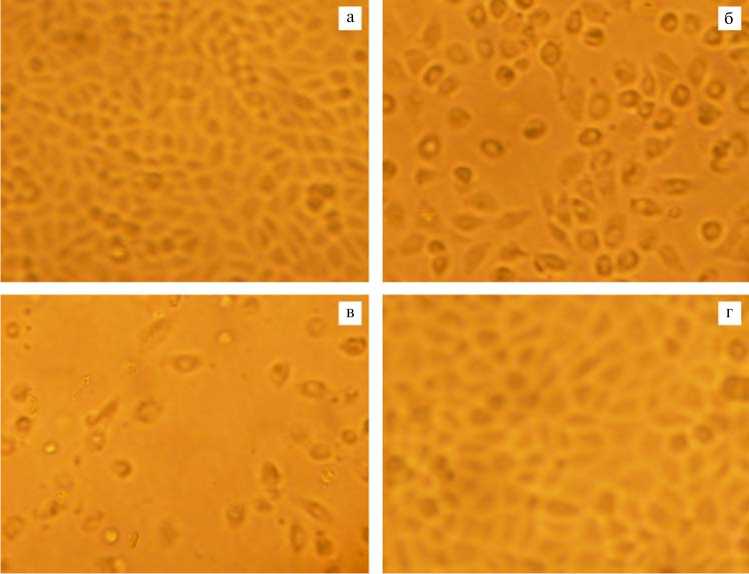
Рис. 1. Цитопатический эффект в культуре клеток Vero, индуцированный полученным изолятом вируса эпизоотической диареи свиней: а, б, в — соответственно 24, 48, 72 ч после заражения; г — незараженная культура (множественность заражения 0,1 ед. на клетку).
При последовательных слепых пассажах проб патологического материала в культурах клеток РК-15, CV-1, MA104 и Vero с использованием двух модификаций метода (с применением трипсина и без его добавления) цитопатогенный вирус был выделен из ткани тонкого отдела кишечника на 5-м пассаже в клетках Vero (рис. 1) в случае, когда инокулят предварительно обрабатывали ферментом. Титр инфекционности при этом составлял 103 , 50 ТЦД50/см3.
Накопление вируса эпизоотической диареи свиней при пассировании в культуре клеток Vero в зависимости от предварительной обработки вируссодержащего материала трипсином ( n = 4)
|
Концентрация трипсина |
Пассаж |
||||
|
1-й |
2-й |
3-й |
4-й |
5-й |
|
|
ТЦД 50 /см3 |
ТЦД 50 /см3 |
ТЦД 50 /см3 |
ТЦД 50 /см3 |
ТЦД 50 /см3 |
|
|
Без обработки (0 мкг/см3) |
3,50 (3,1-3,8) |
3,50 (3,1-3,8) |
3,75 (3,4-4,0) |
3,75 (3,4-4,0) |
3,75 (3,4-4,0) |
|
5 мкг/см3 |
3,50 (3,1-3,8) |
3,75 (3,4-4,0) |
3,75 (3,4-4,0) |
4,00 (3,5-4,5) |
4,00 (3,5-4,5) |
|
10 мкг/см3 |
3,50 (3,1-3,8) |
4,00 (3,5-4,5) |
4,25 (3,7-4,7) |
4,50 (3,9-5,0) |
4,50 (3,9-5,0) |
|
20 мкг/см3 |
3,75 (3,4-4,0) |
4,50 (3,9-5,0) |
5,25 (4,9-5,5) |
5,50 (5,1-5,8) |
5,50 (5,1-5,8) |
|
40 мкг/см3 |
3,75 (3,4-4,0) |
4,50 (3,9-5,0) |
5,25 (4,9-5,5) |
5,50 (5,1-5,8) |
5,50 (5,1-5,8) |
Примечание. Доверительный интервал 95 %.
При определении влияния различных концентраций трипсина на репродукцию вируса в культуре клеток Vero (в качестве контроля культуру клеток инокулировали необработанным вируссодержащим материалом) провели 5 последовательных пассажей (табл.). Как свидетельствуют представленные данные, при обработке трипсином в концентрации 5 мкг/см3 титр вируса возрастал до 4-го пассажа на 0,5 lg. Максимальное увеличение инфекционного титра было установлено после предварительной обработки вируссодержащего материала трипсином в конечной концентрации 20 мкг/см3. В этих условиях титр вируса повышался до 4-го пассажа, составил 5,50 ТЦД 5о /см3, и его величина сохранялась до 25-го пассажа.
Дальнейшее увеличение концентрации трипсина в вируссодержа-щем материале не приводило к повышению инфекционного титра вируса при пассировании на восприимчивой культуре клеток.

I 2 3 4 5 6 7 8 9 10 11 12
Рис. 2. Электрофорез в агаровом геле продуктов ПЦР РНК вируса эпизоотической диареи свиней: 1, 2 — экспертизные тканевые суспензии; 3-8 — пассажи вируса в культуре клеток (соответственно 1, 5, 10, 15, 20 и 25 пассажей); 9, 10 — концентрированный вирус; 11 — положительный контроль; 12 — отрицательный контроль.
При определении типа нуклеиновой кислоты посредством обработки зараженной культуры клеток 5 -йод-2'-дезоксиуридином не отмечалось затруднения репликации, что позволило нам отнести выделенный вирус к РНК-содержащим. При обработке хлороформом вирус потерял инфекционную активность, что указывает на наличие у него липидной оболочки.
Следует отметить, что ин-фекционность вируса не снижалась после обработки ультразву ком и при многократном замораживании/оттаивании. В РН с сыворотками против ВТГС было установлено, что они не нейтрализуют изолят.
При изучении с помощью ПЦР суспензии патологического материала, а также каждого 5-го пассажа выделенного вируса в культуре кле ток мы подтвердили наличие вируса ЭДС как в исходном патологическом материале, так и в последующих 25 пассажах (рис. 2).
Выделенный вирус обозначили как изолят БС-08. К настоящему времени было проведено 25 последовательных пассажей вируса в культуре клеток; срок появления цитопатического действия составлял при этом 2448 ч, инфекционный титр — 104 ’ 75-105 ’ 50 ТЦД50/см3
Итак, из патологического материала от больных 3-5-суточных по- росят, отобранного при вспышке болезни с диарейным синдромом и доставленного с сентября по декабрь 2008 года из западного региона РФ, выделен РНК-содержащий вирус, чувствительный к растворителям липидов. По результатам ПЦР возбудитель идентифицирован как вирус эпизоотической диареи свиней (ЭДС). В настоящее время с использованием этого изолята проводится работа по совершенствованию диагностики ЭДС, созданию средств для специфической иммунопрофилактики болезни и определения напряженности поствакцинального иммунитета.
Автор выражает благодарность И.Ю. Егоровой (Всероссийский НИИ ветеринарной вирусологии и микробиологии) за помощь при выполнении ПЦР.


