Выявление ОМИК-маркеров для прогнозирования риска развития негативных эффектов у детей с повышенным содержанием меди и никеля в крови
Автор: Зайцева Н.В., Землянова М.А., Кольдибекова Ю.В., Булатова Н.И.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Оценка риска в гигиене
Статья в выпуске: 1 (33), 2021 года.
Бесплатный доступ
Технология протеомного профилирования является перспективным направлением для исследования и обоснования молекулярных механизмов возникновения и развития ответных реакций организма на негативные воздействия на самых ранних стадиях их формирования, до возникновения симптомов клеточного и органного поражения. Особую актуальность приобретают исследования, направленные на повышение эффективности прогнозирования развития негативных эффектов для задач раннего выявления и профилактики последствий, ассоциированных с воздействием химических факторов среды обитания, в первую очередь с атмосферным воздухом. Выявлены омик-маркеры для прогнозирования риска развития негативных эффектов у детей с повышенным содержанием меди и никеля в крови. Выполнено протеомное исследование плазмы крови у детей, моделирование причинно-следственных связей. У детей с повышенным (до 3,5 раза) содержанием в крови меди и никеля выявлено порядка двадцати белковых пятен, достоверно отличающихся от соответствующих данных детей группы контроля. Установлены зависимости увеличения относительного объема трех белковых пятен, включающих аполипопротеин A-I, якорный белок А-киназы 9, витронектин, и уменьшения относительного объема одного белкового пятна, включающего транстиретин, от повышенного содержания в крови меди и никеля (R2 = 0,30-0,44; р = 0,0001-0,008). Перечисленные белки являются прогностически значимыми для развития негативных эффектов, связанных с нарушением нейрорегуляции и эндотелиальной дисфункции. Доказана реализация риска развития прогнозируемых негативных эффектов в виде повышенной частоты развития заболеваний нервной и сердечно-сосудистой системы при повышенной концентрации в крови меди и никеля (R2 = 0,35-0,96; р = 0,0001-0,013). Установленный перечень потенциальных молекул-мишеней (аполипопротеин A-I, витронектин, якорный белок А-киназы 9, транстиретин) и генов, кодирующих их экспрессию (APOA1, VTN, AKAP9, TTR), обоснован в качестве омик-маркеров развития негативных эффектов со стороны сердечно-сосудистой и нервной систем.
Медь и никель в крови, риск здоровью, протеомный профиль плазмы крови, нервная система, сердечно-сосудистая система, аполипопротеин a-i, якорный белок а-киназы 9, витронектин, транстиретин
Короткий адрес: https://sciup.org/142229581
IDR: 142229581 | УДК: 612.12: | DOI: 10.21668/health.risk/2021.1.05
OMIC markers identification for predicting risks of negative effects in children with elevated copper and nickel contents in blood
Proteomic profiling is a promising procedure for examining and substantiating molecular mechanisms of body reactions occurrence and development as a response to adverse impacts; it allows detecting and examining these reactions at early stages in their development prior to cellular damage and damage to organs. Studies aimed at increasing efficiency of adverse effects prediction are especially vital for solving tasks related to early detection and prevention of consequences associated with exposure to chemical environmental factors, first of all, ambient air. Our research goal was to identify omic-markers for predicting risks of negative effects in children with elevated copper and nickel contents in blood. We performed proteomic blood plasma examination in children and modeled cause-and-effect relations. Children with copper and nickel contents in their blood being 3.5 times higher than physiological standard had approximately 20 protein stains that were authentically different from those detected in children from the reference group. We detected correlations between an increase in relative volume of three protein stains including apolipoprotein A-I, anchor protein of A-kinase 9, vitronectin, and a decrease in relative volume of one protein strain including transthyretin and elevated copper and nickel contents in blood (R2 = 0.30-0.44; р = 0.0001-0.008). All the above-mentioned proteins have predictive significance when it comes down to negative effects related to neuroregulation disorders and endothelial dysfunction. It was proven that there was a risk of predicted negative effects such as greater frequency of nervous and cardiovascular system diseases in case copper and nickel contents in blood were elevated (R2=0.35-0.96; р=0.0001-0.013). The established list of potential target molecules (apolipoprotein A-I, vitronectin, anchor protein of A-kinase 9, and transthyretin) and genes that coded their expression (APOA1, VTN,AKAP9,TTR) was substantiated as omic-markers indicating a possibility that negative effects might occur in the cardiovascular and nervous system.
Текст научной статьи Выявление ОМИК-маркеров для прогнозирования риска развития негативных эффектов у детей с повышенным содержанием меди и никеля в крови
-
1 Об утверждении Стратегии развития медицинской науки в Российской Федерации на период до 2025 года: Распоряжение Правительства Российской Федерации от 28 декабря 2012 года № 2580-р [Электронный ресурс] // Гарант.Ру. Информационно-правовой портал. – URL: https://www.garant.ru/products/ipo/prime/doc/70192396/ (дата обращения: 20.09.2019).
В условиях особого высокого уровня загрязнения атмосферного воздуха химическими веществами, к числу которых относятся высокотоксичные соединения никеля и меди, существует риск развития негативных эффектов со стороны органов дыхания, системы крови, иммунной и нервной систем2.
В связи с этим особую значимость приобретает идентификация изменений гомеостаза на молекулярном уровне. Этим требованиям в полной мере соответствуют исследования пептидных пулов, играющих исключительную роль в биорегуляции в живых организмах. Эффективным инструментом, позволяющим выполнить анализ самих пептидов, их конечных и промежуточных метаболитов в клетке, является технология протеомного профилирования [1–4]. Данный метод позволяет исследовать и обосновывать молекулярные этиопатогенетические механизмы возникновения и развития ответных реакций организма на негативные воздействия на самых ранних стадиях их формирования, еще до возникновения симптомов клеточного и органного поражения, то есть на уровне трансформированного проте-омного профиля плазмы крови. Для прогнозирования экспрессии данных пептидов важным является определение генов, их кодирующих, что возможно с помощью существующих баз данных (например Sviss Prot). Обозначенная проблема обусловливает актуальность исследований, направленных на идентификацию молекулярных омик-маркеров с целью раннего выявления и профилактики последствий, ассоциированных с аэрогенным воздействием металлов [5, 6].
Цель исследования – выявление омик-марке-ров для прогнозирования риска развития негативных эффектов у детей с повышенным содержанием меди и никеля в крови.
Материалы и методы. Объектом исследования являлись образцы плазмы крови 20 детей в возрасте 4–6 лет, имеющих повышенное содержание меди и никеля в крови (группа наблюдения), и 10 детей этого же возраста с содержанием в крови изучаемых химических веществ, соответствующих минимальным или референтным значениям (группа контроля).
Настоящие исследования выполнены с соблюдением этических требований Хельсинкской декларации (ред. 2013 г.) и одобрены этическим комитетом ФБУН «Федеральный научный центр медикопрофилактических технологий управления рисками здоровью населения» Роспотребнадзора. Сравниваемые группы сопоставимы по гендерному признаку, возрастному критерию и не имеют различий по социально-экономическим факторам риска здоро- вью. Законные представители детей добровольно подписали информированное согласие на участие и публикацию данных несовершеннолетних, участвующих в обследовании.
Химико-аналитическое исследование крови на содержание никеля и меди осуществляли в соответствии с действующими в Российской Федерации методическими указаниями МУК 4.1.3230-14 «Измерение массовых концентраций химических элементов в биосредах (кровь, моча) методом масс-спектрометрии с индуктивно связанной плазмой»3. Использовано аналитическое оборудование: масс-спектрометр с индуктивно связанной аргоновой плазмой Agilent 7500cx (США).
Исследование протеомного профиля плазмы крови детей группы наблюдения и контроля выполнено по технологии двухмерного электрофореза в полиакриламидном геле в соответствии с методиками, рекомендованными для используемого оборудования [7–9]. Полученные электрофореграммы плазмы крови визуализировали методом окраски серебром и документировали с помощью системы для гель-документирования (BioRad, США). Анализ полученных протеомных карт проводили с помощью программного комплекса PDQuest (Bio-Rad, США). В полученной протеинограмме выделяли значимые белковые пятна по их интенсивности и проводили последующий анализ методом жидкостной хроматографии в сочетании с масс-спектрометрическим анализом (на хроматографе UltiMate 3000 (Германия) и тандемном масс-спектрометре ABSciex 4000 QTRAP с источником ионизации Nanospray 3 (Канада)). Данные тандемных экспериментов обрабатывались программой ProteinPilot, версия 4.5 (AB SCIEX), c идентификацией по базе данных UniProt_sprot_fasta (от 24.11.2017), с выборкой по таксону Homo Sapience. Основная часть информации о полученных белках экстрагирована из баз данных UniProt. Установление гена, которому соответствует идентифицированный белок, выполнено с помощью базы данных HGNC database of human gene name.
Характеристики выборок представляли в виде среднего значения ( М ) и ошибки репрезентативности ( m ). Статистическую значимость различий переменных между группами наблюдения и сравнения определяли по критерию Манна – Уитни. Статистическую обработку данных осуществляли с помощью пакета программ Statistica 10.
Для сопоставительного анализа прогнозируемых негативных эффектов в исследуемой выборке (возраст 4–6 лет) использовали оценку заболеваемости детей в возрасте 10–12 лет (по МКБ-10) по данным углубленных исследований.
Маркерные белковые пятна обосновывали на основании полученных достоверных причинно-следственных связей, описываемых многофакторными моделями зависимости «статистически значимое пятно – концентрация никеля и меди в крови» с помощью линейной регрессии. Достоверность и адекватность полученных моделей оценивали на основе дисперсионного анализа с использованием F -критерия Фишера, коэффициента детерминации ( R 2), t -критерию Стьюдента при статистической значимости p ≤ 0,05.
Результаты и их обсуждение. Анализ результатов химико-аналитических исследований крови на содержание никеля и меди позволил установить, что у детей в группе наблюдения выявлен повышенный в 1,2 раза уровень меди (1,04 ± 0,09 мг/дм3) по сравнению с его концентрацией (0,87 ± 0,09 мг/дм3) в группе контроля ( р = 0,011), а также увеличение содержания никеля в крови (0,007 ± 0,002 мг/дм3) до 3,5 раза относительно значения показателя (0,002 ± ± 0,0001 мг/дм3) в контрольной группе ( р = 0,001). Доля проб с содержанием меди и никеля в крови выше референтных значений4 ( RfL меди = 0,09 мг/дм3,
RfL никеля = 0,001 мг/дм3) составила от 77,0 до 82,0 % от общего числа обследованных детей, в то время как в группе контроля от 10,0 до 20,0 % проб.
В результате проведения двумерного электрофореза получены протеомные карты плазмы крови детей исследуемых выборок, в которых денситометрически определены относительные объемы белковых пятен (рис. 1).
Сравнительный анализ результатов денсито-метрического измерения протеомных карт плазмы крови обследуемых детей позволил выявить наличие достоверных различий относительного объема порядка 20 белковых пятен у детей группы наблюдения относительно соответствующих данных группы контроля (табл. 1).
У детей группы наблюдения установлено увеличение в 8,0–12,2 раза объема белковых пятен № 12 и № 18, а также уменьшение в 5,4 раза объема пятна № 19 относительно аналогичных пятен у детей в группе контроля ( р = 0,0001). Выделенные белки и гены, кодирующие их экспрессию, представлены в табл. 2.

а
Рис. 1. Фрагмент 2D-геля плазмы крови детей с указанием номера белковых пятен: а – индивид группы наблюдения, ; б – индивид группы контроля

б
Таблица 1
Спектр пептидов и белков, выделенных в протеомном профиле плазмы крови детей с повышенным содержанием меди и никеля в крови
|
Номер пятна |
Спектр пептида |
Вероятность идентификации пептида, % |
Наименование белка |
|
№ 2 |
RVDGSVDFYRDWATYK |
1,0 |
Фиколин-2 |
|
VDLVDFEDNYQFAK |
56,6 |
||
|
№ 4 |
VDGSVDFYR |
88,0 |
Фиколин-2 |
|
VDLVDFEDNYQFAK |
99,0 |
||
|
VNVDEVGGEALGR |
99,0 |
Бета-субъединица гемоглобина |
|
|
№ 8 |
INGKPLPGATPAK |
40,6 |
тРНК селеноцистеин 1-ассоциированный белок 1 |
4 Тиц Н.У. Клиническое руководство по лабораторным тестам. – М.: ЮНИМЕД-пресс, 2003. – 570 c.
Окончание табл. 1
|
Номер пятна |
Спектр пептида |
Вероятность идентификации пептида, % |
Наименование белка |
|
№ 9 |
GLCVATPVQLR |
99,0 |
Дополнение C4-B |
|
GSFEFPGDVSK |
64,9 |
||
|
LGQYASPTAKRCCQDGVTR |
1,0 |
||
|
QRIEALSLMHPSISFSLR |
59,0 |
Белок репарации несоответствия ДНК Mlh3 |
|
|
DSEATR |
1,0 |
||
|
FYGFR |
1,0 |
||
|
GVGKVPR |
34,1 |
P2Y-пуриноцептор 12 |
|
|
№ 10 |
NIVQNVR |
26,1 |
Сидерофлексин-3 |
|
№ 11 |
VSFLSALEEYTK |
99,0 |
Аполипопротеин A-I |
|
QGLLPVLESFK |
33,6 |
||
|
VKDLATVYVDVLK |
3,8 |
||
|
VDTLEIQGDVTLSYVQIR |
32,2 |
Галектин-4 |
|
|
№ 12 |
DYVSQFEGSALGK |
99,0 |
Аполипопротеин A-I |
|
QGLLPVLESFK |
59,9 |
||
|
LLKILLEVVK |
52,3 |
Якорный белок А-киназы 9 |
|
|
№ 13 |
CYTAVVPLVYGGETK |
99,0 |
J-цепь иммуноглобулина |
|
FVYHLSDLCK |
99,0 |
||
|
AVHVKAQEDER |
1,0 |
||
|
NHLLFWGVLAFIK |
1,0 |
||
|
RPSTPR |
73,2 |
Белковый фагот |
|
|
EKQFLNAESAYMDPMK |
0,2 |
||
|
DRGGRDYPPLR |
1,0 |
||
|
DSTSTAPDSQR |
0,1 |
||
|
LEPLGPGSSGRPGK |
1,0 |
||
|
VLRDGGCSLPIIPNITK |
0,2 |
||
|
HRAAEAAINILK |
72,9 |
Интерферон-индуцируемый активатор двухцепочечной РНК-зависимой протеинкиназы A |
|
|
№ 15 |
GLEEELQFSLGSK |
99,0 |
Дополнение C4-B |
|
DVPRGQVVK |
1,0 |
||
|
HQDFNSAVQLVENFCR |
99,0 |
Протромбин |
|
|
LAVTTHGLPCLAWASAQAK |
18,3 |
||
|
№ 16 |
GLEEELQFSLGSK |
99,0 |
Дополнение C4-B |
|
MPYSVGFR |
23,6 |
Анкирин-1 |
|
|
CYGMTDDKVDK |
1,0 |
||
|
№ 17 |
SIAQYWLGCPAPGHLR |
77,2 |
Витронектин |
|
№ 18 |
SIAQYWLGCPAPGHLR |
95,9 |
Витронектин |
|
№ 19 |
GSPAINVAVHVFR |
99,0 |
Транстиретин |
|
TSESGELHGLTTEEEFVEGIYK |
99,0 |
||
|
ALGISPFHEHAEVVFTANDSGPR |
94,7 |
||
|
AADDTWEPFASCK |
99,0 |
||
|
№ 22 |
DALSSVQESQVAQQAR |
99,0 |
Аполипопротеин C-III |
|
GWVTDGFSSLK |
99,0 |
||
|
DLTEAVPR |
94,1 |
Миотубулярин |
|
|
RDGPGLER |
42,7 |
НАД-зависимый протеин-деацетилаза сиртуин-1 |
|
|
LKSGSGPVR |
32,4 |
Нуклеоплазмин-3 |
|
|
№ 23 |
SIAQYWLGCPAPGHLR |
99,0 |
Витронектин |
|
DALSSVQESQVAQQAR |
3,9 |
Аполипопротеин C-III |
|
|
GWVTDGFSSLK |
42,2 |
||
|
№ 24 |
ESLSSYWESAK |
99,0 |
Аполипопротеин C-II |
|
№ 27 |
FFGHGAEDSLADQAANEWGR |
96,5 |
Сывороточный амилоидный белок А-1 |
|
FFGHGAEDSLAPQAANEWGR |
1,0 |
||
|
RGPGGAWAAEVISNAR |
93,0 |
Сывороточный амилоидный белок А-2 |
|
|
№ 28 |
SFFSFLGEAFDGAR |
99,0 |
Сывороточный амилоидный белок А-2 |
|
LVAASQAALGLK |
79,1 |
Альбумин |
|
|
APLAKYIGENQDSISSK |
1,0 |
||
|
YIGENQDSISSKLK |
1,0 |
||
|
VFDEFKPLVEEPQNLIK |
99,0 |
||
|
№ 30 |
SAVTALWGK |
99,0 |
Бета-субъединица гемоглобина |
|
VNVDEVGGEALGR |
99,0 |
||
|
VLGAFSDGLAHLDNLK |
55,6 |
||
|
№ 31 |
LLVVYPWTQR |
99,0 |
Субъединица гемоглобина гамма-2 |
Таблица 2
Пример спектра одного из пептидов, имеющего связь с повышенным содержанием одновременно меди и никеля в крови, представлен на рис. 2.
При построении многофакторных моделей установлены прямые причинно-следственные связи между повышенным содержанием в крови меди, никеля и увеличением относительного объема белкового пятна № 12, включающего последовательность белка аполипопротеина A-I и якорного белка А-киназы 9 ( R 2 = 0,30; b 0 = –656,8; b 1 = 1801,1; b 2 = 63518,1; р = 0,008) и белкового пятна № 18 (витронектин) ( R 2 = 0,44; b 0 = –1372,0; b 1 = 2743,3; b 2 = 112937,0; р = 0,0001). Выявлена также обратная зависимость уменьшения относительного объема белкового пятна № 19, включающего транстиретин, от повышенного содержания меди и никеля в крови ( R 2 = 0,35; b 0 = 4870,1; b 1 = –3266,9; b 2 = –79946,5; р = 0,003).
Анализ биологической функции идентифицированных белков плазмы крови по данным отечественной и зарубежной научной литературы позволяет прогнозировать развитие ряда негативных эффектов со стороны сердечно-сосудистой и нервной систем. Так, установленные белки аполипопротеин A-I и витронектин характеризуют преимущественно дисфункцию эндотелия, что в дальнейшем может способствовать развитию артериальной гипертонии и
кардиомиопатии [10]. Аполипопротеин A-I - липопротеин высокой плотности, обеспечивает освобождение клеток от избытка холестерина, тем самым предотвращает образование атеросклеротических бляшек и способствует повышению эластичности эндотелия сосудов [11–13]. Витронектин – это клеточно-адгезивный гликопротеин, продуцируемый и секретируемый клетками печени, который в патологических условиях ассоциируется с клеточными поверхностями, например, с активированными тромбоцитами и с внеклеточными матрицами различных тканей (фибрин) [14]. В результате происходит усиление адгезии тромбоцитов и их местной агрегации, что подтверждается данными экспериментальных исследований [15, 16]. При увеличении относительного объема белкового пятна, содержащего аполипопротеин A-I и витронектин, в условиях повышенной концентрации в крови меди и никеля, можно прогнозировать повреждение эндотелиальных клеток кровеносных сосудов активными формами кислорода, запуск провоспалительной реакции и освобождение цитокинов из тканей сердца, через транскрипционные факторы NF-κB (ядерный фактор «каппа-би») и AP-1 (белок-активатор 1), что представлено в ряде зарубежных и отечественных научных работ [17, 18].
Белки и кодирующие их гены, имеющие связь с повышенным содержанием меди и никеля в крови
|
Номер белкового пятна |
Направление изменения объема белкового пятна |
Наименование белка |
Относительный объем * белкового пятна ( M ± m ), int |
Ген, кодирующий белок |
Код гена, кодирующего белок, в базе данных Sviss Prot |
|
|
группа наблюдения ( n = 20) |
группа контроля ( n = 10) |
|||||
|
12 |
увеличение |
Аполипопротеин A-I |
2099 ± 135** |
171 ± 46 |
APOA1 |
P02647 |
|
Якорный белок А-киназы 9 |
AKAP9 |
Q99996 |
||||
|
18 |
увеличение |
Витронектин |
2731 ± 337** |
340 ± 101 |
VTN |
P04004 |
|
19 |
уменьшение |
Транстиретин |
498 ± 143** |
2687 ± 746 |
TTR |
P02766 |
П р и м е ч а н и е :
int* – интенсивность белкового пятна;
**
– достоверность различий средних значений, р ≤0,05.
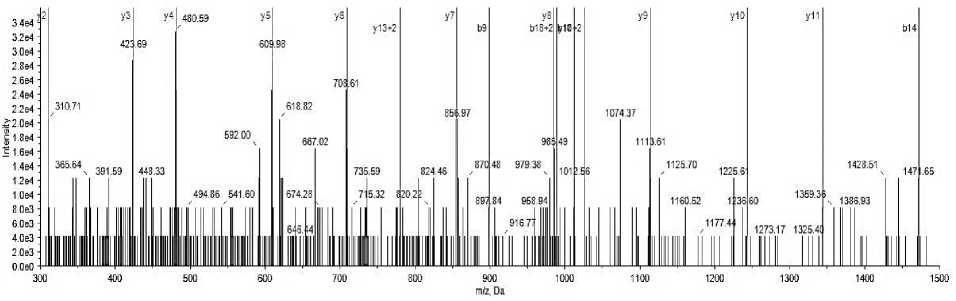
Рис. 2. Спектр пептида TSESGELHGLTTEEEFVEGIYK (Транстиретин) (база данных SwissProt) плазмы крови ребенка в пятне № 19
Якорный белок А-киназы 9 характеризует изменения в нейрорегуляции, поскольку ряд изоформ данного белка способен связываться с рецептором N-метил-D-аспартата в нервно-мышечном соединении и синапсах нейронов, что предполагает изменение в организации постсинаптической специализации [19]. По данным экспериментальных исследований избыточная экспрессия установленного белка может приводить к увеличению длины митохондрий и мембранного потенциала, что снижает чувствительность нейронов к постоянному напряжению в передаче сигналов [19, 20]. В свою очередь известно, что танстиретин – белок, играющий важную роль в развитии нервной системы, нейрональном росте и синаптогенезе, регуляции цитоархитектоники, обеспечивающих когнитивные функции центральной нервной системы (память, эмоциональное состояние, психическое здоровье) [21, 22]. Данное предположение подтверждают результаты зарубежных экспериментальных исследований [21, 23]. Следствием изменения экспрессии транстиретина являются возможные когнитивные нарушения и поведенческие отклонения [23].
По результатам сопоставительного анализа установленных изменений протеомного профиля плазмы крови детей в возрасте 4–6 лет и негативных эффектов, фактически реализованных, у детей в возрасте 10–12 лет выявлена достоверно повышенная в 2,2–3,0 раза частота встречаемости заболеваний по классу болезней сердечно-сосудистой (кардиомиопатии: I42) и нервной систем (функциональные расстройства центральной и вегетативной нервной систем: G90.9, G90.8) относительно соответствующих показателей в группе контроля ( р = 0,001–0,032). При этом у детей старшей возрастной категории установлены достоверные зависимости повышения частоты встречаемости заболеваний нервной системы в виде функциональных расстройств и кардиомиопатий от повышенного содержания в крови меди и никеля ( R 2 = 0,35–0,96; –1,94 ≤ b 0 ≥ –7,22; 1,76 ≤ b 1 ≥ 128,64; р = 0,0001–0,013).
Таким образом, обоснованные омик-маркеры (аполипопротеин A-I, витронектин, якорный белок А-киназы 9, транстиретин) и гены, кодирующие их экспрессию (APOA1, VTN, AKAP9, TTR), могут быть использованы для повышения эффективности
прогнозирования развития негативных эффектов, связанных с нарушением нейрорегуляции и эндотелиальной дисфункции с целью раннего выявления и профилактики негативных последствий со стороны здоровья у детей в условиях высокой аэрогенной нагрузки меди и никеля.
Выводы:
-
1. У детей с повышенным до 3,5 раза содержанием в крови меди и никеля выявлено порядка двадцати белковых пятен, достоверно отличающихся от таковых у детей группы контроля.
-
2. Установлены зависимости увеличения относительного объема трех белковых пятен, включающих аполипопротеин A-I, якорный белок А-киназы 9, витронектин, и уменьшения относительного объема одного белкового пятна, включающего транстиретин, от повышенного содержания в крови меди и никеля ( R 2 = 0,30–0,44; р = 0,0001–0,008).
-
3. Изменения относительного объема белковых пятен, включающих аполипопротеин A-I, якорный белок А-киназы 9, витронектин и транстиретин, являются прогностически значимыми для развития негативных эффектов, связанных с нарушением нейрорегуляции и эндотелиальной дисфункцией.
-
4. Доказана реализация прогнозируемых негативных эффектов в виде повышения частоты развития заболеваний нервной и сердечно-сосудистой системы при повышенной концентрации в крови меди и никеля ( R 2 = 0,35–0,96; р = 0,0001–0,013).
-
5. Для прогнозирования вероятности развития негативных эффектов со стороны сердечно-сосудистой и нервной систем до формирования тканевых и органных поражений обоснован перечень омик-маркеров в виде белков (аполипопротеин A-I, витронектин, якорный белок А-киназы 9, транстиретин) и генов, кодирующих их экспрессию (APOA1, VTN, AKAP9, TTR), позволяющий идентифицировать трансформированный протеомный профиль, ассоциированный с аэрогенным воздействием никеля и меди.
Финансирование. Исследование не имело спонсорской поддержки.
Список литературы Выявление ОМИК-маркеров для прогнозирования риска развития негативных эффектов у детей с повышенным содержанием меди и никеля в крови
- Barbarini N., Magni P. Accurate peak list extraction from proteomic mass spectra for identification and profiling studies // BMC. Bioinformatics. - 2010. - Vol. 11, № 518. - Р. 1-14. DOI: 10.1186/1471-2105-11-518
- Шендеров Б.А. «Омик» - технологии и их значение в современной профилактической и восстановительной медицине // Вестник восстановительной медицины. - 2012. - № 3. - С. 70-78.
- Протеомные методы разделения и анализа белков / Т.А. Полунина, Ю.С. Варшавская, Г.В. Григорьева, Я.М. Краснов // Журнал микробиологии, эпидемиологии и иммунобиологии. - 2014. - № 3. - С. 107-114.
- Ahn S.-M., Simpson R.J. Body fluid proteomics: Prospects for biomarker discovery // Proteomics Clin. Appl. - 2007. -Vol. 1, № 9. - Р. 1004-1015. DOI: 10.1002/prca.200700217
- The proteome of a healthy human during physical activity under extreme conditions (Reviews) / I.M. Larina, V.A. Ivanis-enko, E.N. Nikolaev, A.I. Grigorev // A^ Naturae. - 2014. - Vol. 6, № 3 (22). - Р. 66-75.
- How many human proteoforms are there? / R. Aebersold, J. Agar, I. Amster, M.S. Baker, C.R. Bertozzi, E.S. Boja, C.E. Costello, B.F. Cravatt [et al.] // Nature chemical biology. - 2018. - Vol. 14, № 3. - Р. 206-214. DOI: 10.1038/nchembio.2576
- PROTEAN i12 IEF System. Instruction Manual. - Hercules: Bio-Rad Laboratories, Inc, 2011. - P. 60.
- PROTEAN II xi 2D cell. Instruction Manual. - Hercules: Bio-Rad Laboratories, Inc, 2011. - P. 52.
- ReadyPrep 2-D starter Kit. Instruction manual. - Hercules: Bio-Rad Laboratories, Inc, 2011. - P. 28.
- Chemical constituents of ambient particulate air pollution and biomarkers of in flammation, coagulation and homo-cysteine in healthy adults: a prospec tive panel study / S. Wu, F. Deng, H. Wei, J. Huang, H. Wang, M. Shima, X. Wang, Y. Qin [et al.] // Part. Fibre Toxicol. - 2012. - Vol. 9, № 49. - P. 1-13. DOI: 10.1186/1743-8977-9-49
- Исследование влияния рекомбинантного аполипопротеина А-I на работу сердечной мышцы в эксперименте / Р.А. Князев, Н.В. Трифонова, А.В. Рябченко, М.В. Котова, А.Р. Колпаков, Л.М. Поляков // Патология кровообращения и кардиохирургия. - 2018. - Т. 22, № 4. - С. 88-94.
- Maranhao R.C., Freitas F.R. HDL Metabolism and Atheroprotection: Predictive Value of Lipid Transfers // Advances in Clinical Chemistry. - 2014. - № 65. - Р. 1-41. DOI: 10.1016/B978-0-12-800141-7.00001-2
- Клиническое значение аполипопротеинов А и В / Г.А. Чумакова, О.В. Гриценко, Н.Г. Веселовская, Е.В. Ва-хромеева, А.А. Козаренко // Кардиоваскулярная терапия и профилактика. - 2011. - Т. 10, № 6. - С. 105-111.
- Vitronectin improves cell survival after radiation injury in human umbilical vein endothelial cells / H. Masaharu, Y. Takeshi, N. Katsuko, S.-N. Ai, F. Tomoko, M. Yuichi, G. Takaya, T. Katsushi // FEBS Open Bio. - 2012. - № 2. -Р. 334-338. DOI: 10.1016/j.fob.2012.10.002
- Ruggeri Z.M., Jackson S.P. Platelet Thrombus Formation in Flowing Blood // Platelet biology. - 2013. - № 2. -Р. 399-423. DOI: 10.1016/B978-0-12-387837-3.00020-1
- Plasminogen activator inhibitor-1 and its cofactor vitronectin stabilize arterial thrombi after vascular injury in mice / S. Konstantinides, K. Schafer, T. Thinnes, D.J. Loskutoff // Circulation. - 2001. - № 103. - Р. 576-583. DOI: 10.1161/01.cir.103.4.576
- Fine particulate matter components and emergency department visits for cardiovascular and respiratory diseases in the St. Louis, Missouri-Illinois, Metropolitan Area / S.E. Sarnat, A. Winquist, J.J. Schauer, J.R. Turner, J.A. Sarnat // Environ. Health Perspect. - 2015. - Vol. 5, № 123. - P. 437-444. DOI: 10.1289/ehp.1307776
- Колпакова А.Ф., Шарипов Р.Н., Колпаков Ф.А. Загрязнения воздуха взвешенными частицами как фактор риска сердечно-сосудистых заболеваний // Гигиена и санитария. - 2017. - Т. 96, № 2. - С. 133-137.
- Liu Yu., Merrill R.A., Strack S. A-Kinase Anchoring Protein 1: Emerging Roles in Regulating Mitochondrial Form and Function in Health and Disease (Review) // Cells. - 2020. - Vol. 9, № 298. - Р. 2-12. DOI: 10.3390/cells9020298
- AKAP1 Protects from Cerebral Ischemic Stroke by Inhibiting Drp1-Dependent Mitochondrial Fission / K.H. Flippo, A. Gnanasekaran, G.A. Perkins, A. Ajmal, R.A. Merrill, A.S. Dickey, S.S. Taylor, G.S. McKnight [et al.] // J. Neurosci. -2018. - Vol. 19, № 38. - P. 8233-8242. DOI: 10.1523/JNEUROSCI.0649-18.2018
- Thyroid hormone signaling and adult neurogenesis in mammals / S. Remaud, J.-D. Gothie, G. Morvan-Dubois, B.A. Demeneix // Front. Endocrinol. - 2014. - Vol. 5, № 62. - Р. 1-7. DOI: 10.3389/fendo.2014.00062
- Возможная роль транстиретина в биологическом механизме пептидной нейропротекции / Т.В. Вьюнова, Е.В. Медведева, Л.А. Андреева, Л.В. Дергунова, С.А. Лимборская, Н.Ф. Мясоедов // Молекулярная генетика, микробиология и вирусология. - 2016. - Т. 34, № 3. - С. 104-109.
- Brouillette J., Quirion R. Transthyretin: a key gene involved in the maintenance of memory capacities during aging // Neurobiol. Aging. - 2008. - Vol. 29, № 11. - Р. 1721-1732. DOI: 10.1016/j.neurobiolaging.2007.04.007


