Закономерности взаимодействия бычьего сывороточного альбумина с дифильными молекулами
Автор: Харлов А.Е., Анищук А.Н., Деркач С.Р., Левачев С.М.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Статья в выпуске: 3 (38), 2012 года.
Бесплатный доступ
Методом флуоресценции исследовано взаимодействие глобулярного белка бычьего сывороточного альбумина с дифильными молекулами на примере катионных поверхностно-активных веществ (ПАВ) в водном растворе. Определены количественные параметры связывания катионных ПАВ сывороточным альбумином при образовании комплексов белок-ПАВ переменного состава.
Бычий сывороточный альбумин, поверхностно-активные вещества, флуоресценция, комплексы белок-пав, параметры связывания
Короткий адрес: https://sciup.org/142142558
IDR: 142142558 | УДК: 541.182.64:543.42.062
Interaction between bovine serum albumin and amphiphile molecules of different type
Interaction between globular protein bovine serum albumin and amphiphilic molecules such as cationic surfactants in the aqueous phase have been studied by fluorescence method. It has been found the parameters characterizing protein-surfactant complexes of variable composition formed under binding surfactants by macromolecules of bovine serum albumin.
Текст научной статьи Закономерности взаимодействия бычьего сывороточного альбумина с дифильными молекулами
Сывороточные альбумины обладают уникальной способностью к избирательному связыванию гидрофобных веществ, например жирных кислот, липидов, билирубина, аминокислот [1, 2]. Процессы ассоциации сывороточного альбумина с ПАВ используются при разработке продуктов питания и новых лекарственных веществ, а также при селективной экстракции и очистке белка [3].
В многочисленных исследованиях взаимодействия глобулярных белков, особенно бычьего сывороточного альбумина (БСА), с ионными и неионными ПАВ [4-12] показано, что ПАВ взаимодействуют с БСА с образованием ассоциатов (комплексов) переменного состава, при этом наблюдаются существенные конформационные изменения вторичной структуры белка – доля спиральных a -цепей уменьшается [4, 5, 9, 11, 13], а термическая устойчивость вторичной структуры возрастает [7, 14]. БСА связывает либо индивидуальные молекулы ПАВ, либо образуются мицеллоподобные агрегаты (кластеры) ПАВ [4,5, 8, 10, 15]. При низких концентрациях ПАВ взаимодействие имеет электростатическую природу за счет связывания ионов ПАВ противоположно заряженными группами белка. При высоких концентрациях (в области критической концентрации ми-целлообразования (ККМ) и выше) число связанных молекул ПАВ резко возрастает в результате кооперативности процесса, определяющую роль при этом играют гидрофобные взаимодействия [6, 9, 12, 13, 16-19]. В этом случае мицеллы ПАВ формируются в различных точках частично развернутой полипептидной цепи белка. Размеры связанных агрегатов увеличиваются с ростом концентрации ПАВ вплоть до насыщения белка, причем их размер всегда меньше по сравнению с мицеллами в отсутствие БСА [5, 10, 20].
Целью данной работы является выяснение роли структурных особенностей макромолекулы БСА при связывании катионных ПАВ в смешанных растворах в широком диапазоне концентраций
ПАВ и молярного соотношения компонентов ПАВ/БСА. В работе использовали флуоресцентный метод, который успешно применяется для подобных исследований [11-13, 21-25]. БСА, как и многие белки, содержит флуорофоры: два триптофана ( Trp 135, Trp 214). Триптофан весьма чувствителен к полярности окружения, и спектры флуоресценции могут дать существенную информацию о процессе связывания молекул ПАВ и конформационных изменениях белка.
Материалы и методы
Бычий сывороточный альбумин (БСА) производства « Sigma», глобулярный белок, содержание белка 97 % , молярная масса 6,7∙104 Da, изоэлектрическая точка 4,9. Катионные ПАВ: октаде-кенилдигидроксоэтилметиламмоний хлорид (ОДМАХ) (С 23 Н 48 О 2 NCI), KKМ 1,5 ⋅ 10-4 М, хроматографически чистый, цетилтриметиламмоний бромид (ЦТАБ) (С 19 Н 42 NBr), ККМ 8 ⋅ 10-4 М, производства « Sigma».
Для приготовления растворов БСА, ПАВ и их смесей использовали бидистиллят с удельной электрической проводимостью (22 оС) 6,7 ⋅ 10-6 Ом-1 м-1. Смеси белка с ПАВ получали смешением исходных растворов компонентов. Концентрацию БСА в исследуемых смесях варьировали от 5∙10-6 до 2∙10-5 М. Концентрацию ПАВ варьировали в широком диапазоне до и после ККМ. рН растворов смесей БСА и ПАВ устанавливали равным 5,8.
Концентрацию белка определяли спектрофотометрически по оптической плотности растворов при длине волны 280 нм, используя молярный коэффициент поглощения для БСА 44720 М-1см-1 [24]. Измерения стационарной флуоресценции проводили с применением спектрофлуоримет-ра «Элюмин-2М». Длина волны возбуждения составляла 280 нм. Время жизни флуоресценции определяли из кинетики флуоресценции, измеренной с помощью наносекундного спектрометра «SP-70».
Результаты и их обсуждение
На рисунке 1 представлены зависимости относительной интенсивности флуоресценции БСА I / I 0 (где I 0 , I – интенсивность флуоресценции в отсутствие и в присутствии тушителя соответственно) от концентрации ПАВ при постоянной концентрации белка в растворе C БСА =2 ⋅ 10-5 М. Как видно из рисунка 1, относительная интенсивность флуоресценции резко уменьшается в определенном диапазоне концентраций ПАВ, что свидетельствует о сильном тушении флуоресценции БСА при введении катионных ПАВ.
Можно выделить 3 участка, характерных для обоих катионных ПАВ. В области низких концентраций ЦТАБ (рис. 1а) интенсивность флуоресценции уменьшается с ростом концентрации ПАВ. При концентрации ЦТАБ, равной 6 ⋅ 10-4 М, что соответствует соотношению 30 молекул ЦТАБ на одну молекулу белка, интенсивность флуоресценции достигает наименьшего значения и составляет 26% от исходного значения интенсивности. Далее с увеличением концентрации ЦТАБ интенсивность флуоресценции растет и при 5 ⋅ 10-3 М ЦТАБ составляет 40% от исходного значения I 0 , соотношение компонентов при этом равно 250 молекул ПАВ на молекулу белка. При дальнейшем увеличении концентрации ЦТАБ относительная интенсивность флуоресценции не меняется.
1,1 I / I0
1•
0,9
0,8
0,7
0,6
0,5
0,4
0,3
0,2
(а)
1,1 I / I0
0,9
0,8
0,7
0,6
0,5
0,4
0,3
1∙10-8 1∙10-7 1∙10-6 1∙10-5 1∙10-4 1∙10-3 1∙10-2
(б)
0,2
1∙10-8 1∙10-7 1∙10-6 1∙10-5 1∙10-4 1∙10-3 1∙10-2
CЦТАВ, М
CОДМАХ, М
Рис. 1. Зависимость относительной интенсивности флуоресценции БСА от концентрации добавленного в раствор белка катионного ПАВ: ЦТАБ (а) и ОДМАХ (б), С БСА = 2 ⋅ 10-5 М, рН= 5.8, Т=293К
Аналогичная зависимость получена и при введении катионного ПАВ ОДМАХ (рис. 1б). Первоначально с ростом концентрации ОДМАХ интенсивность флуоресценции уменьшается, достигая наименьшего значения при 5 - 10-4 М ОДМАХ, при этом она составляет 32% от исходной интенсивности флуоресценции БСА, что соответствует 25 молекулам ПАВ на одну молекулу БСА. С увеличением концентрации ОДМАХ до 1 - 10-3 М интенсивность флуоресценции несколько увеличивается, достигая 38% от I 0 , что соответствует 50 молекулам ОДМАХ на молекулу белка, и далее остается постоянной. Необходимо отметить, что максимальное тушение флуоресценции в обоих случаях при введении ЦТАБ и ОДМАХ наблюдается при концентрациях катионных ПАВ в области ККМ.
Тушение флуоресценции может протекать по механизму динамического или статического тушения [25]. В обоих случаях зависимость относительной интенсивности от концентрации тушителя описывается уравнением Штерна-Фольмера (1):
I o /I = 1 + k q T o [Q, I o /I = 1 + K sv [Q], (1) где I0 , I - интенсивность флуоресценции флуорофора в отсутствие и в присутствии тушителя соответственно; kq - константа скорости реакции тушения; т0 - истинное время жизни флуоресценции (в отсутствие тушителя); [ Q ] - концентрация тушителя; K SV - константа Штерна-Фольмера (константа тушения).
Тушение происходит в результате образования в основном состоянии нефлуоресцирующего комплекса белок-ионное ПАВ. Если спектр поглощения такого комплекса близок к спектру поглощения белка, то возбуждающий свет будет поглощаться как свободными, так и связанными в комплекс молекулами БСА, а флуоресцировать будут лишь свободные молекулы БСА. При тушении по статическому механизму константа Штерна-Фольмера представляет собой константу равновесия образования комплекса в основном состоянии [26].
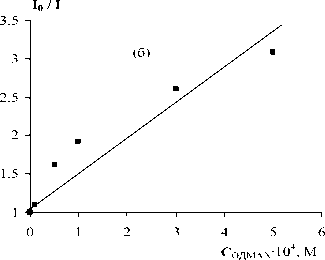
Полученные экспериментальные данные в области низких концентраций катионных ПАВ (см. рис. 1) проанализированы в рамках уравнения Штерна-Фольмера (1) (рис. 2 и табл. 1).
Линейный характер зависимости интенсивности флуоресценции БСА от концентрации ПАВ свидетельствует об образовании комплекса БСА-катионное ПАВ. Константы комплексообразования, вычисленные по уравнению (1), для обоих ПАВ близки и равны (4,7 ± 0,2) - 103 М ' 1 для ЦТАБ и (4,3 ± 0,4) - 103 М-1 для ОДМАХ (см. табл. 1). Истинное время жизни флуоресценции БСА т0 равно 3.9 - 10-9 с и не зависит от концентрации ПАВ, что свидетельствует о статическом тушении. Эти данные совпадают с литературными данными [12, 21]. В работе [21] при измерении времени жизни флуоресценции БСА в присутствии додецилсульфата натрия показано, что тушение флуоресценции протекает преимущественно по механизму статического тушения и обусловлено появлением молекул ионных ПАВ в ближайшем окружении триптофановой группы Trp 135. Для определения значимости механизма статического тушения в работе [23] построена зависимость ln ( I 0 /I) от числа связанных молекул цетилпиридиний хлорида. Полученная линейная зависимость позволила авторам сделать вывод о преимущественно статическом тушении флуоресценции БСА катионным ПАВ.
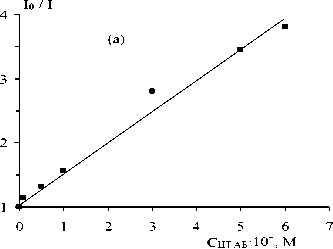
Рис. 2. Тушение флуоресценции БСА катионными ПАВ: ЦТАБ (а) и ОДМАХ (б), С бса = 2 - 10-5 М, рН =5.8, Т=293К
На рисунке 3 приведены спектры флуоресценции БСА и комплексов БСА-ЦТАБ. Длина волны максимума флуоресценции БСА без ПАВ Х м=340 нм. В области низких концентраций ПАВ образование комплексов (в диапазоне молярных соотношений ПАВ/белок от 2,5 до 30 моль
ЦТАБ/моль БСА) сопровождается постепенным сдвигом длины волны максимума флуоресценции в коротковолновую область и уменьшением интенсивности флуоресценции. Максимальный сдвиг на 8 нм ( λ м =332 нм) наблюдается при образовании комплексов БСА-ЦТАБ с молярным соотношением 30 моль ЦТАБ/моль БСА, что соответствует минимальному значению I/I 0 (рис. 1 а). Далее при увеличении соотношений компонентов в области высоких концентраций ПАВ длина волны максимума флуоресценции остается практически постоянной.
Таблица 1
Параметры связывания цетилтриметиламмоний хлорида (ЦТАБ), октадекенилдигидроксоэтилметиламмоний хлорида (ОДМАХ) и цетилтриметиламмоний хлоридом (ЦТАХ) бычьим сывороточным альбумином (БСА), рассчитанные по уравнению Штерна – Фольмера и по изотермам связывания, рН 5,8, Т=293К
|
ПАВ |
K SV ⋅ 10-3, М-1 |
n |
n н |
K ⋅ 10-3, М-1 |
|
ЦТАБ |
4.7 ± 0.2 |
75 ± 3 |
1.57 ± 0.01 |
1.2 ± 0.1 |
|
ОДМАХ |
4.3 ± 0.4 |
70 ± 26 |
1.38 ± 0.06 |
1.2 ± 0.4 |
|
ЦТАХ* |
8.9 ± 0.1 |
133 ± 20 |
1.91 ± 0.02 |
4.0 ± 0.4 |
* – данные работы [11].
Сдвиг максимума спектра флуоресценции комплексов БСА-ОДМАХ равен 4 нм и соответствует образованию комплексов при соотношении 25-50 моль ОДМАХ/моль БСА (рис. 1 б). Необходимо отметить, что присутствие ПАВ приводит к сдвигу длины волны максимума спектров поглощения на 1-3 нм в коротковолновую область.
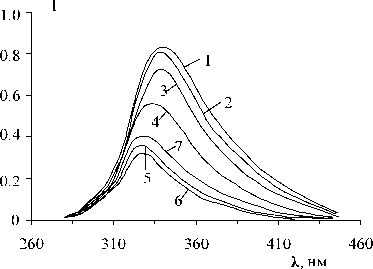
Рис. 3. Спектры флуоресценции БСА при различных концентрациях ЦТАБ, добавленного в раствор белка. С БСА = 2 ⋅ 10-5 М, С ЦТАБ ⋅ 104, М: 0(1), 0.1(2), 0.3(3), 1(4), 3(5), 5(6), 7(7), рН = 5.8, Т=293К
Полученные данные согласуются с результатами работ [11, 21, 27], в которых изучено взаимодействие БСА с додецилсульфатом натрия и цетилтриметиламмоний хлоридом и высказано предположение о существовании в растворе трех равновесных форм белка: собственно белок, комплекс белок-ПАВ и «частично денатурированный» белок. Использование кругового дихроизма показало уменьшение доли a –спиралей во вторичной структуре белка при ассоциации с ПАВ при больших концентрациях [11, 12]. Количественное соотношение между равновесными формами зависит от концентрации ионного ПАВ.
Экспериментальные данные по тушению флуоресценции БСА катионными ПАВ (см. рис. 1) позволяют рассчитать число ν (моль ПАВ/моль БСА) молекул ПАВ, связанных одной молекулой белка при разных молярных соотношениях компонентов в растворе. В области низких концентраций при С ЦТАБ < 6 ⋅ 10-4 М и С ОДМАХ < 5 ⋅ 10-4 число связанных молекул рассчитывали по формуле:
ν = a C S / C P ; (2)
a = ( I - I 0)/( I min - I 0) или a = ( I - 1) /( I min - 1) , (3) I 0 I 0
где a – степень связывания ПАВ белком; С S , С Р – общая концентрация ПАВ и белка, соответственно; I 0 , I и I min – интенсивность флуоресценции БСА, смесей БСА с ПАВ при различных концентрациях ПАВ и минимальная интенсивность.
На рисунке 4 приведены изотермы связывания катионных (зависимость среднего числа молекул ПАВ, связанных одной молекулой БСА) в области низких концентраций ПАВ. В соответствии с [28, 29] образование комплексов белок-ПАВ переменного состава может быть представлено в виде ступенчатого равновесного процесса присоединения молекулы ПАВ (S) к макромолекуле белка (P), уже имеющей некоторое количество связанных молекул ПАВ.
Каждое из этих превращений характеризуется соответствующей константой равновесия. Константы комплексообразования каждой стадии в общем случае не равны, поскольку процесс связывания следующей молекулы зависит от числа уже присоединенных к белку молекул ПАВ.
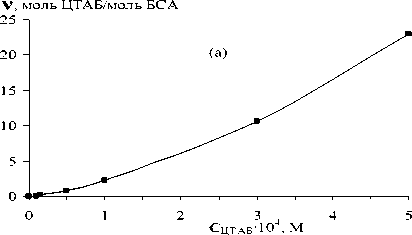
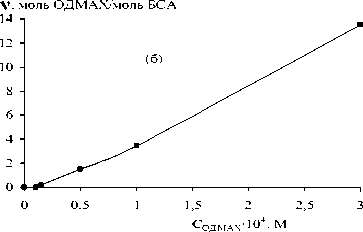
Рис. 4. Изотермы связывания ЦТАБ (а) и ОДМАХ (б) БСА при низких концентрациях катионных ПАВ.
На графиках: точки - экспериментальные данные, линии - обработка экспериментальных данных по уравнению (4), рН 5,8, Т=293К
С учетом кооперативности процесса число v молекул ПАВ, связанных макромолекулой белка, в зависимости от концентрации ПАВ может быть выражено следующим уравнением (4) [28, 29]:
v = n ( K [ S ]) n н , (4)
1 + ( K [ S ]) n н где n - число связанных лигандов (ПАВ); K - константа связывания ПАВ белком; пн - коэффициент кооперативности; [ S ] - концентрация лиганда (ПАВ). Параметры связывания ЦТАБ и ОДМАХ сывороточным альбумином представлены в таблице 1. Интересно отметить, что число n связанных в комплекс молекул катионного ПАВ приблизительно равно числу анионных групп макромолекулы белка. Сумма аминокислотных остатков аспарагиновой и глутаминовой кислот в БСА равна 100 [24].
Для сравнения в таблице 1 приведены константы образования комплекса БСА с цетилтриметиламмоний хлоридом (ЦТАХ) при рН 7.0 [11]. Константы для всех катионных ПАВ примерно одинаковы, более высокие значения KSV и K для ЦТАХ можно объяснить величиной рН. Депротонирование кислотных групп БСА при увеличении рН (от 5,8 до 7,0) приводит к конформационным изменениям белка, что способствует доступности молекул ПАВ к гидрофобным областям связывания, электростатические взаимодействия также увеличиваются. Соответственно коэффициент кооперативности и число связанных молекул в случае ЦТАХ выше аналогичных параметров для ЦТАБ и ОДМАХ при меньшем значении рН.
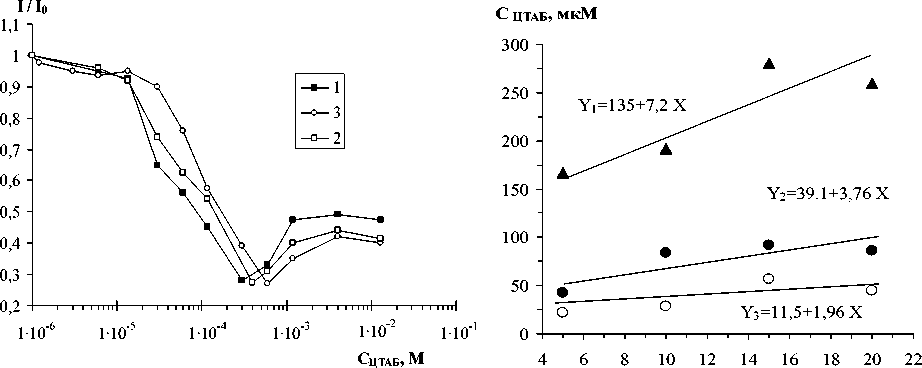
Рассмотрим влияние концентрации БСА на флуоресцентные характеристики его смесей с ЦТАБ. На рисунке 5 приведены зависимости относительной интенсивности флуоресценции от концентрации ЦТАБ при различных концентрациях БСА. Видно, что с увеличением концентрации белка необходима более высокая концентрация ПАВ, чтобы достичь одинакового уменьшения интенсивности флуоресценции (одинакового значения I / 1 0 ).
Полученные данные позволяют провести количественную оценку процесса связывания поверхностно-активного вещества белком способом, предложенным в работе [22]. Процесс связывания описывается суммарным упрощенным равновесием ( S - ПАВ, БСА - белок) S + БСА о- EGAS. Константа равновесия (эффективная константа связывания) равна (5):
K b = [ EGAS ]/{[ S ][ БСА ]} . (5)
При низких концентрациях ПАВ (до насыщения белка) равновесная концентрация комплекса в уравнении (5) равна концентрации связанного ПАВ ([EGAS]=[S]связ.), а равновесная концентра- ция белка равна концентрации белка в растворе. С учетом того, что [S]связ./[БСА] равно числу молекул, связанных одной молекулой БСА, последнее уравнение преобразуется в (6):
K b = V /[ S ] своб. , (6)
где V - число молекул ПАВ, связанных одной молекулой белка, [ S ] своб . - концентрация ПАВ, несвязанного белком.
C БСА , мкМ
Рис. 5. Относительная интенсивность флуоресценции БСА Рис. 6. Концентрации ЦТАБ, в зависимости от концентрации ЦТАБ при концентрациях необходимые для достижения данного
БСА С БСА - 105, М: 0,5(1), 1,0(2), 1,5(3), рН =5,8, Т=293К значения относительной интенсивности
I/I 0 флуоресценции БСА, в зависимости от концентрации БСА в растворе, для I/I 0 : 0,77(1), 0,60(2), 0,40(3), рН= 5,8, Т=293К
Влияние концентрации БСА на изменение флуоресценции с ростом концентрации ЦТАБ (см. рис. 5) обусловлено равновесным распределением молекул ПАВ между комплексом белок-ПАВ и водной средой, что совпадает с литературными данными [22]. Очевидно следующее соотношение (7):
[ S = [ S своб. + V .[ БСА ]. (7)
На рисунке 6 в координатах уравнения (7) представлены зависимости концентрации ЦТАБ от концентрации БСА в смеси при постоянных значениях I/I 0 . Среднее число молекул ПАВ, связанных одной молекулой БСА, рассчитывается по тангенсу угла наклона прямой к оси абсцисс, а концентрация ЦТАБ, несвязанного белком, определяется по точке пересечения прямой с осью ординат. Рассчитанные параметры связывания приведены в таблице 2.
Необходимо подчеркнуть, что образование комплексов белок-ионное ПАВ переменного состава является сложным процессом, сопровождающимся постепенным присоединением молекул ПАВ до насыщения белка и конформационными изменениями макромолекул [5, 10, 20], и вообще говоря, этот процесс не может быть охарактеризован одной константой. Поэтому рассчитанные величины эффективной константы связывания ЦТАБ альбумином (см. табл. 2) позволяют обсуждать лишь оценочные характеристики взаимодействия белка с ПАВ.
Как видно из таблицы 2, константа K b не возрастает с увеличением числа связанных молекул ЦТАБ, что свидетельствует о низкой кооперативности процесса. Этот вывод совпадает с данными таблицы 1, индекс кооперативности для системы ЦТАБ-БСА равен п н =1.57 ± 0.01. Незначительное уменьшение K b при увеличении V может быть обусловлено или конформационными изменениями белка и/или увеличением электростатического отталкивания между заряженными группами ЦТАБ при увеличении числа связанных молекул в условиях низкой кооперативности (при низкой концентрации ПАВ, недостаточной для формирования мицеллоподобных агрегатов на по-липептидной цепи белка).
Таблица 2
Параметры связывания ЦТБА белком при различных значениях относительной интенсивности флуоресценции БСА, рН 5,8, Т=293К
|
I/I 0 |
[ S ] своб ⋅ 106, М |
ν , моль ЦТАБ/моль БСА |
K b ⋅ 10-5, М-1 |
|
0,77 |
12 |
2,0 |
1,7 ± 0,7 |
|
0,60 |
39 |
3,8 |
1,5 ± 0,5 |
|
0,55 |
38 |
4,4 |
1,1 ± 0,6 |
|
0,40 |
135 |
7,2 |
0,53 ± 0,04 |
Выводы
Флуоресценция БСА тушится катионными ПАВ ЦТАБ и ОДМАХ в водном растворе. Константа тушения, представляющая собой константу равновесия связывания молекул ПАВ белком и рассчитанная по уравнению Штерна–Фольмера, равна (4,7 ± 0,2) ⋅ 103 и (4,3 ± 0,4) ⋅ 103 М-1 для ЦТАБ и ОДМАХ соответственно. Тушение происходит преимущественно по статическому механизму [24]. Тушение флуоресценции БСА обусловлено взаимодействием макромолекул белка с молекулами ПАВ, сопровождающимся образованием комплексов БСА – катионное ПАВ. При низких концентрациях ПАВ комплексообразование характеризуется низкой кооперативностью 1 < n н < 2, общее число связанных молекул ПАВ примерно равно числу анионных групп в молекуле БСА. В процессе последовательного увеличения числа молекул ПАВ в комплексе эффективная константа связывания несколько уменьшается. Существенный вклад, наряду с электростатическими взаимодействиями, вносят гидрофобные взаимодействия между молекулами катионного ПАВ и БСА. Длина волны максимума флуоресценции комплекса БСА – катионное ПАВ сдвинута на 4-8 нм в коротковолновую область по сравнению со спектром флуоресценции БСА.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований, грант РФФИ № 10-03-00310-а.


