Значение индекса ALPS и способы оценки глимфатической системы - современное состояние
Автор: Ахлестина А.В., Петряйкин А.В., Владзимирский А.В.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Обзор
Статья в выпуске: 3 т.25, 2025 года.
Бесплатный доступ
В данной работе представлен глубокий анализ научных исследований и публикаций, посвящённых методам оценки глимфатической системы головного мозга. Особое внимание уделяется неинвазивным способам её анализа с использованием индекса ALPS, который рассчитывается на основе диффузионно-взвешенных МРТ-изображений. В процессе исследования были изучены как российские, так и зарубежные публикации, касающиеся этой темы. Ключевые результаты этих исследований были проанализированы и сопоставлены. В заключение предложены направления для дальнейшего научного поиска в данной области.
Глимфатическая система, индекс ALPS, МРТ, диффузионно-взвешенные изображения, нейродегенеративные заболевания, болезнь Альцгеймера
Короткий адрес: https://sciup.org/149149280
IDR: 149149280 | DOI: 10.24412/1999-7264-2025-3-40-50
The ALPS Index and Methods for Glymphatic System Assessment: A Current Overview
This paper provides an in-depth analysis of scientific research and publications on methods for evaluating the glial system of the brain. Particular attention is given to non-invasive analysis methods using the ALPS index, calculated based on diffusion-weighted MRI images. The study examined Russian and foreign publications on this topic. The key results of these studies were analyzed and compared. Finally, directions for further scientific research in this area are proposed.
Текст научной статьи Значение индекса ALPS и способы оценки глимфатической системы - современное состояние
Долгое время считалось, что в головном мозге человека и других млекопитающих отсутствует лимфообращение, поскольку не было обнаружено гистологических доказательств наличия в нём лимфатических сосудов [1,2]. Кроме того, гематоэнцефалический барьер, расположенный в головном мозге, значительно снижает процесс транскапиллярной фильтрации и образования тканевой жидкости, которая впоследствии становится лимфой [3]. Это предполагаемое отсутствие лимфообращения вызывало значительные вопросы, поскольку мозг — это орган с активным метаболизмом, который производит большое количество продуктов распада и токсинов, включая крупные белковые соединения. Определенная роль в выведении продуктов метаболизма отводилась цереброспинальной жидкости (ликвору), тем не менее, оставалось не до конца изученным, как именно продукты метаболизма, выделяемые паренхимой мозга, достигают крупных ликворных пространств — желудочков мозга, цистерн. Однако в 2012 году международная группа учёных из Рочестерского университета под руководством Майкен Недергаард (Дания), провела эксперимент на мышах, доказав, что ликвор циркулирует не только в желудочках мозга, но и в его паренхиме. Используя флуоресцентные метки, исследователи выяснили, что ликвор проникает в паренхиму через периваскулярные пространства, которые окружают артерии, проникающие в ткань мозга. Точно так же он выводится из мозга через периваскулярные пространства вокруг мелких вен. Эту систему, обнаруженную учёными, они назвали «глимфатической». Такое название было выбрано из-за важной роли глиальных клеток в её функционировании и её роли в выведении продуктов метаболизма, что характерно для лимфатической системы.
Исследователи считают, что движение жидкости в периваскулярных пространствах осуществляется благодаря пульсации сосудов, расположенных в этих пространствах, осмотическому давлению, а также активной роли глиальных клеток, особенно астроцитов.
Следует отметить что функция глимфатической системы, по мнению исследователей, тесно связана с активностью белков аквапоринов, в частности аквапорина-4. Аквапорины представляют собой белки, образующие каналы, по которым вода проходит через клеточные мембраны. Эти каналы помогают молекулам воды преодолеть липидный бислой. Аквапорин-4 является преобладающим водным каналом клеток мозга. Наиболее высокая концентрация данного белка обнаруживается в ножках астроцитов — глиальных клеток, формирующих гематоэнцефалический барьер.
В исследованиях на лабораторных животных было обнаружено, что отсутствие белка аквапорин-4 (AQP4) приводит к замедлению тока ликвора по периваскулярным пространствам. В результате клиренс растворенных веществ снижается примерно на 70%. Это открытие позволяет предположить, что астроциты играют важную роль в интрапаренхиматозном токе ликвора [1]. В настоящее время остаётся открытым вопрос о том, как именно аквапорин-4 регулирует поток жидкости в глимфатической системе. Согласно одной из гипотез, вода и растворённые вещества попадают из периартериальных пространств в паренхиму через промежутки между концевыми отростками астроцитов. При этом поток в этих промежутках каким-то образом регулируется AQP4, который является водным каналом, поэтому молекулы растворённых веществ не могут проходить через него напрямую.
По мнению исследователей, образовавшись в желудочках головного мозга и проникнув в паренхиму мозга, ликвор частично смешивается с тканевой интерстициальной жидкостью, а оттекая от паренхимы, обеспечивает тем самым клиренс метаболитов. Затем основная его масса всасывается в кровоток через арахноидальные грануляции [1,2], а отчасти также и в 41
лимфатическую систему через влагалища нервов, в которые продолжаются мозговые оболочки (Рис. 1).
Отмечается, что флуоресцентно-меченный в-амилоид (белок, предположительно, участвующий в патогенезе болезни Альцгеймера) в эксперименте выводился из паренхимы головного мозга по периваскулярным пространствам, а генетически заданное отсутствие AQP4 у лабораторных мышей существенно снижало клиренс в-амилоида, что позволило исследователям предположить о значительной роли дисфункции открытой ими системы в развитии нейродегенеративных заболеваний, в том числе, болезни Альцгеймера [1,4].
По мнению исследователей, этот же механизм обеспечивает удаление тау-белков, накопление которых также характерно для нейродегенеративных заболеваний, таких как упомянутая болезнь Альцгеймера и таупатий. Также этот процесс способствует выведению глиофиламентов — крупных белковых структур, которые образуются в процессе мозговой активности [2].
Interstitial fluid and solute clearance
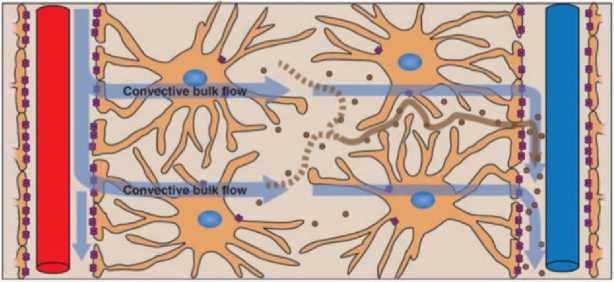
AQP4
Para-arterial influx
Paravenous efflux
Interstitial solutes Solute clearance
Рис. 1. Современное представление о функционировании глимфатической системы на клеточном уровне. Голубыми стрелками продемонстрировано направление тока жидкости в системе, фиолетовым цветом выделены молекулы белка-аквапорина. (Цит. по [1]).

Water flux
Отдельно стоит отметить тот факт, что скорость обмена по глимфатической системе варьирует вместе с циклом сон-бодрствование. Микроскопическая оценка движения флуоресцентных индикаторов, введенных в большую цистерну, выявила увеличение на ~ 95% периартериального притока красителя в мозг мышей во время сна или под наркозом по сравнению с бодрствующими животными [5]. Особое значение при этом имела фаза медленного сна.
Наличие лимфатических сосудов в оболочках головного мозга было многократно подтверждено гистологически, и не отрицается широким кругом исследователей, однако функционально оболочки головного мозга не относятся к паренхиме мозга и не являются его частью.
Способы оценки глимфатической системы
В течение последующих пяти лет после ее открытия оценка глимфатической системы проводилась с помощью двухфотонной микроскопии или введения гадолиний-содержащего контраста и носила исключительно инвазивный характер, что затрудняло изучение ее закономерностей, в том числе в рамках исследования человеческого мозга. Введение индикаторов людям не проводилось, за исключением ограниченного числа исследований [6,7]. За этот период в некоторых исследованиях была установлена взаимосвязь между снижением функции глимфатической системы и рядом патологических состояний, например, нормотензивной гидроцефалией [8].
В 2017 году группа исследователей из Японии [9] предложила новый неинвазивный метод изучения функции глимфатической системы, допускающий оценку ее активности у 42
человека. Данный метод “Diffusion tensor image analysis along the perivascular space (DTI-ALPS)” – анализ изображений тензора диффузии вдоль периваскулярных пространств – предполагал оценку движения молекул воды в трех взаимно перпендикулярных плоскостях (x, y, z) по латеральному краю боковых желудочков мозга по ходу основных проводящих волокон (то есть, прежде всего, в белом веществе головного мозга). В области ассоциативных и проекционных волокон в правом и левом полушарии выделялись точки интереса (ROI), затем подсчитывался индекс ALPS: ALPS = (Dxxpro + Dxxass) / (Dyypro + Dzzass) где Dxxpro, Dxxass, Dyypro, Dzzass – компоненты тензора диффузии, измеренные в областях проекционных и ассоциативных волокон. Исходя из формулы, в идеальной математической системе значение индекса ожидаемо должно быть равно единице, тем не менее на практике значения индекса отклоняются в большую либо меньшую сторону (Рис. 2).
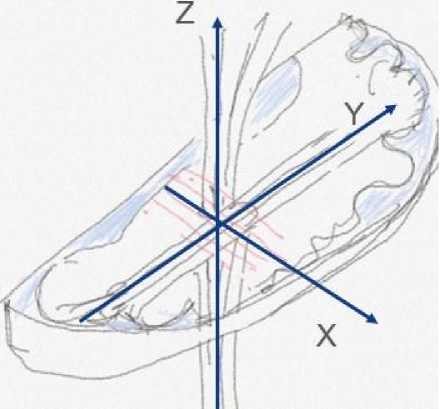
Рис. 2. Взаиморасположение проводящих пучков в головном мозге, перивентрикулярных сосудов (выделены красным) и их соответствие осям Х, Y, Z.
В исследование были включены пациенты с болезнью Альцгеймера, а также пациенты с когнитивными нарушениями разной степени тяжести. Всего в исследовании принял участие 31 пациент (14 мужчин и 17 женщин; возрастной диапазон составил 51–89 лет; медиана — 76 лет). Из 31 пациента 16 страдали болезнью Альцгеймера, остальные имели различные невыраженные когнитивные нарушения, такие как снижение памяти [9]. Была подтверждена значительная корреляция между тяжестью проявления болезни Альцгеймера (степенью выраженности когнитивных нарушений согласно опроснику «MMSE» - mini–mental state examination) и снижением индекса ALPS, отражающего функциональность глимфатической системы. Опросник MMSE – это широко применяемая методика для оценки когнитивных нарушений. Он представляет собой анкету, которую пациент заполняет самостоятельно. В зависимости от набранных баллов – от 0 до 30 – определяется степень выраженности деменции.
Прикладные исследования
Открытие японских ученых позволило расширить спектр изучения глимфатической системы. Появились, в том числе российские работы, посвященные изучению активности данной системы. В российском исследовании, посвященном закономерностям развития перитуморозного отека при менингиомах [10] значение индекса ALPS в группе пациентов без отёка составило 1,510±0,19, при менингиомах с отеком — 1,308±0,19, различие статистически значимо (p=0,014). Таким образом, установлено снижение индекса ALPS при менингиомах с отеком. В другой российской работе, посвященной общим закономерностям развития перитуморозного отёка при различных новообразованиях мозга (менингиомах, глиомах Grade III—Grade IV, метастазах, лимфомах) [11] было выявлено значимое снижение индекса ALPS у пациентов с вызывающими перитуморозный отек новообразованиями головного мозга. Отдельным достоинством данного исследования [11] следует назвать участие в нем контрольной группы здоровых добровольцев. Так было выявлено, что при опухолях без перитуморзного отека значения ALPS были близки к таковым для неизмененного мозга, что может свидетельствовать о более высокой глимфатической функции, которая способствует клиренсу интерстициальной жидкости и предотвращению возникновения отека.
В 2021 году была опубликована работа [12], посвященная исследованию индекса ALPS в когорте пожилых пациентов. В исследование были включены пациенты без когнитивных нарушений, пациенты с болезнью Альцгеймера и пациенты c начальными когнитивными нарушениями. Для оценки состояния данных пациентов также был использован вышеназванный опросник MMSE (краткая шкала оценки психического статуса). Также в данной работе использовалась шкала ADAS-Cog 11 – тест оценки тяжести болезни Альцгеймера, состоящий из 11 пунктов, как это следует из его названия, широко используемый в практической медицине и клинических испытаниях с 1984 года, входящий в «золотой стандарт» диагностики болезни Альцгеймера. В ходе исследования было выявлено, что показатели этих шкал имеют обратную зависимость от изменений индекса ALPS. Также было обнаружено, что колебания индекса ALPS значительно различаются в трёх исследуемых группах пациентов: без признаков деменции, с лёгкими когнитивными нарушениями, с диагностированной болезнью Альцгеймера.
Была установлена взаимосвязь между отложениями амилоида и тау-белка и изменениями индекса ALPS у пациентов с сахарным диабетом [13]. Тау-протеин – белковое соединение, в норме присутствующее в головном мозге, но также его избыточное накопление характерно для болезни Альцгеймера и других форм деменции. Содержание данных соединений в головном мозге устанавливалось путём позитронно-эмиссионной томографии (ПЭТ). Значимые отрицательные корреляции между значениями индекса ALPS и накоплением амилоида (по данным ПЭТ) были обнаружены в коре височных и теменных долей с обеих сторон, а также в задней поясной извилине слева (серое вещество головного мозга). Поясная извилина (лат. gyrus cinguli) является частью поясной коры и расположена непосредственно над мозолистым телом. Поясная кора считается частью лимбической доли. В этой же анатомической области, по данным российских исследований, происходят изменения морфометрических показателей головного мозга при деменции — наиболее значимыми зонами, отличающими группы пациентов с деменцией и умеренными когнитивными расстройствами, является кора задних отделов поясных извилин и надкраевая извилина слева [14]. Кроме того, у всех испытуемых была обнаружена сильная отрицательная корреляция между индексом ALPS и накоплением тау-белка. Удивительно, что индекс ALPS связан с отложением тау-белка и амилоида в областях мозга, которые не связаны с белым веществом вокруг боковых желудочков, что обычно оценивается с помощью метода ALPS.
Были предприняты попытки установить взаимосвязь колебаний индекса с болезнью Паркинсона, которая также является нейродегенеративным заболеванием и связана с накоплением белка альфа-синуклеина – небольшого белкового соединения, состоящего из ~140 аминокислот. Данный белок, как известно, патологически накапливается в нейронах черной субстанции, чем вызывает их дисфункцию и гибель нервных клеток [15,16]. Поскольку данная патология также связана с избыточным накоплением белковых веществ, было выдвинуто предположение, что её возникновение может быть обусловлено сбоями в работе глимфатической системы и нарушениями циркуляции жидкости в головном мозге.
Исследование, в котором проводилось сравнение между группами пациентов с болезнью Паркинсона и группой пациентов с эссенциальным тремором показало более низкие значения индекса ALPS в группе пациентов с болезнью Паркинсона и более высокие значения индекса в группе пациентов, страдающих от эссенциального тремора [17].
В исследовании были проанализированы значения индекса ALPS у пациентов с артериальной гипертензией и сравнены с показателями контрольной группы людей без признаков гипертонии [18]. Результаты показали, что значения индекса в группе с артериальной гипертензией значительно ниже, чем в контрольной группе. Кроме того, у всех испытуемых наблюдалась достоверная отрицательная корреляция между ALPS-индексом и значениями артериального давления, а также с пульсовым давлением — разницей между систолическим и диастолическим артериальным давлением. Это может означать, что артериальная гипертензия, которая приводит к очаговым сосудистым изменениям в головном мозге, вызывает их косвенно, через нарушение динамики тока жидкости в мозге.
В исследовании, в котором приняли участие 133 пациента с проявлениями болезни малых сосудов различной степени выраженности [19], была выявлена корреляция между снижением внимания и памяти и низкими значениями индекса ALPS. В исследовании с более чем двумя тысячами участников [20] были получены данные о том, что чем ниже значения индекса, тем более выражены проявления болезни малых сосудов на МР-изображениях. Независимо от проявлений болезни малых сосудов, низкий индекс ALPS был достоверно ассоциирован с другими неблагоприятными МР-признаками, такими как наличие на изображениях расширенных периваскулярных пространств (в том числе в области базальных ядер [20,21]), сосудистыми лакунами [21] и корковой атрофией [20].
Как уже было сказано выше [8], инвазивные исследования показали снижение функциональности глимфатической системы у пациентов с идиопатической нормотензивной гидроцефалией – нейродегенеративным заболеванием, которое клинически характеризуется снижением когнитивных способностей, нарушением походки и недержанием мочи, а по данным МР-изображений – расширением желудочковой системы на фоне внутричерепного давления, находящегося в пределах возрастной нормы. Идиопатическая нормотензивная гидроцефалия зачастую является состоянием, коморбидным болезни Альцгеймера. Неинвазивные исследования, основанные на расчете индекса ALPS [22], продемонстрировали значительно более низкие значения индекса в группе пациентов с истинной идиопатической нормотензивной гидроцефалией и более высокие значения индекса в группе пациентов, не подходящих под критерии истинной нормотензивной гидроцефалии. При этом при дифференциальной диагностике истинной нормотензивной гидроцефалии и имитирующих ее состояний различия индекса ALPS показали более высокую диагностическую значимость, чем индекс Эванса или изменения угла мозолистого тела, которые обычно используются для дифференциальной диагностики данного состояния [22].
Так как одним из способов лечения нормотензивной гидроцефалии является проведение шунтирования, была предпринята попытка измерения индекса до операции и в послеоперационной когорте пациентов [23]. При этом усредненные значения для группы послеоперационных пациентов оказались выше, чем значения индекса до проведения шунтирования. Стоит отметить, что повышение индекса определялось исключительно в той части послеоперационной когорты пациентов, которая демонстрировала улучшение симптоматического состояния после операции. В группе пациентов после операции, у которых не было улучшения их симптоматического состояния, повышения индекса ALPS достоверно не отмечалось.
Были предприняты попытки установить взаимосвязь между колебаниями индекса и возрастом пациентов. В некоторых работах, посвященных взаимосвязи возраста и индекса ALPS, была установлена отрицательная корреляция между возрастом и значениями индекса. Однако в данные исследования также включались предпочтительно пациенты с болезнью Альцгеймера, эссенциальным тремором и другими нейродегенеративными состояниями. Можно назвать лишь отдельные работы, в которых анализировались данные условно здоровых участников исследования в возрасте от 50 лет и старше [24] (по итогам работы была установлена отрицательная корреляция), однако лица более молодого возраста в когорту испытуемых включены не были.
Также были предприняты попытки изучить изменения этого индекса у детей и молодых людей в возрасте от 12 до 46 лет, страдающих эпилепсией. Однако не все специалисты считают эту работу объективной. Дело в том, что у детей не все волокна белого вещества полностью сформированы, и некоторые авторы не считают корректным включать их в исследование наравне со взрослыми. Кроме того, в данной работе анализировались только пациенты, у которых уже были эпилептические проявления, в то время как условно здоровые люди не рассматривались в большом количестве.
Кроме многократно упомянутого нами выше опросника MMSE (краткая шкала оценки психического статуса) и шкалы ADAS-Cog 11, используемой для диагностики болезни Альцгеймера, снижение индекса ALPS коррелировало в других работах со снижением показателей по тестам Time Up and Go test (TUG) – тест для оценки подвижности пациента и его способности поддерживать равновесие [25] и Montreal Cognitive Assessment (MoCA-J) – форме скрининга когнитивных нарушений [21].
Заключение
В апреле 2024 года группа японских исследователей, возглавляемая Taoka, основоположником метода, опубликовала объемный обзор, посвященный индексу ALPS [26], его применению с момента внедрения, предположительным достоинствам и недостаткам метода. В данной работе было указано, что, несмотря на все достоинства метода ALPS-DTI, данный метод не может быть однозначным критерием оценки глимфатической системы, так как при его использовании объективно измеряется исключительно диффузия воды вдоль периваскулярных пространств в белом веществе головного мозга в ограниченной анатомической области (по краям боковых желудочков головного мозга). Функциональность глимфатической системы может нарушаться при нейродегенеративных заболеваниях, опухолях и других патологиях как в белом, так и в сером веществе головного мозга, затрагивая различные анатомические области. Это создает определённые ограничения в исследованиях. Однако, как уже упоминалось ранее, в некоторых работах изменения индекса в белом веществе коррелировали со структурными изменениями в сером веществе [13]. К сожалению, как считают авторы метода ALPS, в настоящее время не существует единого метода, который мог бы полностью оценить работу глимфатической системы. Этот метод должен включать в себя оценку циркуляции жидкости как на микроуровне в сером и белом веществе, так и в крупных ликворных пространствах. Taoka и его коллеги надеются, что в будущем будет разработан метод, который объединит все существующие на данный момент способы изучения глимфатической системы и циркуляции жидкости в центральной нервной системе.
Несмотря на ограничения метода, измерение индекса ALPS остается наиболее дешевым, быстрым, безопасным методом оценки глимфатической системы, позволяющим по изменению ее функциональности в белом веществе, судить об общем состоянии данной системы в головном мозге. Многочисленные работы, подтвердившие статистическую значимость колебаний данного индекса при нейродегенеративных и других заболеваниях головного мозга, подтверждают высокую актуальность дальнейшего изучения возможностей метода. Так как во всех проанализированных нами работах не было предпринято попыток установить эталонное значение индекса в популяции и его нормальное распределение по возрастным группам, в том числе в зависимости от пола и других легко определяемых критериев, дальнейший научный поиск должен продолжаться, включая данное направление. Необходимо определить статистически обоснованные нормы изменений этого индекса в зависимости от пола и возраста пациентов. Также важно выяснить, как на ALPS влияют наиболее распространенные в популяции изменения головного мозга: болезнь малых сосудов, расширение наружных ликворных пространств, увеличение желудочков и другие.
Такое масштабное исследование возможно благодаря технологиям искусственного интеллекта, которые активно применяются в лучевой диагностике, в том числе для научных целей [27].
Как уже было отмечено, в идеальной математической модели значение индекса должно быть равно единице. Однако на практике у пациентов этот индекс может отклоняться от единицы как в сторону увеличения, так и в сторону уменьшения. Чтобы оценить адекватность математической модели, необходимо провести испытания на упрощённом фантоме, который имитирует движение жидкости в мозге человека, исключая индивидуальные особенности каждого пациента [28]. Таким образом, при анализе степени изменчивости индекса, мы будем отталкиваться не от идеальной модели, где индекс равен 1,00, а от значений фантома, который будет отражать реальные идеальные значения индекса в клинической практике.
Выводы
-
1. Получены доказательства наличия в головном мозге так называемой «глимфатической системы», аналогичной лимфатической системе других органов и тканей, ответственной за выведение из головного мозга токсинов и крупных белковых соединений. Установлена важная роль этой системы в удалении крупных белковых соединений. Это позволяет предположить, что она играет ключевую роль в развитии многих нейродегенеративных заболеваний, таких как болезнь Альцгеймера, болезнь Паркинсона и различные виды деменции, которые характеризуются накоплением белков в мозге.
-
2. Активность глимфатической системы можно измерить как инвазивными, так и неинвазивными методами. Одним из таких неинвазивных способов является измерение индекса ALPS-DTI. На данный момент этот индекс считается одним из самых простых, доступных и безопасных способов оценки глимфатической системы.
-
3. Многие исследования подтвердили взаимосвязь между снижением индекса ALPS и развитием нейродегенеративных заболеваний. Кроме того, было установлено, что снижение индекса может быть связано с некоторыми другими патологическими состояниями, такими как образование отёков при опухолях.
-
4. Индекс ALPS не отражает функционирование глимфатической системы в целом, поскольку он измеряется в определённом анатомическом регионе головного мозга — в белом веществе по краю тел боковых желудочков. Тем не менее индекс ALPS продемонстрировал свою эффективность в качестве диагностического критерия, и требуется дальнейшее исследование его возможностей. В частности, необходимо определить значения индекса для различных возрастных групп условно здоровых пациентов. Также важно сравнить математическую модель индекса с данными «идеального» фантома, который имитирует движение жидкости в головном мозге человека.
-
5. Перспективным выглядит проведение популяционного исследования данного индекса для различных возрастных групп.
Вклад авторов . А.В. Петряйкин: формулирование идеи, подбор иллюстраций, редактирование и утверждение окончательного варианта статьи; А.В. Ахлестина: формулирование идеи, сбор, обработка и анализ материала, интерпретация результатов исследования, редактирование текста рукописи; А.В. Владзимирский: редактирование и утверждение окончательного варианта статьи. Все авторы прочли и одобрили окончательный вариант статьи.
Финансирование. Данная статья подготовлена авторским коллективом в рамках НИР «Научное обеспечение стандартизации, безопасности и качества магнитно-резонансной томографии», (№ ЕГИСУ: № 123031500007-6) в соответствии с Приказом от 17.12.2024 г. № 1184 "Об утверждении государственных заданий, финансовое обеспечение которых осуществляется за счет средств бюджета города Москвы государственным бюджетным (автономным) учреждениям подведомственным Департаменту здравоохранения города Москвы, на 2025 год и плановый период 2026 и 2027 годов" Департамента здравоохранения города Москвы.
Заявление об информационном согласии. Данное обзорное исследование было основано на опубликованных работах и поэтому не требовало одобрения этического комитета.


