Анализ свободных легких цепей иммуноглобулинов сыворотки крови у больных хроническим лимфолейкозом в процессе химиоиммунотерапии
Автор: Голенков А.К., Клинушкина Е.Ф., Катаева Е.В., Чуксина Ю.Ю., Митина Т.А., Трифонова Е.В., Захаров С.Г., Высоцкая Л.Л., Черных Ю.Б., Белоусов К.А., Савин А.О., Марьина С.А., Когарко И.Н., Когарко Б.С.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.17, 2021 года.
Бесплатный доступ
Современная химиоиммунотерапия (ХИТ) хронического лимфолейкоза (ХЛЛ) постоянно совершенствуется, что требует изучения дополнительных методов оценки ее эффективности. Существующий иммунофенотипический метод позволяет определять минимальную остаточную болезнь (МОБ) с точностью <0,01% опухолевых клеток, что обозначается как неизмеряемая остаточная болезнь (НМОБ). Показано, что достижение НМОБ улучшает отдаленные результаты лечения. Идея предпринятой работы заключается в том, что при достижении НМОБ часть опухолевых клеток может остаться in situ за счет их адгезивных свойств, в то время как синтез свободных легких цепей (СЛЦ) опухолевыми клетками позволяет определить их в крови
Хронический лимфолейкоз, свободные легкие цепи, иммунофенотип, химио-иммунотерапия
Короткий адрес: https://sciup.org/170175828
IDR: 170175828
Analysis of free light chains of blood serum immunoglobulins in patients with chronic lymphocytic leukemia during chemoimmunotherapy
Modern chemoimmunotherapy (CIT) of chronic lymphocytic leukemia (CLL) is constantly being improved, which requires the study of methods for assessing its effectiveness. The existing immunophenotypic method allows the determination of minimal residual disease (MRD) with an accuracy of <0.01% of tumor cells, which is referred to as unmeasurable residual disease (IMRD). It has been shown that the achievement of BMD improved treatment results. The idea of the undertaken work is that, upon reaching BMP, some of the tumor cells can remain in situ due to their adhesive properties, while the synthesis of free light chains (FLC) by tumor cells makes it possible to detect them in the blood. Materials and methods
Текст научной статьи Анализ свободных легких цепей иммуноглобулинов сыворотки крови у больных хроническим лимфолейкозом в процессе химиоиммунотерапии
Введение. Проблема химиоиммунотерапии (ХИТ) хронического лимфолейкоза (ХЛЛ) получила свое широкое развитие с момента опубликования работы [1], показавшей клиническое преимущество комбинации противоопухолевых препаратов флударабин, циклофосфан, ритуксимаб (FCR) в сравнении с флударабином и циклофосфаном (FС). Дальнейшее совершенствование программ лечения ХЛЛ было связано с синтезом новых противоопухолевых препаратов, действие которых было направлено на ключевые сигнальные пути, обеспечивающие функцию опухолевых клеток.
К ним относятся ингибитор брутонтирозин-киназы ибрутиниб (ибр.), ингибитор BCL-2 вене-токлакс, ингибитор PI3K – иделалисиб и новые генерации моноклональных антител к CD20. Оценивая в целом современный иммунохимиотера-певтический потенциал ХЛЛ, следует отметить его высокую противоопухолевую избирательность. В свою очередь, это требует совершенствования оценочных систем лечения, которые необходимы для сравнительного анализа эффективности новых лекарственных препаратов, а также для установления причинной связи между минимальной остаточной болезнью (МОБ) и отдаленными результатами лечения.
Это положение подтверждается опубликованными работами, показавшими что МОБ является независимым прогностическим фактором выживаемости без прогрессии (ВБП) и общей выживаемости (ОВ) [2]. Высокая воспроизводимость результатов, указывающих на связь МОБ и ОВ и ВБП, была получена при использовании иммунофено-типического анализа с повышенной разрешающей способностью [3]. При чувствительности <0,01% опухолевых клеток (неизмеряемая МОБ – НМОБ) эта закономерность сохраняется для стандарт- the method of analysis of variance.
Results. It was found that in 32 out of 50 studied patients, the FLC clone (64%) was established in the blood serum. No FLC changes were found in 18 clonal changes (18%). When studying the phenotype of the FLC clone in 32 patients, и-type was determined in 26 (81.3%), λ-type in 6 (18.7%). Conducting HIT according to FCR programs. BR, ibrutinib proportionally reduced the concentration of tumor FLC and, to a lesser extent, FLC of physiological antibody producers. In 30% of cases, upon reaching IMOB, the concentration of FLC and the и /Л ratio had a tumor character.
ных и инновационных программ лечения. Более точным местом для установления НМОБ является костный мозг, так как там реже достигается НМОБ, чем в периферической крови [4], что, по-видимому, связано с адгезивностью опухолевых лимфоцитов [5]. Этот факт подтверждает точку зрения о том, что топографическая ассиметрия распространения опухолевых лимфоцитов при ХЛЛ, обусловленная адгезивными свойствами, может создавать условия для функционирования остаточной опухоли in situ [6]. При этом опухолевые клетки не выходят в циркуляцию, что может искажать результаты НМОБ. В этой связи следует отметить, что СЛЦ не связаны с клеточной адгезией и могут быть определены в циркуляции, независимо от адгезивных свойств опухоли. Важно отметить, что продукция свободных легких цепей (СЛЦ) иммуноглобулинов сыворотки крови доказана у большинства больных ХЛЛ [7, 8]. Поэтому в группе больных СЛЦ(+) ХЛЛ методом определения СЛЦ (Free Light) можно визуализировать остаточную болезнь in situ в случаях НМОБ и более точно прогнозировать отдаленные результаты лечения.
Методы исследования. Исследовано 50 больных ХЛЛ, мужчин 31, женщин 19, в возрасте 61 год (30-76). Впервые выявленный ХЛЛ диагностирован у 20, фаза прогрессии или рецидива установлена у 23, состояние полной (ПО) или частичной (ЧО) ремиссии было у 7 больных. У 11 больных исследование СЛЦ проводили в динамике до и после проведенных только программ ИХТ FCR, BR (бен-дамустин и ритуксимаб) или в сочетании с ибру-тинибом (BR+ибрутиниб). Диагноз заболевания устанавливали в соответствии с существующими рекомендациями [9, 10]. Стадию болезни устанавливали согласно критериям Rai. Эффективность лечения оценивали по критериям международной рабочей группы по ХЛЛ (IWCLL) [11]. Иммунофе-нотипирование лимфоцитов крови проводили методом проточной цитофлуориметрии (2-лазерный проточный цитометр “Facs Calibur”, США) с использованием панели моноклональных антител “Becton Dickinson”. Определяли экспрессию CD45; CD19; CD20; CD22; CD79b; CD5; CD23; CD43; CD200; CD25; CD38, а также экспрессию легких цепей к и Л. Оценку МОБ проводили методом 4-х цветной проточной цитофлуориметрии по международному стандартизованному протоколу для мониторинга МОБ ХЛЛ и в модификации European Research Initiative in CLL (ERIC) [12].
Концентрацию СЛЦ сыворотки крови определяли на иммунохимическом анализаторе Immage
800 “Beckman Coulter”, США. В качестве реактивов использовали поликлональные антисыворотки к к и λ СЛЦ (Binding Site, Англия). Всем больным проводили стандартные клинические исследования, принятые в гематологическом стационаре. При статистической обработке результатов использовали метод дисперсионного анализа.
Результаты. Данные полученных концентраций СЛЦ анализировали вместе с клиническими данными на момент исследования СЛЦ в связи с результатами проведенной ХИТ. При анализе результатов установлено, что из 50 обследованных больных ХЛЛ СЛЦ клон был установлен у 32 (64%). (таблица 1).
Таблица 1
Подгруппы больных с ХЛЛ в зависимости от наличия клона свободных легких цепей иммуноглобулинов сыворотки крови
|
Число больных |
СЛЦ клон* |
||||
|
есть |
% |
нет |
% |
||
|
к |
λ |
||||
|
50 |
26 |
6 |
64 |
18 |
36 |
|
32 |
|||||
* к/Л отношение 0.6 (0.26-1.65)
У большинства больных (26 из 32) клон СЛЦ был фенотипа к (81.3%). Опухолевый клон, секретирующий СЛЦ λ-типа был установлен у 6 из 32 больных (18.7%). Это очень важное положение свидетельствует о том, что у большинства больных с ХЛЛ опухолевые клетки секретируют СЛЦ. Это согласуется с ранее опубликованными на-
Таблица 2
Изменение концентраций к и Л СЛЦ у 18 больных с СЛЦ (-) ХЛЛ
|
Число больных |
СЛЦ мг/л |
||
|
к |
λ |
к /Л |
|
|
9 |
↑ |
↑ |
0,30-1,59 |
|
7 |
↑ |
↓ |
|
|
2 |
↓ |
↓ |
|
|
Нормальные значения |
7,3 (3,3-19,4) |
12,7 (5,7-26,3) |
0,6 (0,26-1,65) |
Из данных таблицы 2 видно, что у 9 больных концентрации к и Л СЛЦ были повышены (поликлональный характер изменений). У 7 больных концентрация цепи к была повышена, а Л-цепи была снижена. В 2 наблюдениях концентрации к и λ СЛЦ были снижены. Причем в некоторых наблюдениях к/Л соотношения выходили за пределы нормальных значений, но они не сопровождались повышением концентрации одной из СЛЦ, а нао блюдениями [7, 8].
При анализе полученных результатов у 18 больных где не было установлено клональных изменений концентраций СЛЦ (к/Л отношение в пределах нормы – 0.30-1.59) данные имели разнонаправленный характер.
борот сопровождались избирательным снижением концентрации одной из них. По-видимому, это следует расценивать как дизрегуляцию в системе антителопродуцентов при ХЛЛ.
Следующим этапом анализа полученных результатов было изучение концентрации СЛЦ у 32 первичных и предлеченных больных ХЛЛ с клональной секрецией СЛЦ.
Таблица 3Концентрация СЛЦ у 32 первичных и предлеченных СЛЦ (+) больных ХЛЛ
|
Количество больных |
Опухолевый клон и -типа |
Опухолевый клон λ-типа |
Предлеченность |
|||||
|
32 и -26 λ -6 |
СЛЦ и |
СЛЦ λ |
и /А |
СЛЦ и |
СЛЦ λ |
и /А |
||
|
75,8 мг/л (16,7-700) |
10,1 (мг/л) (5,7-26,3) |
7,5 |
1,59 мг/л (1,12-2,58) |
12,4 мг/л (7,5-169) |
0,12 |
и 14/26 53,8% |
λ 4/6 66% |
|
|
Нормальные значения |
и 7,3 мг/л (3,3-19,4) |
А и /А 12,7 мг/л 0,6 мг/л (5,7-26,3) (0,26-1,65) |
||||||
Как следует из таблицы 3 среди 32 изученных больных СЛЦ клон фенотипа и установлен у 26, а λ-фенотипа у 6 больных. Оценивая концентрации СЛЦ у больных с фенотипом и СЛЦ-клона, следует отметить что концентрация клональной СЛЦ-и у этих больных составляла 75,8 мг/л (16,7-700), что значительно превышало нормальные значения для и-СЛЦ 7,3 мг/л (3,3-19,4). Концентрация Л СЛЦ, не вовлеченной в опухолевый процесс была несколько ниже нормы и составляла 10,1 мг/л. При этом нормальные значения составляли 12,7 мг/л (5,.7-26,3).
Ключевым признаком наличия клона опухолевых клеток, продуцирующих СЛЦ -фенотипа было и/Л отношение, которое носило клональный характер, так как в 12,5 раз превышало аналогичный показатель нормальных значений (7,5 против 0,6). Из 26 больных этой группы у 14 (53,8%) была предлеченность ХИТ, что в целом уменьша- ло интенсивность продукции СЛЦ опухолевыми клетками. У 6 больных с клональным характером изменений СЛЦ Л-фенотипа, и/Л отношение составляло 0,12 и было в 5 раз меньше нормальных значений аналогичного показателя (0.6). Концентрация опухолевой СЛЦ λ-фенотипа составляла 12,4 мг/л и практически не отличалась от средних значений нормы (12,7-МЕ) с колебаниями концентраций (от 7,5 до 169 мг/л). Предлеченность больных в этой группе составляла 66% (4 из 6). Следует отметить, что в эту группу были включены больные с клональным и/Л отношением <0,26, с повышением концентраций λ СЛЦ у 3.
В качестве подтверждения роли проводимой противоопухолевой ИХТ на продукцию СЛЦ был проведен анализ концентрации опухолевых СЛЦ-и и неопухолевых СЛЦ-Лу 11 больных с впервые выявленным ХЛЛ до проведения ИХТ.
Таблица 4
|
Число больных |
СЛЦ мг/л (Ме*) |
% получавших ХИТ |
||
|
11 |
и |
λ |
и /А |
|
|
121 (30,3-700) |
11,4 (8,38-61) |
9,04 (3,15-33,8) |
0 |
|
|
Нормальные значения |
7,3 (3,3-19,4) |
12,7 (5,7-26,3) |
0,6 (0,26-1,65) |
|
Концентрация опухолевых СЛЦ- и и неопухолевых СЛЦ-Ху 11 больных с впервые выявленным ХЛЛ
*Ме-медиана
Из таблицы 4 следует, что Ме концентрации опухолевых СЛЦ-и у 11 больных составляла 121 мг/л (30,3-700), что значительно превышало аналогичный показатель в группе больных, где 53,8% проводилась ИХТ (75,8 мг/л). Очевидно, что это различие связано с супрессивным влиянием ХИТ на опухолевые клетки, секретирующие СЛЦ-клон. Эти данные позволяют утвердительно оценивать метод free light assay в качестве дополнительного оценочного критерия эффективности противоопухолевого лечения ХЛЛ. Следует отметить, что под влиянием ИХТ, применяемой для лечения больных в нашем исследовании не произошло существенного снижения СЛЦ-λ, которая не была ассоциирована с опухолевым клоном и по существу отражала состояние нормальных антитело-продуцентов. Падение концентрации опухолевой СЛЦ-и в группе больных, получавших ИХТ про- изошло на 37,4%, а нормальной λ-цепи на 11,5%. (таблица 3; 4). Это соотношение может указывать на достаточно высокую степень избирательности противоопухолевого действия применяемых про- грамм лечения.
Более доказательно эта закономерность продемонстрирована у 15 больных СЛЦ-х ХЛЛ, получавших курсы ХИТ.
Таблица 5.
Концентрация СЛЦ у 15 больных ХЛЛ -фенотипа, получавших курсы ХИТ
|
Число больных |
СЛЦ мг/л (Ме*) |
|||
|
15 |
х |
λ |
х /Л |
% получавших ХИТ |
|
30 (16,7-290) |
9,01 (5,2-24,1) |
3,3 (1,65-23,3) |
100 |
|
|
Нормальные значения |
7,3 (3,3-19,4) |
12,7 (5,7-26,3) |
0,6 (0,26-1,65) |
|
*Ме-медиана
Как следует из таблицы 5, у этих больных Ме концентрации опухолевой СЛЦ-х составляла 30 мг/л (16,7-290). Концентрация неопухолевой λ-СЛЦ составляла 9,01 мг/л (5,2-24,1). Отношение х/Л составляло 3,3 (1,65-23,3). О высокой избирательности (FCR, BR, ибрутиниб) программ лече- ния ХЛЛ свидетельствуют (рисунок 1) достоверные снижения концентрации опухолевой СЛЦ-х (p=0,05) в зависимости от химиотерапевтической нагрузки и отсутствии достоверных изменений СЛЦ нормальных антителопродуцентов.
Свободные легкие цепи каппа
Свободные легкие цепи лямбда
80-
60-
40-
20-
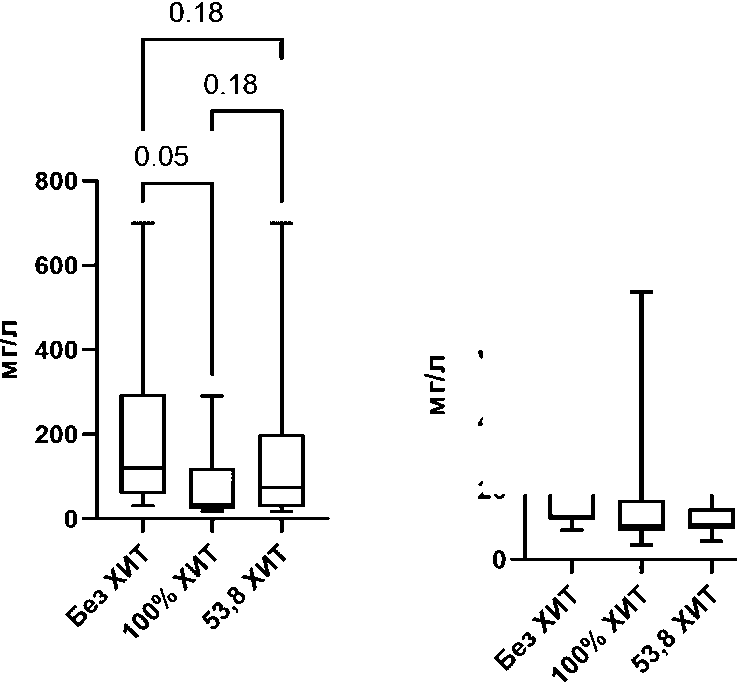
Рисунок 1 . Сравнительный анализ концентраций СЛЦу 26 больных ХЛЛ СЛЦ- х в зависимости от проводимой ИХТ
100-1
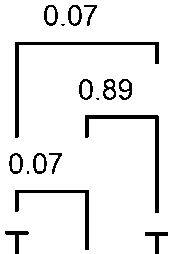
У 26 больных ХЛЛ с СЛЦ-х клоном опухолевых клеток была изучена кратность изменения концентрации СЛЦ относительно нормальных их значений.
Таблица 6
Кратность изменения концентраций СЛЦ у 26 больных с ХЛЛ СЛЦ -фенотип
|
Число больных 26 |
СЛЦ |
|
|
и |
λ |
|
|
16,5 (1,6-95,8) |
0,74 (0,40-0,96) у 18 больных 1,65 (1,1-4,8) у 8 больных |
|
Как видно из таблицы 6, в исследуемой смешанной группе больных, где у 53,8% проводили ХИТ, было превышение концентраций опухолевой СЛЦ-и в 16,5 раза. Кратности изменения концентраций неопухолевой λ-СЛЦ носили разнонаправленный характер и были снижены (0,74) у 18 и повышены (1,6) у 8 больных. Этот анализ показывает, что при повышении концентраций опухолевых СЛЦ-и одновременно происходило снижение не вовлечённой в опухолевый процесс λ-СЛЦ, что может свидетельствовать о супрессии нормальных антителопродуцентов, связанных с патологией В-лимфопролиферативного процесса или проводимой ХИТ.
Изучение концентрации СЛЦ опухолевого клона до и после ИХТ было проведено у 11 больных ХЛЛ, которых лечили по программам FCR, BR, BR+B, BR+ибрутиниб. У всех больных исходно диагностированы резистентность или прогрессия заболевания. Интервалы между исследованиями СЛЦ составляли 8 месяцев (ме) (1-10 месяцев). В этой клинической модели было обращено внимание на объективный статус, достигнутый за пери- од лечения в сравнении с данными СЛЦ-анализа. Достигнуто совпадение результатов по указанным параметрам у 10 из 11 больных. Значения СЛЦ соответствовали прогрессии, ремиссии, резистентности, стабилизации. В одном наблюдении такого совпадения не было достигнуто. При констатации полной ремиссии, подтвержденной МОБ (3,5%), концентрация опухолевой СЛЦ-и снизилась с 148 до 37,6 мг/л (норма 7,3 мг/л), и/Л отношение 4,0-4,57 (норма 0,6). Это очень важное положение свидетельствует о том, что Free Light assay обладает большей разрешительной способностью, чем иммунофенотипическое исследование и визуализирует нодальную и экстранодаль-ную остаточную опухоль.
Дальнейший анализ касался изучения концентрации СЛЦ и и/Л отношений у 12 больных ХЛЛ после завершения FCR, BR, FLUCAM, ибр. программ и поддерживающего лечения ритукси-мабом. Одновременно проводили анализы МОБ, клинического статуса и легких цепей на мембране лимфоцитов (таблица 7).
Таблица 7
Сравнительная характеристика показателей МОБ и СЛЦ у 12 больных ХЛЛ после завершения программ ИХТ и поддерживающего лечения ритуксимабом
|
N исследования |
Клиническая характеристика |
МОБ (ИФТ) %* |
СЛЦ мг/л |
ИФТ ЛФ |
|||
|
и |
λ |
и /Л** |
|||||
|
Статус |
ХТ |
||||||
|
1 |
Н.О. |
RB (4) |
2 |
13,2 |
8,76 |
1,5 |
и |
|
2 |
ПО |
FCR (6)+R |
0,02 |
22,1 |
68,1 |
0,32 |
λ |
|
3 |
ПО |
FCR (6)+R |
0,0002 |
1,12 |
7,56 |
0,15 |
и |
|
4 |
ПО |
FCR (6)+R+FLUCAM |
0,002 |
2,9 |
8,95 |
0,21 |
и |
|
5 |
ЧО |
FCR (6)+R+RB |
0,007 |
28 |
17,3 |
1,62 |
и |
|
6 |
ПО |
FCR (6)+R |
1 |
1,96 |
7,68 |
0,26 |
λ |
|
7 |
Н.О. |
BR-11 |
7,6 |
2,58 |
15,9 |
0,16 |
λ |
|
8 |
ЧО |
FCR (6)+R |
0,02 |
15,8 |
19,2 |
0,82 |
λ |
|
9 |
ЧО |
RB (7) |
0,02 |
12,6 |
7,91 |
1,59 |
м |
|
10 |
ПО |
Ибр→RC |
0,56 |
12,5 |
15,9 |
0,79 |
м |
|
11*** |
в/в IIст. |
до леч. |
н,д, |
1,59 |
33,4 |
0,04 |
λ |
|
12 |
в/в IIст. |
до леч. |
н,д, |
30,3 |
8,8 |
3,4 |
м |
*НМОБ <0.01%; ПО- полный ответ; ЧО- частичный ответ; Н.О.- нет ответа
** м/Л- норма 0.6 (0.26-1.65); ***в/в-впервые выявленный
В исследовании №1 (таблица 7) отсутствие клинического ответа сопровождалось значительным снижением МОБ (2%), но оставалась повышенной концентрация опухолевой СЛЦ-м при верхней границе нормы м/Л отношения (1,5). В этом наблюдении можно говорить о наступлении МОБ и СЛЦ-ответов при запаздывании нодальной редукции массы опухоли, или остаточной опухоли in situ после лечения.
В исследовании №2 (таблица 7) достигнутый полный клинический ответ подтверждался глубоким ИФТ ответом (МОБ – 0,02%), однако оставалась значительно повышенной концентрация опухолевой СЛЦ-Л. При этом м/Л отношение оставалось в пределах нижней границе нормальных показателей, но ниже средних значений. Однако в связи с высокой концентрацией СЛЦ-λ, что совпадает λ фенотипом опухолевых В-лимфоцитов, можно предполагать наличие минимального опухолевого клона. Это означает, что СЛЦ метод оценки остаточной болезни при СЛЦ-позитивном ХЛЛ более чувствительный, чем существующие методы. Вероятно, адгезивность опухолевых лимфоцитов удерживает их остаточное количество в депо, и они не могут быть определены в циркуляции, а СЛЦ могут свободно выходить в циркуляцию и определяться в крови.
В исследовании №3 (таблица 7) можно говорить о полном клиническом ответе, подтвержденном НМОБ (<0,01%), супрессией опухолевой СЛЦ-м и неопухолевой СЛЦ- λ после курсов FCR и поддержки ритуксимабом. При этом клональное соотношение м/Л (0,15) Л-типа при -типе опухолевых лимфоцитов связано с преимущественной супрессией опухолевых СЛЦ-м и преобладанием Л-СЛЦ нормальных антителопродуцентов. В данном наблюдении совпадение результатов.
В исследовании №4 (таблица 7) получен полный клинический ответ после FCR+R+FLUCAM, подтвержденный НМОБ с супрессией опухолевых лимфоцитов типа м до 0,002%. Соответственно, СЛЦ-м была значительно ниже нормальных значений (2,9 мг/л). Очевидно, что в этом наблюдении определяется высокая избирательность противоопухолевого действия программы лечения, содержащей моноклональные антитела против В-лимфоцитов. Следует отметить, что м/Л отношение лимфоидной опухоли -типа соответствует λ-типу. Это противоречие произошло за счет относительного уве- личения СЛЦ-λ при преимущественной супрессии опухолевой СЛЦ-м. В целом здесь можно говорить о полном совпадении клинической динамики, клеточных и гуморальных оценочных критериев.
В исследовании №5 (таблица 7) зафиксирован частичный ответ после проведенной программы лечения FCR+R+RB. Важно отметить, что это сопровождалось достижением НМОБ (0,007%). Это означает, что НМОБ не идентифицирует опухолевые клетки, которые находятся вне циркуляции. В тоже время, анализ СЛЦ показал, что концентрация опухолевой СЛЦ-м была значительно повышена, а м/Л отношение было больше нормальных средних значений и приближалась к верхней границе нормы. Полученные результаты свидетельствуют о том, что метод Free Light assay более чувствительный, чем определение НМОБ и может оценивать наличие опухолевых клеток in situ.
В исследовании №6 (таблица 7) достигнута полная ремиссия после проведения программы FCR и поддерживающего лечения ритуксимабом. Клинический результат соответствовал результату МОБ (1%). Анализ СЛЦ показал супрессию концентраций м и опухолевой Л СЛЦ, при снижении м/Л отношения ниже средних нормальных значений, но в нормальных пределах. В этом наблюдении также можно отметить совпадение клинических результатов с данными МОБ и СЛЦ.
В исследовании №7 (таблица 7) не было зафиксировано клинического ответа после проведения курсов ИХТ по программе BR. Это совпадало с результатами МОБ (7,6%). При анализе результатов исследования концентраций СЛЦ также отмечалась повышенная концентрация опухолевой СЛЦ Л, супрессия нормальных антителопродуцентов м и снижения м/Л отношения по Л типу (0,16). В этом исследовании получено подтверждение клинической оценки лечения по результатам изучения МОБ и СЛЦ.
В исследовании №8 (таблица 7) проанализированы клинические результаты после лечения по программе FCR+R. Достигнут частичный ответ, что подтверждается данными МОБ (0,02%). По экспрессии мембранных ЛЦ установлен λ-тип опухоли. Анализ концентрации СЛЦ показал верхние границы нормальных концентраций м и Л СЛЦ при нормальном м/Л отношении (0,82). В этом наблюдении клинические и лабораторные критерии (МОБ и СЛЦ) оценки лечения полностью совпали, хотя они ближе к ПО.
В исследовании №9 (таблица 7) получен частичный ответ после проведения программы BR. При этом достигнута МОБ (0,02%). Анализ концентраций СЛЦ показал увеличение -СЛЦ выше средних значений нормы и снижение Х- цепи, х/Х отношение было на верхних границах нормы. Это может свидетельствовать о существовании остаточной нодальной опухоли -типа и супрессии неопухолевых λ продуцентов. В данном наблюдении СЛЦ метод был более чувствительным, чем НМОБ.
В исследовании №10 (таблица 7) достигнут полный ответ после лечения ибрутинибом. При этом МОБ составляла 0,56%, а концентрация СЛЦ и х/Х отношения были в пределах нормальных значений. В данном наблюдении имеет место совпа- дение клинических и лабораторных результатов (МОБ, СЛЦ) в оценке эффективности проведенного противоопухолевого лечения. В исследованиях №11 и 12 (таблица 7) концентрация СЛЦ была изучена у впервые выявленных больных ХЛЛ IIст. В обоих случаях отмечены клональные изменения х/Х отношений х (3,4) и X (0,04) типов. Эти данные были подтверждены ИФТ опухолевых лимфоцитов х или Х. По результатам данного исследования следует отметить, что наряду с увеличением концентрации опухолевых СЛЦ установлено снижение СЛЦ, не вовлеченных в опухолевых процесс.
Анализ СЛЦ до и после проведения противорецидивной программы BR+ибрутиниб у 2 больных с СЛЦ-х фенотипом ХЛЛ представлен в таблица 8.
Таблица 8
Эффективность BR + ибрутиниб терапии у 2 больных с прогрессией СЛЦ- х ХЛЛ.
|
N исследования |
ИХТ |
х |
λ |
х /Х |
Интервал |
Лечение* |
Статус |
|
до |
33 мг/л |
9,51 мг/л |
3,47 |
10 мес. |
BR+ибр. |
ПО** |
|
|
1 |
после |
11,7 мг/л |
13,9 мг/л |
0,84 |
|||
|
2 |
до |
15,3 мг/л |
9,83 мг/л |
1,56 |
8 мес. |
BR+ибр. |
ПО |
|
после |
7,34 мг/л |
10,07 мг/л |
0,68 |
*BR- бендамустин, ритуксимаб, ибрутиниб; **ПО- полный ответ
Как видно из таблицы 8 через 8-10 месяцев лечения концентрация СЛЦ-х снизилась на 64,5% и немного превышала норму в одном наблюдении. В другом наблюдении снижение СЛЦ было на 52% вплоть до нормальных значений. Важно отметить, что концентрация нормальных антитело-продуцентов повысилась практически до нормы (на 31,5% и 2,4%). Это свидетельствовало о высокой избирательности BR+ибрутиниб программы, которая снимала супрессивный эффект с нормальных антителопродуцентов, осуществляемый опухолевыми клетками. При этом х/Х отношение оставалось немного повышенным (0,84) в первом и нормализовалось во 2 наблюдении. Сравнивая полученные результаты у двух больных, достигших ПО, можно сказать, что в первом наблюдении определялась остаточная опухоль in situ.
Обобщая результаты, представленные в таблице 7, можно обратить внимание на взаимосвязь между категорией клинического ответа на лечение, характеристикой МОБ (НМОБ), концентрацией СЛЦ, х/Х отношением и мембранными ЛЦ на опухолевых лимфоцитах крови. Установлено, что в трех наблюдениях при констатации полного или частичного ответов на лечение (МОБ от 0,02 до 0,007) были отчетливые признаки наличия СЛЦ опухолевого клона, клетки которого практически не определялись в циркуляции, а продуци- ровали СЛЦ in situ. По существу, речь идет о визуализации нодального пула опухоли (№2; 5 и 9).
В исследованиях №8 и 10 можно условно говорить о совпадении результатов МОБ (0,02 и 0,56%) и концентрации СЛЦ и х/Х отношения, колебания которых не выходили за пределы нормальных значений. Однако концентрации опухолевых СЛЦ превышали средние значения нормы, а их принадлежность к опухолевому клону подтверждалась идентичным изотипом СЛЦ на мембране опухолевых лимфоцитов.
В исследованиях №3, 4 и 6 концентрации СЛЦ совпадали с категорией клинического ответа и минимальными значениями циркулирующих опухолевых лимфоцитов (МОБ и НМОБ). В этих наблюдениях следует отметить цитостатическую супрессию опухолевых и неопухолевых СЛЦ. Причем в 2 случаях (№3 и 4) это привело к искажению х/Х отношения. Установлен Х-тип клональности (0—>15 и 0—>21) при х-типе мембранных СЛЦ.
В исследованиях №1 и 7 не было клинического результата после проведенных ИХТ программ, хотя опухолевые лимфоциты в циркуляции были значительно снижены и составляли от исходных значений 2 и 7,6%, соответственно. Анализ показал, что концентрации опухолевых СЛЦ и х/Х отношения свидетельствовали об опухолевом типе изменений. В этих наблюдениях можно говорить о совпадении полученных результатов. Рассматривая метод СЛЦ с позиций новых оценочных критериев эффективности ХТ при ХЛЛ, следует отметить, что в нашей исследовательской модели совпадение с клиническим статусом и МОБ (НМОБ) достигнуто в 7 из 10 наблюдений. В трех наблюдениях при НМОБ от 0,02 до 0,007 (%) от исходных значений изменения СЛЦ носили опухолевый характер, что свидетельствовало о наличии остаточной опухоли in situ. Следовательно, метод СЛЦ в оценке остаточной болезни после ИХТ ХЛЛ был на 30% чувствительнее, чем имму-нофенотипическое определение МОБ.
Выводы. Таким образом, в представленном исследовании приведены результаты анализа СЛЦ иммуноглобулинов сыворотки крови у 50 больных ХЛЛ, проведен анализ концентрации СЛЦ в зависимости от проводимой ХИТ (FCR; R; BR; ибрутиниб). При этом сравнивали показатели и и Л СЛЦ в группе без лечения с группами, где все получали лечение. Кроме этого анализа была проведена динамическая оценка концентрации СЛЦ до и после завершения курсов ИХТ в сравнении с результатами стандартной клинической оценки. Важным этапом этой работы был сравнительный анализ МОБ, включая НМОБ и концентрации опухолевой СЛЦ после проведенного противоопухолевого лечения. Следует от- метить, что проведенные исследования можно расценивать как иммунологический мониторинг (МОБ и СЛЦ) эффективности ХИТ. Одним из важных итогов работы следует считать установление частоты встречаемости СЛЦ патологии при ХЛЛ. Было установлено, что моноклональный характер изменений СЛЦ (повышение концентрации одной из СЛЦ и измененное и/Л отношение) был у 32 больных (64%) и без СЛЦ патологии был у 18 больных (36%). На наш взгляд это важное положение, позволяющее использовать СЛЦ в качестве дополнительного иммунологического мониторинга ИХТ ХЛЛ.
Конфликты интересов отсутствует
Источник финансирования
Исследование не имело источника финансирования
Вклад авторов
Концепция и дизайн: все авторы
Сбор и обработка данных: все авторы
Предоставление материалов исследования: все авторы
Анализ и интерпретация: все авторы Подготовка рукописи: все авторы Окончательное одобрение рукописи: все авторы
Список литературы Анализ свободных легких цепей иммуноглобулинов сыворотки крови у больных хроническим лимфолейкозом в процессе химиоиммунотерапии
- Hallek M., Fisher K., Fingerle–Rowson Y. et al. Addition of rituximab to fludarabine and cyclophosphamide in patients with chronic lymphocytic leukaemia: a randomised, open–label, phase 3 trial // Lancet. – 2010. – Vol. 376, N2. – P. 1164–1174.
- Betteher S., Ritgen M., Fischer K. et al. Minimal residual disease quantification is an indepentend predictor of progression free and overall survival in chronic lymphocytic Leukemia. A multivariate analysis from the randomized GCLLSG CLL 8 trial // J Clin Oncol. – 2012. – Vol. 30, N9.– P. 980–988.
- Rawstron A., Fazi C., Agathagelidis A. et al. A Commplementary role of multiparameter flow cytometry and high–throughput sequencing for minimal residual direction in chronic lymphocytic Leukemiа: an European Researoh initiative on CLL study // Leukemiа. – 2016. – Vol. 30, N4. – P. 929–936.
- Rowstron A., Cohen D., de Tute R. et al. Bone marrow is more sensitive than peripheral blood for detection of MDR in CLL and provides a more reliable prediction of ancome across different treatments // Haematologica. – 2015. – Vol. 100, (Suppl 1).–Abstract S794
- Голенков А.К., Митина Т.А., Новиков В.В., Тагиров О.Т. и др. Клиническое значение растворимых молекул адгезии (sCD50 – ICAM – 3), апоптоза (sCD95) и sHLA класса – I при лимфопролиферативных заболевания // Российский Биотерапевтический журнал. – 2002. – № 1. – С. 60-64
- Митина Т.А. Клиническое значение линейного и адгезивного фенотипов опухолевых клеток при хроническом лимфолейкозе // Дисс. канд. М. – 2003. 27 с.
- Катаева Е.В., Голенков А.К., Митина Т.А., Клинушкина Е.Ф. и др. Клинические аспекты определения свободных легких цепей иммуноглобулинов сыворотки крови у больных хроническим лимфолейкозом // Гематология и трансфузиология. – 2017. – Т. 62, № 3. – С. 153-157.
- Martin W., Abraham R., Shanafelt T., Clark R. et al. Serum free light chain – a new biomarker for patients with B-cell non-Hodgkin lymphoma and chronic lymphocytic leukemia // Translational Research. – 2007. – Vol. 149, № 4. – Р. 231-235.
- Бессмельцев С.С. Современные методы диагностики и лечения больных хроническим лимфолейкозом. // Вестник гематологии. – 2011. – №1.– С. 137-156
- Савченко В.Г. Алгоритмы диагностики и протоколы лечения заболеваний системы крови. 2018, том 2, с.323-361.
- Hallek M., Cheson B.D., Catovsky D., Calligaris-Cappio F. et al. International workshop on chronic lymphocytic leukemia. Guidelines for the diagnosis and treatment of chronic lymphocytic leukemia: a report from the international workshop on chronic lympocytic leukemia updating the National Cancer Institute- working group 1996 guidelines // Blood. – 2008. – Vol. 111, № 12. – Р. 5446-56
- Rawstron A.C. International standartized approach for flow cytometrics residual disease monitoring in chronic lymphocytic leukemia // Leukemia: – 2007. – Vol. 21, № 5. – Р. 956-964.


