Бластная плазмоцитоидная дендритно-клеточная неоплазия - диагностика и результаты первого и второго этапа лечения(клиническое наблюдение)
Автор: Черноусов И.М., Клеина И.В., Новосельцева Л.Г., Филиппович Т.В., Смирнов Р.Н., Алексеев С.А., Троян В.Н., Рукавицын О.А.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Клиническое наблюдение
Статья в выпуске: 1 т.19, 2023 года.
Бесплатный доступ
Бластная плазмоцитоидная дендритно-клеточная неоплазия - редкое заболевание, исходящее из плазмоцитоидных дендритных клеток. Приведены данные, характеризующие процесс диагностики и лечения пациента, наблюдаемого с установленным диагнозом с февраля 2022 года. На первом этапе лечение оказалось успешным. В дальнейшем у пациента развилась нейролейкемия, курсы противоопухолевой химиотерапии были неэффективны. Проводилась лучевая терапия на весь объем головного мозга. Сделан акцент на необходимости накопления информации о редкой гематологической патологии. Это должно привести к формированию стандартных подходов к терапии редкого заболевания.
Бластная плазмоцитоидная дендритно-клеточная неоплазия, диагностика, лечение, нейролейкемия
Короткий адрес: https://sciup.org/170198329
IDR: 170198329
Blastic plasmacytoid dendritic cell neoplasia - diagnosis and results of the first and second stages of treatment (clinical observation)
Blastic plasmacytoid dendritic cell neoplasia is a rare disease originating from plasmacytoid dendritic cells. The data characterizing the process of diagnosis and treatment of a patient observed with an established diagnosis since February 2022 are presented. At the first stage, the treatment was successful. Subsequently, the patient developed neuroleukemia, courses of antitumor chemotherapy were ineffective. Radiation therapy was carried out on the entire volume of the brain. Emphasis is placed on the need to accumulate information about rare hematological pathology. This should lead to the formation of standard approaches to the treatment of a rare disease.
Текст научной статьи Бластная плазмоцитоидная дендритно-клеточная неоплазия - диагностика и результаты первого и второго этапа лечения(клиническое наблюдение)
Бластная плазмоцитоидная дендритно-клеточная неоплазия (БПДКН) – редкая гематологическая злокачественная опухоль. Она может характеризоваться поражениями кожи и агрессивным клиническим течением, с быстрым поражением костного мозга и лимфатических узлов. Пациентов с БПДКН принято разделять на группы с кожными поражениями и без них, однако клиническое значение такого разделения не вполне ясно: данных о том, что лечение разнится и прогноз неодинаков, пока нет [1]. Обычно БПДКН характеризуется плохим прогнозом и низкими показателями выживаемости. Опухоль исходит из плазмоцитоидных дендритных клеток; детальный патогенез ее неясен. Опухолевые клетки характеризуются аберрантной экспрессией CD4, CD56, альфа-цепи рецептора интерлейкина 3 (CD123), антигенов дендритных клеток крови 2 (BCDA2/ CD303) и 4 (BCDA4), а также транскрипционного фактора (TCF4) [2]. В зависимости от типа экспрессии делаются попытки разделить пациентов с БПДКН на подгруппы (с экспрессией CD123, CD303 и т.д.), но целесообразность этого разделения неочевидна [3]. Лечение БПДКН не разработано, но обычно основано на препаратах, применяемых для терапии лейкозов и лимфом [4]. Рецидивы заболевания и резистентность к проводимому лечению встречаются часто. Трансплантация аллогенных гемопоэтических стволовых клеток может быть выполнена в полной ремиссии заболевания [5].
Цитогенетические исследования выявляют разнообразные и множественные хромосомные аберрации, нередко в составе комплексного кариотипа; возможно развитие нескольких клонов, либо клонов с субклонами. Ввиду редкости заболевания клиническое и прогностическое значение цитогенетических находок неопределенно [6,7].
Клиническое наблюдение. Пациент Г., мужчина 66 лет без выраженной коморбидности. Анамнез заболевания: считает себя больным с января 2022 г., когда впервые отметил появление одышки, общей слабости, периодических носовых кровотечений. 26.01.22 обратился к терапевту по месту жительства, назначена противовирусная терапия. С 04.02.22 отметил увеличение шейных лимфатических узлов, к терапии добавлены антибактериальные препараты. По данным компьютерной томографии органов грудной клетки (КТ ОГК) данных за поражение легочной ткани не выявлено. Госпитализирован в стационар для обследования. Выполнена стернальная пункция. Диагностирован острый лейкоз (мие-лограмма от 16.02.22: бластные клетки – 95%). Для дальнейшего обследования и лечения переведен в гематологический стационар.
При поступлении жалобы на общую слабость, учащенное сердцебиение, головокружение, одышку в покое и при незначительной физической нагрузке, повышение температуры тела до субфебрильных цифр, периодические носовые кровотечения, увеличение периферических лимфоузлов. Гемограмма 18.02.22: лейкоциты – 192,48х109/л, гемоглобин – 6,9 г/дл, тромбоциты – 38х109/л, бластные клетки – 91 %. Миелограмма 18.02.22: костный мозг гиперклеточный. Бластные клетки составляют 93,2 % (рис.1 а) и б)).
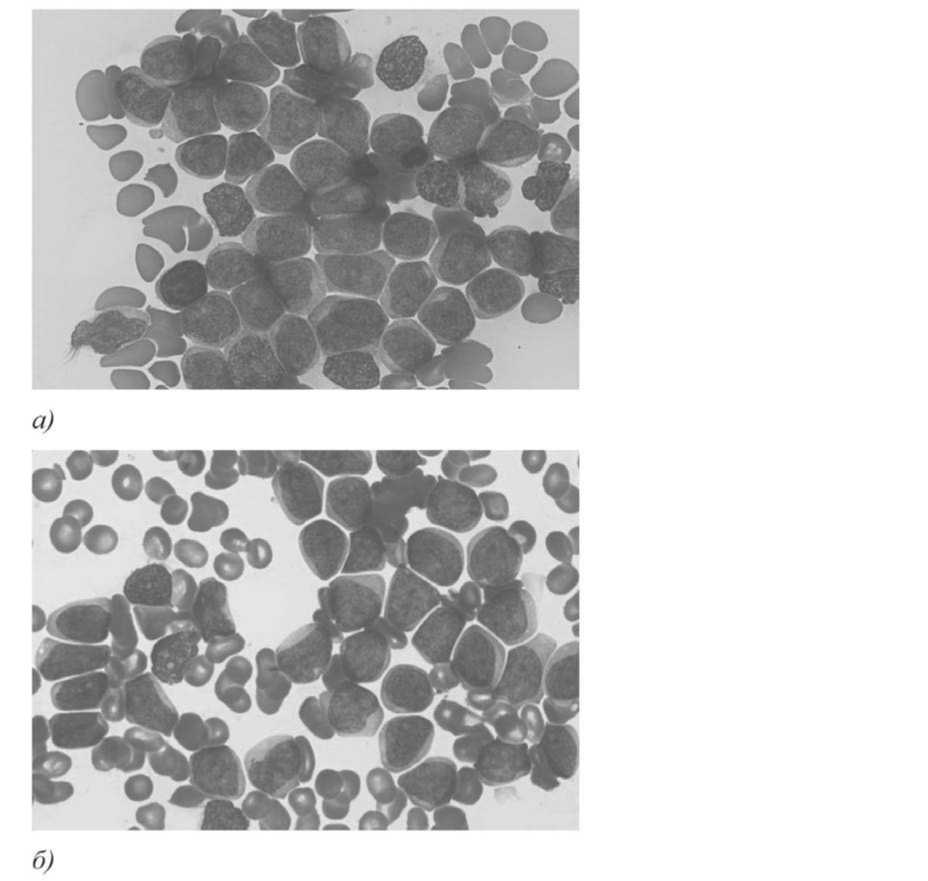
Рис .1. Препарат костного мозга : метаплазия бластными клетками
Они представлены мономорфно клетками небольшого размера с умеренным ядерно-цитоплаз-матическим соотношением, ядра округлые, видны 1-2 нуклеолы, цитоплазма умеренно базофильная, не содержит включений. Цитохимические реакции на пероксидазу, липиды и неспецифическую эстеразу отрицательные, гликоген в части клеток в слабодиффузной и диффузно-гранулярной формах. Иммунофенотип: бластные клетки CD45low экспрессируют антигены CD123, CD56, CD7, CD33, CD117low; экспрессия cyCD3 слабее, чем на лимфоцитах CD45++, что не позволяет диагностировать Т-ОЛЛ. Полученные данные более соответствуют бластной плазмоцитоидной дендритно-клеточ- ной опухоли. Цитогенетическое исследование клеток костного мозга от 18.02.22 г: кариотип – 45,ХY, add(1)(p36), del(3)(p25), der(8), der(9), del(12)(p13), add(12)(p11) или t(3;12)(p25;p11), -13, der(17) (рис. 2).
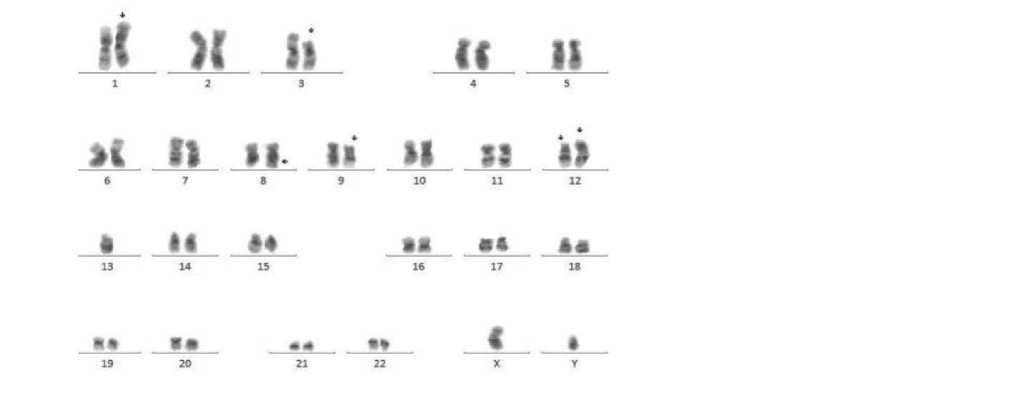
Рис .2. Результат стандартного цитогенетического исследования : Кариотип : 45, Х Y, add(1) (p36), del(3)(p25), der(8), der(9), del(12)(p13), add(12)(p11) or t(3;12)(p25;p11), -13, der(17)
В результате проведенных исследований (методом стандартного цитогенетического исследования и FISH) выявлены клон и субклон. Клон с деле-цией локуса гена ETV6/12р13 и делецией региона 13q14; субклон с комплексными изменениями кариотипа: дериватами хромосом 1, 8, 9, 12, 17, деле-цией короткого плеча хромосомы 3, биаллельной делецией локуса гена ETV6/12р13, делецией локуса гена ABL/9q34; моносомией по хромосоме 13.
Заключение: опухоль из бластных плазмоци-тоидно-дендритных клеток. С 18.02.22 начата 1-я фаза индукции по программе «ОЛЛ-2009» (преднизолон 60 мг/сутки внутрь 1-19 дни, даунорубицин 60 мг в/в в 8-й день, винкристин 2,0 мг в/в в 8-й день) на фоне аллопуринола, стандартной инфузионной, антиэметической и гемозаместительной терапии. На 10-й день курса выполнена контрольная стернальная пункция, в миелограмме от 28.02.22 бластные клетки – 11,8 %. Терапию перенес без осложнений. Проводилась антибактериальная (це-фепим), противогрибковая (флуконазол), гемостатическая (этамзилат, транексам), заместительная гемотрансфузионная (19 л.д. тромбоконцентрата, 10 доз эритроцитной массы). Лечение продолжено. В рамках протокола «ОЛЛ-2009» (I фаза индукции) выполнены введения химиопрепаратов (винкри-стин 2,0 мг в/в струйно 15-й и 21-й дни, даунору-бицин 90 мг в/в капельно 15-й и 21-й дни) на фоне аллопуринола, стандартной инфузионной, антиэ-метической и гемозаместительной (5 доз СЗП, 1 л.д. тромбоконцентрата) терапии. Пациент в удовлетворительном состоянии выписан на амбулаторное долечивание под наблюдение гематолога по месту жительства до следующего введения химиопрепаратов. Через 2 месяца от начала лечения констати- рована полная ремиссия заболевания.
В дальнейшем лечение по протоколу было продолжено. В рамках протокола «ОЛЛ-2009» (индукция II) выполнены введения химиопрепаратов (ци-клофосфан 1800 мг в/в струйно 43-й день, цитозар 100 мг в/в капельно 45-48-й дни, аспарагиназа 10 тыс Ед в/в капельно 50-й и 57-й дни, меркаптопурин 50 мг внутрь 43-57-й дни) на фоне аллопуринола, стандартной инфузионной, антиэметической и гемозаместительной (2 дозы СЗП) терапии. В рамках протокола «ОЛЛ-2009» с 10.05.22 по 17.05.22 (индукция II) выполнены введения химиопрепаратов (цитозар 100 мг в/в капельно 59-62-й дни, аспарагиназа 10 тыс. Ед в/в капельно 64-й день, меркаптопурин 50 мг внутрь 59-65-й дни) на фоне аллопуринола, стандартной инфузионной терапии. Пациент в удовлетворительном состоянии был выписан на амбулаторное долечивание под наблюдение гематолога по месту жительства до следующего введения химиопрепаратов.
При поступлении в мае 2022 г. жалобы на головокружение, головные боли, неустойчивость при ходьбе. В миелограмме 26.05.2022: костномозговой пунктат скудной клеточности, полиморфный, бластов 1,2 %. Сохраняется костномозговая ремиссия. FISH-исследование на суспензии клеток спинномозговой жидкости 27.05.2022: в 94 % ядер отсутствует один сигнал от локуса гена ETV6(12p13), делеция короткого плеча хромосомы 12. FISH-исследование на суспензии клеток костного мозга 30.05.2022: транслокация t(12;21)(р13;q11), деле-ция короткого плеча хромосомы 12 не выявлены. Цитохимическое исследование костного мозга 31.05.2022: сидеробласты ниже нормы, кольцевидные сидеробласты не обнаружены. Положительные реакции на миелопероксидазу и гликоген в клетках эритроидного ряда указывают на цитохимические признаки дисэритропоэза. При контрольной люмбальной пункции выявлены признаки нейролейкемии. Выполнено 9 люмбальных пункций с целью санации ликвора с положительной динамикой (1-ая пункция 26.05.22: цитоз 11200 кл/3мкл, бластных клеток 100%, лейкоциты – 70-80 в поле зрения (п/зр; 9-я пункция 23.06.22: цитоз 17/3 кл/3мкл, бластных клеток – 1 клетка, лейкоциты – единичные, лимфоциты – 12 клеток, макрофаги – 2 клетки, моноциты – 1 клетка, нейтрофилы – 1). С 08.06.22 по 21.06.22 проведена консолидация I в рамках протокола «ОЛЛ-2009» (дексаметазон 12 мг 1 р/сут. в/в капельно 14 дней, винкристин 2 мг 1 раз/сут. в/в струйно в 1-й день, 14-й день, доксорубицин 50 мг в/в капельно 1 раз/сут. в 1-й и 14-й дни). Пациент в удовлетворительном состоянии был выписан на амбулаторное долечивание под наблюдение гематолога по месту жительства до следующего введения химиопрепаратов.
При поступлении в июле 2022 г. жалобы на общую слабость, головные боли при перемене положения тела. В миелограмме 08.07.2022: костномозговой пунктат скудной клеточности, полиморфный, бластов – 1,6 %. FISH-исследование на суспензии клеток костного мозга 08.07.2022: в 4 % ядер выявлена делеция короткого плеча хромосомы 12. При контрольной люмбальной пункции констатирован нейролейкоз, ликвор санирован. Выполнено 5 люмбальных пункций с целью санации ликвора с положительной динамикой (1-ая пункция 08.07.22 г.: цитоз 42/3, бластных клеток 17%, лейкоциты – 1-1-2 в п/зр., белок-2,35 г/л; 5-я пункция 20.07.22: цитоз 6/3 клеток, бластных клеток – отр., лейкоциты – единич., лимфоциты – 4 кл., макрофаги – 1кл., нейтрофилы – 1 кл.). Проведена консолидация II в рамках протокола «ОЛЛ-2009» без осложнений. Состояние больного улучшилось.
Госпитализация в августе 2022 г. При поступлении жалобы на общую слабость, головные боли при перемене положения тела. Выполнена люмбальная пункция с интратекальным введение препаратов, ликвор в норме (бесцветный, цитоз 8/3, нейтрофилы – 6, лимфоциты – 2). В миелограмме 08.08.2022: костномозговой пунктат гипоклеточный, полиморфный, бластов – 1,0 %. FISH-исследование на суспензии клеток костного мозга 08.08.2022г.: де-леция короткого плеча хромосомы 12 не выявлена. В рамках протокола «ОЛЛ-2009» (консолидация III) введены: циклофосфан 1400 мг, цитозар 150 мг в/в капельно 1-4-й дни, принимал 6-меркаптопурин. В удовлетворительном состоянии выписан на перерыв в химиотерапии под наблюдение гематолога по месту жительства. При поступлении в сентябре 2022 г. жалобы на общую слабость, головные боли при перемене положения тела. Ликвор от 05.09.22: бесцветный, цитоз 2816/3, бластные клетки 100
%, ликвор от 14.09.22 г.: бесцветный, прозрачный, цитоз-5/3, бластные клетки – 60 %. Пациенту выполнены 5 люмбальных пункций с интратекаль-ным введением препаратов без эффекта. В связи с чем после завершения консолидации III в рамках протокола «ОЛЛ-2009» было показано проведение дистанционной лучевой терапии на весь объем головного мозга (СОД 25 Гр). Лучевая терапия выполнена в полном объеме. С заместительной целью перелито: тромбоконцентрата 5 л.д., эритроцитной массы 1 доза.
При поступлении в октябре 2022 г. жалобы на общую слабость, головные боли. В миелограм-ме 18.10.2022: костномозговой пунктат нормоклеточный, полиморфный, бластов 3,6 %. FISH-исследование на суспензии клеток костного мозга 18.10.2022: в 1,2 % ядер выявлена делеция короткого плеча хромосомы 12. Пациенту выполнено 4 люмбальных пункции с интратекальным введением препаратов (ликвор от 19.10.22: бесцветный, ци-тоз 18/3, бластные клетки 80 %, ликвор от 31.10.22 г.: бесцветный, прозрачный, цитоз 1/3, нейтрофилы – 1 клетка). Нейролейкоз сохранялся. В рамках протокола «ОЛЛ-2009» (консолидация V) введены цитозар 4 г в/в кап 25.10.22, аспарагиназа 10 тыс Ед в/в капельно 27.10.22, дексаметазон 40 мг в/в кап 25.10-27.10.2022. В удовлетворительном состоянии выписан на перерыв в химиотерапии под наблюдение гематолога по месту жительства.
На основании имеющихся данных сформулирован диагноз: Основное заболевание: Бластная плазмоцитоидная дендритно-клеточная неоплазия от 02.2022. Гиперлейкоцитоз. Индукционная терапия: «ОЛЛ-2009». Ремиссия от 05.04.22. Изолированный внекостномозговой (ЦНС) рецидив I (май 2022 г.). Санация ликвора (07.22 г.). Изолированный внекостномозговой (ЦНС) рецидив II (сентябрь 2022 г.). Дистанционная лучевая терапия на весь объем головного мозга (СОД=25 Гр). Осложнения основного заболевания: Постцитостатическая панцитопения. Анемия 2 ст. Тромбоцитопения 3 ст. Сопутствующие заболевания: ИБС. Диффузный кардиосклероз. Желудочковая экстрасистолия. Гипертоническая болезнь 2 стадии (медикаментозная нормотензия, риск ССО 4). ХСН I ст. ФК – 2 (NYHA).
Заключение
В качестве резюме можно констатировать, что мы наблюдаем пациента с редким заболеванием, имеющим клинико-гематологическую картину, идентичную острой лейкемии. Обусловлен и выбор программы лечения, применяющейся при остром лимфобластном лейкозе. Можно констатировать успех первого этапа лечения, быстрое достижение полной клинико-гематологической ремиссии. Однако, она была короткой. Возник рецидив заболевания в виде нейролейкемии, которая затем рецидивировала повторно. Неэффективность кур- сов противоопухолевой химиотерапии привела к проведению дистанционной лучевой терапии на весь объем головного мозга. Проводится дальнейшее лечение пациента. Накопление информации об этой редкой нозологической форме может привести к формированию стандартных терапевтических подходов и к улучшению результатов лечения пациентов.
Список литературы Бластная плазмоцитоидная дендритно-клеточная неоплазия - диагностика и результаты первого и второго этапа лечения(клиническое наблюдение)
- Suzuki Y., Kato S., Kohno K. et al. Clinicopathological analysis of 46 cases with CD4 + and/or CD56 + immature haematolymphoid malignancy: reappraisal of blastic plasmacytoid dendritic cell and related neoplasms // Histopathology. - 2017. - Vol. 71, No. 6. - Р. 972-984.
- Riaz W., Zhang L., Horna P. et al. Blastic plasmacytoid dendritic cell neo-plasm: update on molecular biology, diagnosis, and therapy // Cancer Control. - 2014. - Vol. 21, No. 4. - P. 279-289.
- Rauh M.J., Rahman F., Good D. et al. Blastic plasmacytoid J dendritic cell neo-plasm with leukemic presentation, lacking cutaneous involvement: case series and literature review // Leuk Res. - 2012. - Vol. 36, No.1. - P. 81-86.
- Cheng W., Yu T., Tang A.-P. et al. Blastic Plasmacytoid Dendritic Cell Neoplasm: Progress in Cell Origin, Molecular Biology, Diagnostic Criteria and Therapeutic Approaches // Curr Med Sci. - 2021. - Vol. 41, No. 3. - P. 405-419.
- Kharfan-Dabaja M.A., Lazarus H.M., Nishihori T. et al. Diagnostic and therapeutic advances in blastic plasmacytoid dendritic cell neoplasm: a focus on hematopoietic cell transplantation // Biol Blood Marrow Transplant. - 2013. - Vol. 19, No. 7. - P. 1006-1012.
- Kopeczi J., Benedek E., Kakucs E.et al. Blastic plazmacytoid dendritic cell neoplasia - a rare type of acute leukemia// Revista Romana de Medicina de Laborator. - 2014. - Vol. 22, No.1. - P. 69-77.
- Валиев Т.Т., Серегин Г.З., Серебрякова И.Н. и др. Опухоль из бластных плазмоцитоидных дендритических клеток // Вопросы гематологии/онкологии и иммунопатологии в педиатрии. - 2019. - Т. 18, № 4. - С.79-89.


