Физиологические особенности роста и развития поросят разных генотипов по генам FUT1 и MUC4
Автор: Закирова А.В., Ткачев А.В., Нотина Е.А., Быкова И.А., Ткачева О.Л.
Рубрика: Зоотехния
Статья в выпуске: 4 т.264, 2025 года.
Бесплатный доступ
ДНК-технологии дают возможность реализовать принципиально новые подходы в селекции животных. Прежде всего это генетическая идентификация конкретных особей с последующим генетико-популяционным анализом, обеспечивающим получение количественных характеристик генофондов исследуемых популяций. Целью исследования было установить физиологические особенности роста и развития поросят разных генотипов по генам FUT1 и MUC4 при добавлении витаминной подкормки. Исследования выполняли с 2023 по 2024 гг. В работе использовали 88 поросят крупной белой породы в период от рождения до отъёма. Животные были разделены на 6 групп. Поросята в каждой группе взвешивались в первый день жизни, на 3 сутки, и затем через каждые 3 суток до возраста 21 день. Наибольшая живая масса была у поросят с генотипом АА/GG (FUT1/MUС4), потом следовали особи с генотипом АG/GС (FUT1/MUС4) кроме третьей группы, и наименьшая живая масса была у поросят с генотипом GG/СС (FUT1/ MUС4). В третьей группе животных максимальная живая масса была более 5860 г у генотипа АА/GG (FUT1/MUС4), что на 352,1 г больше (р<0,05) от генотипа GG/СС (FUT1/MUС4) и на 676,6 г больше (р<0,001) генотипа АG/GС (FUT1/MUС4). В четвертой группе поросят максимальная живая масса была более 5710 г у генотипа АА/GG (FUT1/MUС4), что на 681,53 г больше (р<0,05) от генотипа GG/СС (FUT1/MUС4) и на 153 г больше генотипа АG/GС (FUT1/MUС4). Таким образом, полученные результаты указывают на то, что генотипирование поросят по генам FUT1 и MUС4 может быть использовано не только для определения устойчивости к кишечным инфекциям, но и для прогнозирования физиологических особенностей роста и развития на ранних стадиях онтогенеза.
Полиморфизм генов, кормление, подсосный период, FUT1, MUC4
Короткий адрес: https://sciup.org/142246750
IDR: 142246750 | УДК: 619:636.4.033:575.22 | DOI: 10.31588/2413_4201_1883_4_264_90
Physiological characteristics of growth and development of piglets of different genotypes for FUT1 and MUC4 genes
DNA technologies make it possible to implement fundamentally new approaches in animal breeding. First of all, this is the genetic identification of specific individuals with subsequent genetic-population analysis, which provides quantitative characteristics of gene pools of the studied populations. The aim of the study was to establish the physiological characteristics of growth and development of piglets of different genotypes for FUT1 and MUC4 genes with the addition of vitamin supplements. The study was carried out from 2023 to 2024. The work involved 88 piglets of large white breed from birth to weaning. The animals were divided into 6 groups. The piglets in each group were weighed on the first day of life, on the 3rd day, and then every 3 days until the age of 21 days. The highest live weight was in piglets with AA/GG (FUT1/MUC4) genotype, followed by individuals with AG/GC (FUT1/MUC4) genotype except for the third group, and the lowest live weight was in piglets with GG/CC (FUT1/ MUC4) genotype. In the third group of animals, the maximum live weight was more than 5860 g in AA/GG (FUT1/ MUC4) genotype, which is 352.1 g more (p<0.05) than GG/CC (FUT1/MUC4) genotype and 676.6 g more (p<0.001) than AG/GC (FUT1/MUC4) genotype. In the fourth group of piglets, the maximum live weight was more than 5710 g for AA/GG (FUT1/MUC4) genotype, which is 681.53 g more (p<0.05) than GG/CC (FUT1/MUC4) genotype and 153 g more than AG/GC (FUT1/MUC4) genotype. Thus, the obtained results indicate that genotyping of piglets for FUT1 and MUC4 genes can be used not only to determine resistance to intestinal infections, but also to predict the physiological characteristics of growth and development in the early stages of ontogenesis.
Текст научной статьи Физиологические особенности роста и развития поросят разных генотипов по генам FUT1 и MUC4
Исследование животных по генам количественных признаков (Quantitative Trait Loci) дает возможность предсказывать хозяйственную ценность животного на уровне ДНК в раннем возрасте и даже еще до его рождения. В связи с этим крайне интересно изучить особенности роста и развития поросят при выпаивании только молозивом от родных свиноматок; выпаивании молозивом и молоком родной свиноматки в течение 21 дня на фоне внутримышечных инъекций (в срединную треть шеи) витаминного раствора «Элеовит»; и при вскармливании поросят мачехой. Высокая конечная живая масса поросят не всегда сопровождается высокой интенсивностью роста, что и может зависеть не только от генотипа, но и от технологических условий выращивания, что и требует дополнительного изучения [3, 4].
Изучение поголовья поросят по хозяйственно-полезным признакам всегда будет актуальным и важным для практического свиноводства, так как позволяет лучше понять механизмы взаимоотношений генотип-среда и предложить новые технологические подходы в выращивании животных [5, 6].
Изучение особенностей генотипа поросят по гену альфа-(1,2)-фукозилтрансферазы-1 (FUT1) может иметь значение не только для установления устойчивости к болезням [7], но и возможно связано с интенсивностью роста и развития в подсосный период.
Доказанная связь аллелей поросят по гену FUT1 с устойчивостью к колибактериозу позволила разработать различные методики экс-пресс-диагностики прогнозирования устойчивости поросят к инфекции. Практическое применение новых методик экспресс-диагностики может помочь вовремя элиминировать из стада животных склонных к болезням, а значит эти особи могут обладать меньшей энергией роста и развития, что и требует дополнительного изучения [8].
Энтеротоксические E. coli , образующие фимбрии F4 (K88) чаще всего являются теми бактериями, которые вызывают диарею и смерть новорожденных и отлученных поросят. Е. coli с адгезивным антигеном F4 вызывают в 71% случаев диарею новорожденных поросят. Известны три антигенных варианта фимбрий F4-F4ab, F4ac и F4ad. Согласно данным анализа сцепления генов F4ab/F4ac было выявлено полное соответствие их гаплотипов гаплотипа сиалогликопротеина муцина 4 (MUC4) [9, 10].
Научно доказано, что ген муцина 4 расположен в 13-й хромосоме в 41-м регионе. И некоторые авторы предположили, что единичные мутации гена муцина 4 в позиции 1849 п.н. могут быть связаны с хозяйственнополезными признаками у поросят [11].
Цель исследований - установить физиологические особенности роста и развития поросят разных генотипов по генам FUT1 и MUC4 при добавлении витаминной подкормки.
Условия, материалы и методы. Исследования выполняли с 2023 по 2024 годы в Московской области на свиноферме ООО «Чароен Покпанд Фудс» Луховицкого района и в КФХ деревни Кулаково городского округа Чехов. В работе использовали 88 поросят крупной белой породы в период от рождения до отъёма. Животные были сгруппированы в 6 групп: 1 группа – 16 голов, 2 группа – 19 голов, 3 группа – 19 голов, 4 группа – 12 голов, 5 группа – 12 голов, 6 группа – 14 голов. Поросята в каждой группе взвешивались в первый день жизни, на 3 сутки, и затем через каждые 3 суток до возраста 21 день. В первой и во второй группах поросят выпаивали только молозивом от родных свиноматок. В третьей и четвертой группах поросята выпаивались молозивом и молоком родной свиноматки в течение 21 дня на фоне внутримышечных инъекций (в срединную треть шеи) витаминного раствора «Элеовит» в объёме 0,5 мл один раз каждые семь день. В пятой и шестой группах поросята были переведены к мачехе на 3 день её лактации.
В возрасте 21 дня от каждого поросенка была взяты пробы крови и щетины для генотипирования по генам FUT1 и MUС4. После генотипирования проводился анализ особенностей роста и развития поросят в разрезе исследуемых генов в каждой группе отдельно.
Кровь для исследования отбирали из ушной вены, используя одноразовые системы для взятия крови, одноразовой иглой в объеме 2-3 мл в стерильную пробирку с антикоагулянтом (6% раствор ЭДТА в соотношении 1:19 или 4% раствор цитрата натрия в соотношении 1:9). Закрытую пробирку с кровью несколько раз встряхивали для равномерного смешивания с антикоагулянтом. На пробирки наносили соответствующие записи для дальнейшей идентификации образцов. Пробирки транспортировали в тот же день в термоконтейнерах при температуре 5±3°С в лабораторию ООО НИЦ «Черкизово». В лаборатории содержимое пробирок высушивали на стерильной марлевой ткани в течение 1 суток в поле ламинарного потока воздуха. Высушенные образцы переносили в стерильные пакеты типа "Ziplock". На пакеты наносили соответствующие записи для дальнейшей идентификации образцов.
Щетину отбирали из холки животных с помощью пинцета в стерильные пакеты типа "Zip-lock". На пакеты наносили соответствующие записи для дальнейшей идентификации образцов. Полученные образцы к моменту проведении исследований хранили в холодильнике при температуре 5±3°С. Транспортировку осуществляли в термоконтейнерах при температуре 5±3°С.
Для выделения ДНК из биопроб с помощью ионообменной смолы Chelex-100 [CAS: 68954-42-7 Chelex-100] готовят 5% рабочий раствор этого реагента. В мерной колбе объемом 100 мл вносят 5 г Chelex-100 и добавляют дистиллированной воды до объема 100 мл. В одноразовые полипропиленовые пробирки Eppendorf объемом 1,5 мл вносят 1000 мкл стерильной дистиллированной воды. К пробиркам добавляют пробы, объемом не более 200 мкл. Смесь инкубируют 15 минут при температуре 18-25°С. Пробирки центрифугируют 1 минуту на скорости 8 тысяч об/минуту. После отделения осадка осторожно удаляют надосадочную жидкость, оставляя около 20 мкл жидкости над осадком. Центрифугирование образца проводят несколько раз до полного обесцвечивания осадка. К пробиркам добавляют 180 мкл 5% стерильного водного раствора Chelex-100 и инкубируют в течение 30 минут при 56°С на термостате. Затем содержимое пробирки перемешивают и центрифугируют 1 минуту на скорости 8 тыс. об/ минуту. Для амплификации используют 5 мкл надосадочной жидкости, содержащей ДНК. Раствора выделенной ДНК достаточно для проведения 20-100 амплификаций. Хранить образцы при минус 20°С в течение 6 месяцев. После каждого размораживания образцы встряхивают и центрифугируют 5 минут на скорости 6 тысяч об/минуту (Минакова Н. Геномные технологии для животноводства / Н. Минакова // Наука и инновации. 2021. № 8 (222). С. 4-8).
Последовательность праймеров: FUT1 — F: 5/-
CCAACGCCTCCGATTCCTGT-3/,
FUT1 — R: 5/-
GTGCATGGCAGGCTGGATGA-3/.
MUC4 — F: 5/-
GTGCCTTGGGTGAGAGGTTA-3/,
MUC4 — R: 5/-
CACTCTGCCGTTCTCTTTCC-3/.
Математико-статистические расчеты результатов физиологических показателей роста и развития поросят осуществляли по критерию Стьюдента в SPSS for Windows (IBM, USA).
Результаты и обсуждение. Изучение физиологических особенностей роста и развития поросят удобнее всего охарактеризовать изучением динамики живой массы в процессе выращивания. Поэтому в первую очередь мы провели анализ динамики живой массы поросят только в разрезе групп без учета их генотипа по генам FUT1 и MUС4. Полученные результаты представлены на рисунке.
Анализ данных рисунка мы начнем с оценки интенсивности роста поросят в группах. За 21 день выращивания наиболее интенсивно росли поросята второй группы, так как их живая масса увеличилась в 4,52 раза. Затем следовала шестая группа поросят, масса которых с рождения до 21 суток увеличилась в 4,4 раза. В четвертой группе масса поросят увеличилась в 4,27 раз к завершению В третьей группе поросят их живая масса уве-периода наблюдения с момента рождения. личилась в 3,98 раза.
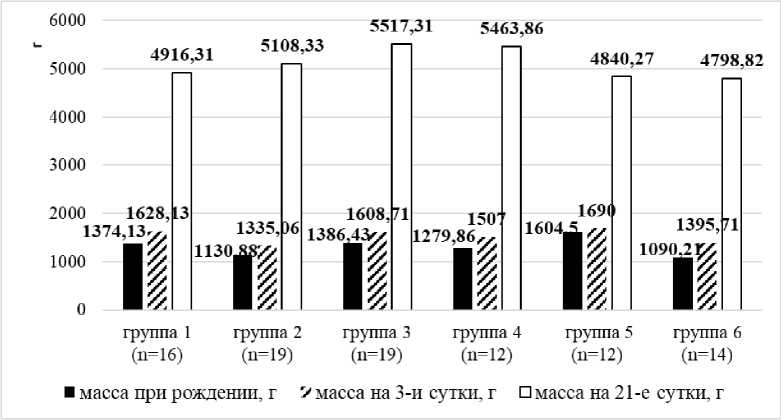
Рисунок - Динамика живой массы поросят без учета особенностей их генотипа
Средняя живая масса поросят первой группы увеличилась в 3,58 раза. Наименьшая интенсивность роста наблюдалась нами в пятой группе животных, так как их живая масса увеличилась за 21 день только в 3,02 раза. Получается, что максимальная интенсивность роста поросят в группах животных не сопровождалась максимальной живой массой в группах на момент завершения эксперимента.
Максимальная живая масса поросят на 21 сутки выращивания наблюдалась нами в третьей группе, которая занимала лишь 4 место по интенсивности роста, и составила 5517 г, что на 53,45 г больше поросят четвертой группы (3 место по интенсивности роста).
Третья группа поросят превосходила живую массу второй группы на 409 г, у которой была наилучшая интенсивности роста. Максимальная живая масса поросят третьей группы была больше шестой группы (у которой была 2-я интенсивность роста) животных на 718,5 г (р<0,05). Поросята первой и пятой групп также уступали (р<0,05) животным третьей группы по показателю максимальной живой массы на 601 и 677 г соответственно.
На следующем этапе нашего исследования изучались физиологические особенности изменений в живой массе поросят в зависимости от генотипа по генам FUT1 и MUС4 (табл.).
Таблица - Физиологические особенности живой массы поросят разных генотипов по генам FUT1 и MUС4
|
Показатель |
Группа |
|||||
|
1 |
2 |
|||||
|
Генотип по FUT1 |
GG |
AA |
AG |
GG |
AA |
AG |
|
Генотип по MUC4 |
CC |
GG |
GC |
CC |
GG |
GC |
|
Живая масса при рождении, г |
1404,38 ±52,54 |
1297,6 ±53,68 |
1421,0 ±5,7 |
1059,5 ±19,5*** |
1228,8 ±37,7 |
1081,75 ±37,9*** |
|
Живая масса на 3 сутки, г |
1608,0 ±59,9 |
1546,4 ±69,03 |
1818,0 ±46,61 |
1559,0 ±31,0 |
1299,2 ±85,3* |
1316,9 ±48,02*** |
|
Живая масса на 9 сутки, г |
2245,25 ±119,9 |
2364,2 ±126,59 |
2332,7 ±106,73 |
2749,0 ±322,0** |
2617,2 ±87,1* |
2782,5 ±81,9** |
|
Живая масса на 21 сутки, г |
4724,25 ±44,92 |
5196,2 ±59,68 |
4962,0 ±17,62 |
4918,5 ±24,5* |
5293,8 ±51,1 |
5039,9 ±32,39 |
|
Показатель |
Группа |
|||||
|
3 |
4 |
|||||
|
Генотип по FUT1 |
GG |
AA |
AG |
GG |
AA |
AG |
|
Генотип по MUC4 |
CC |
GG |
GC |
CC |
GG |
GC |
|
Живая масса при рождении, г |
1306,0 ±63,49 |
1522,25 ±103,4 |
1311,5 ±70,4 |
1306,5 ±36,06 |
1254,8 ±38,89** |
1298,0 ±29,3 |
|
Живая масса на 3 сутки, г |
1593,2 ±74,22 |
1626,0 ±94,35 |
1575,3 ±104,32 |
1525,67 ±76,11 |
1534,0 ±77,05 |
1539,5 ±127,41 |
|
Живая масса на 9 сутки, г |
2850,2 ±135,7 |
2821,5 ±61,9 |
2812,75 ±105,44 |
2756,17 ±66,45 |
2811,2 ±137,99 |
2795,0 ±200,74 |
|
Живая масса на 21 сутки, г |
5508,2 ±32,34 |
5860,3 ±55,6 |
5185,7 ±83,37 |
5034,67 ±98,15*** |
5716,2 ±111,3 |
5563,2 ±125,18** |
Продолжение Таблицы
|
Показатель |
Группа |
|||||
|
5 |
6 |
|||||
|
Генотип по FUT1 |
GG |
AA |
AG |
GG |
AA |
AG |
|
Генотип по MUC4 |
CC |
GG |
GC |
CC |
GG |
GC |
|
Живая масса при рождении, г |
1645,0 ±175,0 |
1575,33 ±48,67 |
1698,17 ±107,66 |
1043,5 ±144,5*** |
1012,67 ±9,39*** |
1132,0 ±45,68*** |
|
Живая масса на 3 сутки, г |
1683,5 ±79,5 |
1699,67 ±54,91 |
1708,33 ±134,31 |
1491,5 ±18,5* |
1375,0 ±56,71* |
1342,83 ±63,42* |
|
Живая масса на 9 сутки, г |
2381,5 ±97,5 |
2497,6 ±205,96 |
2304,5 ±83,61 |
2317,0 ±120,0 |
2180,0 ±73,7* |
2242,33 ±24,03 |
|
Живая масса на 21 сутки, г |
4488,5 ±12,5 |
5131,0 ±126,51 |
4812,17 ±21,12 |
4642,5 ±48,5* |
4934,33 ±14,68 |
4783,17 ±25,02 |
Примечание: * -р<0,05, ** -р<0,01, *** -р<0,001, 2-я группа в сравнении с 1-й, 4-я группа в сравнении с 3-й, 6-я группа в сравнении с 5-й группой.
Анализ данных таблицы позволяет заключить, что даже при одинаковом генотипе по генам FUT1 и MUС4 живая масса поросят имела достоверные различия как при рождении, так и в процессе выращивания.
Таким образом, полученные данные прямо указывают на факт того, что условия кормления поросят до отъёма существенно сказывались на интенсивности роста особей с одинаковыми аллелями по генам FUT1 и MUC4.
После проведения анализа физиологических особенностей динамики изменения живой массы поросят в зависимости от аллелей по генам FUT1 и MUС4 выяснилось, что наибольшая живая масса была у поросят с генотипом АА/GG (FUT1/MUС4). Второе место занимали особи поросят с генотипом АG/ GС (FUT1/MUС4) кроме третьей группы. Наименьшую живую массу в нашем исследовании мы установили у поросят с генотипом GG/СС (FUT1/MUС4). В третьей группе животных, которой добавляли инъекции препарата «Элеовит», максимальная живая масса была более 5860 г у генотипа АА/GG (FUT1/ MUС4), что на 352,1 г больше (р<0,05) от генотипа GG/СС (FUT1/MUС4) и на 676,6 г больше (р<0,001) генотипа АG/GС (FUT1/ MUС4). В четвертой группе поросят, которой добавляли инъекции препарата «Элеовит», максимальная живая масса была более 5710 г у генотипа АА/GG (FUT1/MUС4), что на 681,53 г больше (р<0,05) от генотипа GG/СС (FUT1/MUС4) и на 153 г больше генотипа АG/ GС (FUT1/MUС4). В пятой и шестой группе поросят, которых на третий день перевели к мачехе, максимальная живая масса на 21 сутки выращивания была 5131 и 4934 г соответственно у генотипов АА/GG (FUT1/MUC4).
Таким образом, нами показаны функциональные особенности влияния условий кормления поросят крупной белой породы разных генотипов по генам FUT1 и MUС4 как на конечную живую массу, так и на интенсивность роста животных в подсосный период. Более высокая интенсивность роста и развития может наблюдаться у групп поросят с меньшей живой массой на момент отъема и с меньшей живой массой на момент рождения.
Выводы. Установлены физиологические особенности интенсивности роста и развития поросят разных генотипов по генам FUT1 и MUС4. После проведения анализа физиологических особенностей динамики изменения живой массы поросят в зависимости от аллелей по генам FUT1 и MUС4 выяснилось, что наибольшая живая масса была у поросят с генотипом АА/GG (FUT1/MUС4), потом следовали особи с генотипом АG/GС (FUT1/MUС4) кроме третьей группы, и наименьшая живая масса была у поросят с генотипом GG/СС (FUT1/MUC4).
Таким образом, полученные результаты указывают на то, что генотипирование поросят по генам FUT1 и MUС4 может быть использовано не только для определения устойчивости к кишечным инфекциям, но и для прогнозирования физиологических особенностей роста и развития на ранних стадиях онтогенеза.


