Иммуноферментная тест-система для межоперационного контроля специфичности рекомбинантного капсидного белка цирковируса свиней 2-го типа
Автор: Кузнецова Ю.А., Ахунова А.Р., Галеева А.Г., Хаертынов К.С., Ефимова М.А.
Рубрика: Ветеринария
Статья в выпуске: 4 т.264, 2025 года.
Бесплатный доступ
Цирковирусные инфекции свиней (ЦВИС), вызываемые преимущественно цирковирусом свиней 2-го типа (ЦВС-2), представляют собой одну из наиболее значимых проблем в мировом свиноводстве. Ключевым инструментом контроля и профилактики ЦВИС является вакцинация. Рекомбинантные аналоги капсидного белка (rCap) цирковируса свиней 2-го типа (ЦВС-2) являются ключевыми компонентами современных диагностических тест-систем и субъединичных вакцин. Стабильность его антигенной активности – критический параметр, определяющий эффективность и воспроизводимость функционального продукта. Целью настоящего исследования явилась разработка и апробация иммуноферментной тест-системы для межоперационного контроля специфической активности белка rCap. Для получения рекомбинантных аналогов капсидного белка ЦВС-2 использовали ранее сконструированные рекомбинантный штаммпродуцент E. coli BL21(DE3)pLysS-ORF2 (для прокариотического аналога) и стабильно экспрессирующую клеточную линию яичников китайского хомячка CHO-K1/PCV-ORF2 (для эукариотического аналога), очистку белков проводили по ранее разработанным протоколам. Для сенсибилизации твердой фазы (полистироловых планшетов) использовали хроматографически очищенный IgG, выделенный из пула сывороток серопозитивных к ЦВС-2 свиней; специфический пероксидазный конъюгат получали перйодатным методом. В результате исследований получен стабильный пероксидазный конъюгат с плотностью мечения 1,5:1. Разработанная тест-система позволила провести полуколичественный анализ рекомбинантного сырья, демонстрируя хорошую воспроизводимость (коэффициент вариации < 7%). Установлено, что тест-система является универсальной и позволяет оценивать активность вариантов rCap, полученных как в прокариотических, так и в эукариотических системах экспрессии, корректно распознавая их антигенные детерминанты. Таким образом, внедрение метода полуколичественного ИФА в производственный цикл позволит стандартизировать процесс межоперационного контроля качества биомассы, полученной при помощи технологий рекомбинантных ДНК, и гарантировать стабильные антигенные характеристики вакцинных и диагностических препаратов.
Цирковирус свиней 2-го типа, капсидный белок, технологии рекомбинантных ДНК, гетерологичная экспрессия, иммуноферментный анализ, межоперационный контроль качества сырья
Короткий адрес: https://sciup.org/142246744
IDR: 142246744 | УДК: 636.3:619:578:577.2 | DOI: 10.31588/2413_4201_1883_4_264_50
Enzyme immunoassay test system for interoperative control of the specificity of recombinant capsid protein of porcine circovirus type 2
Porcine circovirus infections, primarily caused by porcine circovirus type 2 (PCV2), are one of the most significant problems in global pig production. Vaccination is a key tool for control and prevention of porcine circovirus infections. Recombinant analogs of capsid protein (rCap) of porcine circovirus type 2 (PCV2) are key components of modern diagnostic test systems and subunit vaccines. The stability of its antigenic activity is a critical parameter determining the efficiency and reproducibility of the functional product. The aim of this study was to develop and test an enzymelinked immunosorbent assay system for interoperational monitoring of the specific activity of rCap protein. To obtain recombinant analogues of the PCV-2 capsid protein, the previously constructed recombinant E. coli BL21(DE3)pLysSORF2 producer strain (for prokaryotic analogue) and the stably expressing Chinese hamster ovary cell line CHO-K1/PCVORF2 (for eukaryotic analogue) were used; protein purification was performed according to previously developed protocols. Chromatographically purified IgG isolated from a pool of sera from PCV-2-seropositive pigs was used for sensitization of the solid phase (polystyrene plates); the specific peroxidase conjugate was obtained by the periodate method. The study resulted in the production of a stable peroxidase conjugate with a labeling density of 1.5:1. The developed test system enabled semiquantitative analysis of recombinant raw materials, demonstrating good reproducibility (coefficient of variation <7%). The test system was found to be universal and capable of assessing the activity of rCap variants obtained in both prokaryotic and eukaryotic expression systems, accurately recognizing their antigenic determinants. Thus, the implementation of the semiquantitative ELISA method in the production cycle will standardize the process of in-process quality control of biomass obtained using recombinant DNA technologies and guarantee stable antigenic characteristics of vaccines and diagnostic products.
Текст научной статьи Иммуноферментная тест-система для межоперационного контроля специфичности рекомбинантного капсидного белка цирковируса свиней 2-го типа
В этих условиях вакцинация является ключевым инструментом контроля и профилактики ЦВС-2. Наряду с традиционными инактивированными вакцинами все большее значение приобретает разработка современных генно-инженерных вакцин. Такие препараты, основой которых являются рекомбинантные аналоги мажорного капсидного белка ЦВС-2 (Cap), кодируемого геном ORF-2 и содержащего основные протективные эпитопы, обладают рядом преимуществ: высокой степенью очистки, безопасностью (отсутствием риска реверсии вирулентности), стабильностью и возможностью крупномасштабного стандартизированного производства [6, 7, 8].
Производство рекомбинантных вакцин является многостадийным технологическим процессом, требующим строгого контроля сырья на каждом этапе. Одним из важнейших аспектов считается подтверждение специфичности рекомбинантного антигена – это является гарантией того, что в ходе культивирования штамма-продуцента либо стабильно экспрессирующей клеточной линии был получен целевой белок, сохранивший свою антигенную структуру [9, 10]. Особенно актуальной эта задача становится при использовании различных систем экспрессии для разных целей
(диагностических и профилактических), таких как прокариотических (E. coli) или основанных на применении перевиваемых линий клеток млекопитающих. Белки, полученные путем биосинтеза в разных системах экспрессии, могут отличаться посттрансляционными модификациями и конформацией, что потенциально влияет на их антигенные и иммуногенные свойства [11]. Следовательно, необходим универсальный метод межоперационного контроля, способный подтвердить наличие и специфичность рекомбинантного капсидного белка ЦВС-2.
Для решения этой задачи наиболее подходящим инструментом является иммуно-ферментный анализ (ИФА) в «сэндвич»-формате [12]. В отличие от таких методов, как электрофорез в полиакриламидном геле и вестерн-блоттинг, которые в первую очередь оценивают молекулярную массу белка и его реактивность к антителам в денатурирующих условиях, антигенный ИФА позволяет оценить нативную или близкую к нативной конформацию антигена. «Сэндвич»-ИФА, использующий два типа специфических антител (первичные – связывающие и вторичные – детектирующие), обеспечивает высокие чувствительность и специфичность реакции [13]. Этот метод позволяет не только подтвердить наличие рекомбинантного антигена, но и количественно оценить его концентрацию в неочищенных культуральных жидкостях и первичных клеточных лизатах, промежуточных фракциях и конечном продукте. Высокая производительность, возможность автоматизации и относительно низкая стоимость делают ИФА оптимальным выбором для рутинного межоперационного контроля в условиях промышленного производства вакцин.
Целью настоящей работы явилась разработка и валидация иммуноферментной тест-системы для межоперационного контроля специфичности рекомбинантного капсидного белка (rCap) ЦВС-2.
Условия, материалы и методы. Исследования проводились в лаборатории вирусных антропозоонозов ФГБНУ «ФЦТРБ-ВНИВИ» в период с августа по октябрь 2025 г.
Продуценты и референтные образцы антигенов .
В работе использовались:
-
– Штамм E. coli – продуцент rCap BL21 (DE3)pLysS-ORF2 (ФГБНУ «ФЦТРБ-ВНИВИ»);
-
– Стабильно экспрессирующая клеточная линия яичников китайского хомячка - CHO-K1/PCV-ORF2 (ФГБНУ «ФЦТРБ-ВНИВИ»);
-
- Нативный антиген ЦВС-2 (штамм «PCV2 -SHBC», ФКП «Щелковский биокомбинат» с исходной концентрацией 2 мг/мл [14];
-
– Рекомбинантный аналог Cap прокариотического происхождения (ФГБНУ «ФЦТРБ-ВНИВИ» с исходной концентрацией 6 мг/мл [15];
-
– Рекомбинантный аналог Cap,
полученный путем биосинтеза в клеточной линии CHO-K1 (ФГБНУ «ФЦТРБ-ВНИВИ») с исходной концентрацией 4 мг/мл.
Получение специфического пероксидазного конъюгата . Выделение специфических иммуноглобулинов из пула сывороток свиней, иммунных к ЦВС-2, производили методом трехкратного переосаждения насыщенным раствором сульфата аммония (НСА) с последующей хроматографической очисткой на ДЭАЭ-целлюлозе.
Постановка ИФА . Протокол постановки непрямого варианта ИФА был оптимизирован методом шахматного титрования сенсибилизирующего иммуноглобулина, антигена и специфического пероксидазного конъюгата. 96-луночные полистироловые планшеты средней сорбции (ВНИИ «Медполимер», Россия) сенсибилизировали двукратными разведениями иммуноглобулина (от 10 до 0,05 мкг/мл) на 0,05 М карбонатно-бикарбонатном буфере (рН 9,6) в объеме 100 мкл/лунку и инкубировали 18 ч при 4°С. Промывку осуществляли трехкратно после каждого этапа ИФА фосфатносолевым буфером с добавлением 0,05% Tween-20 (ФСБ-Т). Нативные и рекомбинантные референс-антигены вносили в концентрациях от 1 до 0,001 мг/мл на ФСБ-Т и инкубировали 1 ч при 37°С. Специфический пероксидазный конъюгат, предварительно полученный перйодатным методом по Nakane [16], вносили в концентрациях от 5 до 0,01 мкг/мл и инкубировали аналогично. После финальной промывки добавляли по 100 мкл/лунку субстратного раствора тетраметилбензидина (ТМБ, «BD Biosciences», США), реакцию останавливали через 15 мин внесением 100 мкл 2 М H 2 SO 4 . Оптическую плотность (ОП) измеряли на спектрофотометре «Model 680» («Bio-Rad», США) при длине волны 450 нм. Ключевым критерием оценки сохранности специфической антигенной активности рекомбинантных аналогов белка Cap считали коэффициент специфического связывания (S/N, signal-to-noise), который рассчитывался для каждой концентрации специфических компонентов как отношение ОП ср в лунках с положительными контрольными антигенами к ОП ср в лунках с отрицательными контрольными антигенами.
Статистический анализ . Эксперименты проводились в трипликатах, данные представлены в виде среднего значения и стандартного отклонения (M±SD). Статистическую обработку результатов проводили с использованием программного обеспечения «GraphPad Prism 9.0» («GraphPad Software», США). Для построения кривых титрования использовали нелинейную регрессию. Различия считали статистически значимыми при p<0,05.
Результаты и обсуждение. Для создания стандартизированной ИФА-тест-системы, предназначенной для межоперационного контроля специфичности rCap, требовались получение и характеристика ключевых компонентов для анализа.
В качестве основного реагента для сенсибилизации твердой фазы был использован иммуноглобулин класса G (IgG), выделенный из пула сывороток позитивных к ЦВС-2
свиней. Контроль чистоты препарата, подвергнутого ионо-обменной хроматографии на ДЭАЭ-целлюлозе, осуществляли при нативного электрофореза помощи (рис. 1).
а)
б)
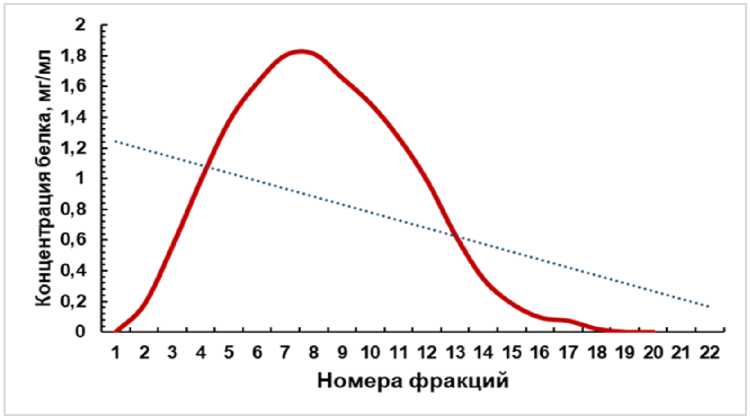
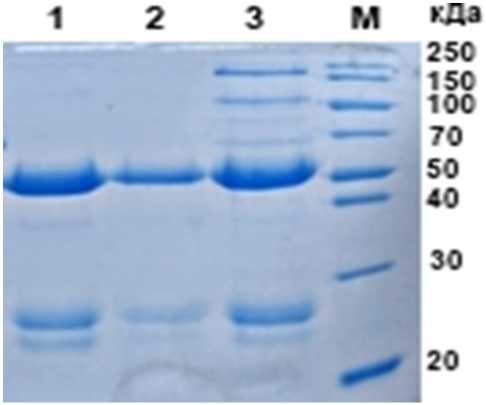
Рисунок 1 - Результаты хроматографической очистки анти-ЦВС иммуноглобулинов: а - гистограмма элюции IgG, б - нативная электрофореграмма очищенных IgG, где 1-3 - фракции IgG, М - маркер молекулярных масс «PageRuler» («Thermo Scientific», США)
Из электрофореграммы (рис. 1б) визуализируются две основные полипептидные фракции, соответствующие тяжелой (H-цепь, 50 кДа) и легкой (L-цепь, 25 кДа) цепям IgG, при этом выраженность минорных полос незначительна, что свидетельствует о высокой степени очистки препарата и его пригодности для дальнейшего использования в ИФА.
Далее для детекции комплекса «антиген-антитело» был получен конъюгат анти-ЦВС иммуноглобулина с пероксидазой хрена (ПХ). Конъюгация была проведена перйодатным методом, обеспечивающим ковалентное связывание через альдегидные группы, образующие при окислении углеводных компонентов молекулы ПХ. Ключевой характеристикой, определяющей чувствительность и специфичность конъюгата, является плотность мечения – молярное соотношение молекул ПХ к молекулам IgG, вычисляемое по максимумам поглощения гема пероксидазы (403 нм) и ароматических аминокислот белка (280 нм). Проведенные расчеты показали, что для полученного конъюгата плотность мечения составила 1,5:1. Такое значение способно обеспечить достаточную ферментативную активность для надежной детекции сигнала, но при этом минимизирует риск стерических погрешностей и неспецифического связывания. Конъюгат был стабилизирован добавлением 1% БСА.
На основе кривых титрования, полученных для исходной партии анти-ЦВС иммуноглобулина, была определена его оптимальная рабочая концентрация (ОРК). За ОРК принимали наименьшие концентрации специфического иммуноглобулина и пероксидазного конъюгата, которые обеспечивали: а) соотношение ОПср(К+) в диапазоне 1,1-1,4, что соответствует линейному участку детекции спектрофотометра; б) максимально возможное значение коэффициента S/N, но не менее 6,5. В данном эксперименте ОРК иммуноглобулина составила 4,5 мкг/мл, ОРК пероксидазного конъюгата - 8 мкг/мл: при этих концентрациях значение S/N составляло в среднем (10,2±0,8) ед.
Для межоперационного контроля рекомбинантных антигенов каждая новая партия rCap тестировалась с помощью разработанного ИФА параллельно с референс-образцами. Партия считалась соответствующей требованиям специфической антигенной активностью, если при ее тестировании с ОРК специфического иммуноглобулина выполнялись следующие условия:
-
1. Значение ОП ср образца находилось в пределах ± 20% от значения ОП ср (К+), полученного для референс-антигенов в том же эксперименте.
-
2. Значение коэффициента S/N было не ниже 85% от значения S/N референсантигенов, т.е. не ниже 8,6 ед. (для данной партии конъюгата).
Этот подход позволил стандартизировать оценку функциональной активности антигена, нивелируя межпланшетную и межоператорскую вариабельность, и гарантировать стабильность диагностических характеристик тест-системы при использовании различных серий рекомбинантных белков.
Ключевой задачей при производстве вакцин и диагностикумов с использованием технологий рекомбинантных ДНК является обеспечение стабильности и функциональной активности антигена на всех этапах - от индукции экспрессии до очистки конечного продукта. Рекомбинантный капсидный белок ЦВС-2 может быть получен в нескольких системах, каждая из которых имеет свои особенности, влияющие на фолдинг, посттрансляционные модификации и, как следствие, антигенную активность и иммуногенность белка. Исходя из этого, необходимо учитывать следующее:
-
а) Прокариотический синтез (в E. coli ) позволяет получить большое количество белка, но это часто приводит к образованию нерастворимых агрегатов (телец включения). Процесс рефолдинга (восстановления нативной структуры) является критическим этапом и напрямую определяет долю функционально активного белка в конечном препарате. Некорректно свернутые молекулы, присутствуя в образце, могут не распознаваться специфическими антителами.
-
б) Эукариотический синтез (в клетках млекопитающих) обеспечивает нативный фолдинг и гликозилирование белка, что приближает его структуру к оригинальной. Однако культуральная среда и продукты лизиса клеток могут содержать компоненты, интерферирующие в анализе и снижающие стабильность антигена при хранении.
Для унификации контроля качества было необходимо установить зависимость между концентрацией рекомбинантного белка и его функциональной активностью, выраженной посредством коэффициента S/N. Для апробации данного критерия был проведен анализ различных образцов рекомбинантного сырья: исходных клеточных лизатов, промежуточных продуктов очистки, очищенных продуктов. Все образцы перед анализом были нормализованы по общей концентрации белка до 1 мг/мл. Результаты ИФА представлены в таблице.
Таблица - Оценка специфической антигенной активности продуктов рекомбинантного синтеза капсидного белка ЦВС-2
|
№ п/п |
Вид технологического сырья |
Значение S/N |
Соответствие критерию (S/N > 8,6 для данной партии конъюгата) |
|
1 |
Нативный цельновирионный антиген ЦВС-2 |
10,3 ± 0,7 |
соответствует |
|
2 |
Референс-антиген rCap прокариотического происхождения |
11,2 ± 0,8 |
соответствует |
|
3 |
Референс-антиген rCap эукариотического происхождения |
15,2 ± 1,1 |
соответствует |
|
4 |
Лизат клеток штамма-продуцента E. coli BL21(DE3)/pLysS-pET-28a(+)-ORF2 |
9,7 ± 0,4 |
соответствует |
|
5 |
Бесклеточный экстракт штамма-продуцента E. coli BL21(DE3)/ pLysS-pET-28a(+)-ORF2 |
3,1 ± 0,2 |
не соответствует |
|
6 |
Солюбилизированные тельца включения, содержащие агрегированный rCap |
9,1 ± 0,7 |
соответствует |
|
7 |
rCap прокариотического происхождения после рефолдинга и финишной очистки |
10,9 ± 0,9 |
соответствует |
|
8 |
Лизат клеток экспрессирующей линии CHO-K1/ORF2 |
9,5 ± 1,1 |
соответствует |
|
9 |
Бесклеточный экстракт экспрессирующей линии CHO-K1/ORF2 |
8,9 ± 0,4 |
соответствует |
|
10 |
rCap эукариотического происхождения после финишной очистки |
17,7 ± 2,1 |
соответствует |
Представленные данные демонстрируют, что партии сырья, прошедшие полный цикл очистки (позиции 7 и 10) демонстрируют высокие коэффициенты S/N, сопоставимые с референс-образцами или превосходящие их. В то же время прокариотический препарат, не подвергавшийся процедуре рефолдинга (6), и эукариотический препарат до очистки от балластных компонентов (9), демонстрировали в среднем более низкие значения S/N, несмотря на то, что общая концентрация белка была стандартизирована. Это наглядно демонстрирует преимущество разработанного метода для выявления именно функционально активного антигена. Примечательно, что варианты капсидного белка, синтезированного в эукариотической системе экспрессии (3, 10), отличались наибольшим коэффициентом S/N, что может свидетельствовать о более подходящей для серологических реакций конформации иммуногенных эпитопов.
Выводы. В рамках настоящего исследования была проведена апробация непрямой ИФА-тест-системы для полуколичественной оценки специфической антигенной активности рекомбинантного капсидного белка (rCap) ЦВС-2. Данная методика является важным инструментом для стандартизации и контроля качества биомассы, полученной при помощи технологий рекомбинантного синтеза, где стабильность функциональных свойств антигенов от партии к партии имеет критическое значение.
Ключевым результатом работы стало создание набора реагентов, в том числе рекомбинантных референс-антигенов, высокоочи-щенного IgG к ЦВС-2 и специфического пероксидазного конъюгата с плотностью мечения 1,5:1, что обеспечило высокую чувствительность и специфичность анализа. Метод продемонстрировал хорошую воспроизводимость (коэффициент вариации составил < 7%), что позволит применять его в целях рутинного межоперационного контроля. Преимуществом разработанного подхода является его универсальность: метод основан на оценке способности антигена связываться с поликлональными антителами, что позволяет эффективно детектировать и оценивать активность rCap независимо от системы его экспрессии. Метод является эффективным как в отношении белка, полученного в прокариотической системе экспрессии, так и в отношении его гликозилированных вариантов, полученных в клетках млекопитающих.
Таким образом, внедрение данного метода в производственный процесс, в том числе при использовании разных платформ синтеза антигенов либо при переходе с одной технологии на другую, позволит повысить качество конечного продукта и обеспечить их стабильность.


