Исследование электронной структуры и связывающих орбиталей афлатоксина В1 методом DFT
Автор: Руськина А.А., Малинин А.В.
Рубрика: Биохимический и пищевой инжиниринг
Статья в выпуске: 1 т.14, 2026 года.
Бесплатный доступ
Данное исследование представляет собой комплексный анализ электронной структуры молекулы афлатоксина B1, выполненный современными квантово-химическими методами. Афлатоксин В1 является вторичным метаболитом, который продуцируется некоторыми видами микроскопических плесневых грибов рода Аспергилл (Aspergillus flavus, A. Parasiticus). Основной целью работы было применение двух высокоэффективных инструментов: теории функционала плотности (метод DFT с расчетным уровнем B3LYP/3-21G) и анализа естественных связывающих орбиталей (NBO). Данные подходы позволяют детально изучить распределение электронных плотностей внутри молекулы, показывая высокую степень делокализации электронов, распространяющихся вплоть до внутренних слоев атомов углерода. Такой эффект обусловлен сильными донорно-акцепторными взаимодействиями, способствующими повышенной стабильности молекулы. Ключевым моментом стало обнаружение уязвимого участка молекулы – лактонной связи O4–C23, характеризующейся выраженной поляризацией. Эта связь выступает своего рода «слабым звеном», определяющим повышенную реакционную способность афлатоксина B1. Именно эта область проявляет особую активность, играя ключевую роль в механизмах токсического воздействия афлатоксина B1. Понимание особенностей строения молекулы позволяет углубленно исследовать ее взаимодействие с компонентами клеточных структур, особенно с клейковинными белками зерновых культур. Полученные данные обладают большим потенциалом для разработки методов защиты пищевой продукции от загрязнения микотоксинами, обеспечивая биобезопасность конечного продукта. Результаты представленного исследования вносят существенный вклад в фундаментальные знания о структуре и функционировании афлатоксина B1, позволяя создать новые стратегии борьбы с опасным загрязнением пищевых ресурсов.
Афлатоксин В1, теория функционала плотности, естественная связывающая орбиталь, квантово-химическое моделирование
Короткий адрес: https://sciup.org/147253475
IDR: 147253475 | УДК: 664.696.9 | DOI: 10.14529/food260106
DFT study of the electronic structure and bonding orbitals of Aflatoxin B1
This study presents a comprehensive analysis of the electronic structure of the aflatoxin B1 molecule, performed using modern quantum chemical methods. Aflatoxin B1 is a secondary metabolite produced by certain species of microscopic mold fungi of the genus Aspergillus (Aspergillus flavus, A. parasiticus). The primary objective of the study was the application of two highly effective tools: density functional theory (DFT with the B3LYP/321G calculation level) and natural bonding orbital (NBO) analysis. These approaches enable a detailed study of the electron density distribution within the molecule, revealing a high degree of electron delocalization extending all the way to the inner layers of carbon atoms. This effect is due to strong donoracceptor interactions, which contribute to the increased stability of the molecule. A key achievement was the discovery of a vulnerable region of the molecule – the lactone bond O4C23, characterized by pronounced polarization. This bond acts as a “weak link” that determines the increased reactivity of aflatoxin B1. It is this region that exhibits particular activity, playing a key role in the mechanisms of aflatoxin B1's toxic effects. Understanding the structural features of the molecule allows for a more indepth study of its interactions with cellular components, particularly with gluten proteins in grain crops. The data obtained hold great potential for developing methods to protect food products from mycotoxin contamination, ensuring the biosafety of the final product. The results of this study significantly contribute to fundamental knowledge of the structure and function of aflatoxin B1, enabling the development of new strategies to combat this dangerous contamination of food resources.
Текст научной статьи Исследование электронной структуры и связывающих орбиталей афлатоксина В1 методом DFT
А.А. Ruskina, , A.V. Malinin, , South Ural State University, Chelyabinsk, Russia
Афлатоксин В1 является органическим соединением из группы поликетидов и относится к микотоксинам. Это вторичный метаболит, который продуцируется некоторыми видами микроскопических плесневых грибов рода Аспергилл ( Aspergillus flavus, A. parasiticus ). Заражение зерновых культур, кормов афлатоксином B1 и актуальность его обеззараживания связаны с тем, что даже минимальное количество афлатоксинов способно нанести вред здоровью населения. Биологическая активность афлатоксина B1 заключается в особенностях его электронной структуры, в частности в высокой реакционной способности концевого дигидрофуранового фрагмента.
Детальное понимание природы химических связей и внутримолекулярных взаимодействий в афлатоксине B1 необходимо для разработки стратегий его нейтрализации [1, 3].
Теория функционала плотности (DFT) предоставляет надежную основу для квантово-химического моделирования таких сложных органических молекул. Для интерпретации результатов DFT в терминах классической химической теории связи особенно эффективен анализ естественных связывающих орбиталей (NBO), который позволяет количественно оценить вклад различных делока-лизационных и донорно-акцепторных взаимодействий в стабильность молекулы [7, 10].
Метод NBO (Natural Bond Orbital) – это подход для анализа природы связей в молекулах. Он позволяет вычислять естественные орбитальные связи (NBO) – локализованные орбитали с несколькими атомными центрами, которые описывают модель молекулярных связей электронных пар в оптимально компактной форме. Метод основан на методе оптимального преобразования заданной волновой функции в локализованную форму, соответствующую элементам структуры Льюиса: одноцентровым («неподелённые пары») и двухцентровым («связи») [2].
В анализе NBO входной набор атомных орбиталей афлатоксина В1 преобразуется через естественные атомные орбитали и гибридные орбитали в NBO. Алгоритм состоит из поиска орбиталей с высокой занятостью в локализованных регионах молекулы. Далее осуществляется расчёт энергии и выбор резонансной структуры взаимодействия орбиталей, которая позволит найти оптимальную структуру Льюиса.
Целью данной работы является анализ электронной структуры молекулы афлатоксина В1 с помощью метода естественных связывающих орбиталей (NBO/ DFT).
Объекты и методы исследования
Для изучения электронной структуры мо- лекулы афлатоксина В1 с помощью метода естественных связывающих орбиталей (NBO) проводились квантово-химические расчеты с использованием программного пакета Gaussian 16. В исследованиях использовался метод Ground State DFT (Default Spin) с применением базисного набора 3-21G/ B3LYP (гибридный функционал).
Исходные данные о молекуле афлатоксина В1 для квантово-химического расчета были получены при помощи базы данных PubChem. В рамках исследования учитывались такие показатели, как локализация молекулярных орбиталей HOMO и LUMO, анализ естественных связывающих орбиталей (NBO), анализ NBO второго порядка для молекулы. Затем осуществлялась статистическая обработка полученных данных квантово-химических расчётов.
Результаты и их обсуждение
На первом этапе исследования после оптимизации геометрии, которая позволяет найти наиболее стабильную структуру, которая имеет наименьшую энергию, осуществлялся расчет энергии высшей занятой (HOMO) и низшей свободной (LUMO) молекулярных орбиталей афлатоксина В1. Локализация молекулярных орбиталей HOMO и LUMO для афлатоксина В1 представлена на рис. 1.
Локализация молекулярных орбиталей
Молекулярные орбитали афлатоксина В1
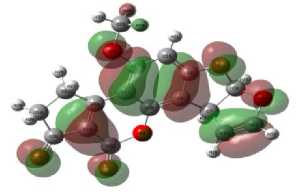
HOMO
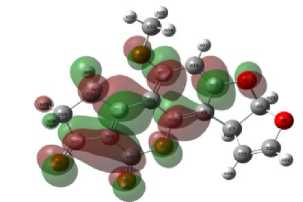
LUMO
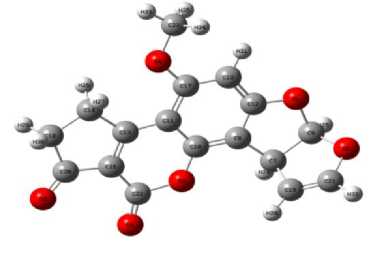
Химическая структура
Рис. 1. Локализация молекулярных орбиталей HOMO и LUMO афлатоксина В1
HOMO афлатоксина В1 преимущественно наблюдается на π-системе кумарина. Локализация молекулярных орбиталей LUMO афлатоксина В1 наблюдается на 8,9-двойной связи фуранового кольца. Данная информация является важной для понимания электронной структуры молекулы афлатоксина В1 [5, 6].
На втором этапе исследования проводился анализ естественных связывающих орбиталей (NBO) афлатоксина В1, результаты которого представлены на рис. 2.
Проведенный анализ показывает разделение электронной плотности на Льюисовскую (локализованные связи) и не-Льюисовскую (делокализация, перенос заряда) составляющие. На рис. 2 показаны итерации поиска оптимального «Льюисовского» представления, где Occ. Thresh. (Occupancy Threshold) является порогом занятости, который постепенно снижается (с 1,90 до 1,50), позволяя включать в Льюисовскую структуру все более слабые (делокализованные) орбитали. К финальной итерации (22 цикла) достигается стабильное разбиение на Lewis при значении 158,279e (97,7 % от 162 валентных электронов) и NonLewis при значении 3,721e (2,3 %). Таким образом, полученные результаты квантово- химического расчета афлатоксина В1 позволяют отнести окончательную структуру молекулы к сильно делокализованной.
Программа обнаружила, что ядерные (core) 1s-орбитали 17 атомов углерода (C7-C23) имеют заселенность менее 2,0000 электронов. Полученные результаты указывают на сильную делокализацию электронов с внутренних оболочек.
Молекула афлатоксина В1 содержит конденсированные ароматические системы (кумариновый и фурановый фрагменты, а также гидрированный циклопентановый цикл, конъюгированный с системой). В таких высо-коконъюгированных системах делокализация π-электронов настолько сильна, что может вовлекать в общее взаимодействие даже σ-каркас и, как видно из анализа, затрагивать внутренние оболочки атомов. Это признак исключительно высокой степени сопряжения и электронной делокализации в молекуле афлатоксина В1 [8, 9, 11].
Valence Lewis (Валентные Льюисовские) составляет 112,309e (96, 82 % от 116). Это доля валентных электронов, описываемых классическими связями (CR, BD, LP). Далее Valence non-Lewis (Валентные не-Льюисов-
NATURAL BOND ORBITAL ANALYSIS
|
Cycle |
Occ. Thresh. |
Occupancies |
Lewis Structure |
Low occ (L) |
High OCC (NL) |
Dev |
||||
|
Lewis |
Non-Lewis |
CR |
BD |
3C |
LP |
|||||
|
1(1) |
1.90 |
155.94787 |
6.05213 |
23 |
47 |
0 |
11 |
11 |
10 |
0.49 |
|
2(4 |
1.90 |
156.16378 |
5.83622 |
23 |
46 |
0 |
12 |
9 |
9 |
0.49 |
|
3(3) |
1.90 |
156.16378 |
5.83622 |
23 |
46 |
0 |
12 |
9 |
9 |
0.49 |
|
4(1) |
1.80 |
156.27026 |
5.72974 |
23 |
43 |
0 |
15 |
5 |
8 |
0.49 |
|
5(2) |
1.80 |
156.27026 |
5.72974 |
23 |
43 |
0 |
15 |
5 |
8 |
0.49 |
|
6(1) |
1.70 |
157.29093 |
4.70907 |
23 |
44 |
0 |
14 |
2 |
8 |
0.37 |
|
2(2) |
1.70 |
157.29093 |
4.70907 |
23 |
44 |
0 |
14 |
2 |
8 |
0.37 |
|
8(1) |
1.60 |
157.76826 |
4.23174 |
23 |
45 |
0 |
13 |
1 |
8 |
0.40 |
|
9(2) |
1.60 |
157.84651 |
4.15349 |
23 |
45 |
0 |
13 |
1 |
8 |
0.33 |
|
10(3) |
1.60 |
157.81866 |
4.18134 |
23 |
45 |
0 |
13 |
1 |
8 |
0.37 |
|
11(4) |
1.60 |
157.76826 |
4.23174 |
23 |
45 |
0 |
13 |
1 |
8 |
0.40 |
|
12(5) |
1.60 |
157.84651 |
4.15349 |
23 |
45 |
0 |
13 |
1 |
8 |
0.33 |
|
13(1) |
1.50 |
157.84651 |
4.15349 |
23 |
45 |
0 |
13 |
1 |
8 |
0.33 |
|
14(2) |
1.50 |
158.27868 |
3.72132 |
23 |
46 |
0 |
12 |
0 |
8 |
0.37 |
|
15(3) |
1.50 |
158.21108 |
3.78892 |
23 |
46 |
0 |
12 |
0 |
8 |
0.40 |
|
16(4) |
1.50 |
157.84651 |
4.15349 |
23 |
45 |
0 |
13 |
1 |
8 |
0.33 |
|
17(5) |
1.50 |
158.27868 |
3.72132 |
23 |
46 |
0 |
12 |
0 |
8 |
0.37 |
|
18(6) |
1.50 |
158.21108 |
3.78892 |
23 |
46 |
0 |
12 |
0 |
8 |
0.40 |
|
19(7) |
1.50 |
157.84651 |
4.15349 |
23 |
45 |
0 |
13 |
1 |
8 |
0.33 |
|
20(8) |
1.50 |
158.27868 |
3.72132 |
23 |
46 |
0 |
12 |
0 |
8 |
0.37 |
|
21(9) |
1.50 |
158.21108 |
3.78892 |
23 |
46 |
0 |
12 |
0 |
8 |
0.40 |
|
22(1) |
1.50 |
158.27868 |
3.72132 |
23 |
46 |
0 |
12 |
0 |
8 |
0.37 |
Рис. 2. Результаты анализа естественных связывающих орбиталей (NBO) афлатоксина В1 в соответствии с циклами оптимизации ские) составляет 3,235e (2,00 %). Данная мера относится к делокализации (резонанс, гиперконъюгация, донорно-акцепторные взаимодействия). Rydberg non-Lewis (Ридберговские не-Льюисовские) составляет 0,487e (0,30 %), что наиболее часто связано с вакантными антисвязывающими орбиталями высоких энергетических уровней.
Стандартное Льюисовское описание (23 остова (CR), 46 связей (BD), 12 неподеленных пар (LP) в последней строке) покрывает ~97,7% электронной плотности. Однако оставшиеся ~2,3 % не-Льюисовской плотности, а особенно аномально низкая заселенность core-орбиталей множества атомов углерода, являются ярким квантово-химическим свидетельством экстремального сопряжения и делокализации электронов, которая пронизывает всю молекулу, включая σ-каркас и внутренние оболочки. Это может вносить вклад в высокую реакционную способность и электрофильность афлатоксина B1, особенно его способность к электрофильным атакам на ДНК.
На заключительном этапе исследования проводился анализ NBO второго порядка для молекулы афлатоксина В1, который показывает донорно-акцепторные взаимодействия внутри молекулы, стабилизирующие её структуру.
Донорная орбиталь является заполненной электронной парой. Акцепторная орбиталь является вакантной или частично заполненной. Под E(2) (ккал/моль) понимается ключевая величина, демонстрирующая энергию стабилизации за счет донорно-акцепторного взаимодействия. Чем выше значение, тем сильнее взаимодействие и тем больше его вклад в стабильность молекулы. Порог вывода равен 0,5 ккал/моль. Меньшая разность энергий E(j)-E(i) между акцепторной и донорной орбиталями (в атомных единицах) облегчает взаимодействие. Интеграл матрицы Фока между орбиталями i и j, обозначает меру их перекрывания.
Афлатоксин B1 имеет сложную полициклическую структуру с фурановым кольцом, кумариновым фрагментом и лактоном. Взаимодействия с энергиями E(2) > 10,000 ккал/моль, что указывает на критически важные для структуры взаимодействия, часто связанные с σ → σ или n → σ перекрываниями в напряженных циклах или соседних связях.
Таким образом, C-H → RY\* / BD\* (σ(C-H) → вакантные орбитали): строка 40. BD (1) C 18–H 29 /226. RY*(1) C 23 E(2) = 66357,06 ккал/моль – абсолютный максимум. Связь C18–H29 является мощнейшим донором электронной плотности на вакантную RY* орбиталь атома C23. Это говорит о сильном внутримолекулярном перераспределении заряда, возможно, стабилизирующем лактонный или фурановый фрагмент. Строка 40. BD (1) C18–H29 /258. BD*(1) C7–H24 E (2) = 27749,47 ккал/моль – сильнейшее σ(C-H) → σ*(C-H) взаимодействие. Строка 46. BD (1) C23–H35 /107. RY*(4) O 4 E(2)=18388,76 ккал/моль и другие взаимодействия с участием C23–H35. Атом C23, вероятно, находится в ключевом положении в лактонном кольце.
C-C → RY\* (σ(C-C) → вакантные орбитали): cтрока 29. BD (1) C14–C18 /202. RY*(8) C 18 E(2) = 13217,04 ккал/моль – связь C14–C18 (вероятно, в фурановом кольце) сильно донирует на свой же атом C18. Это признак многоцентровой связи или сильной поляризации.
Основные каркасные взаимодействия молекулы афлатоксина B1 (E(2) ~ 1000–5000 ккал/моль). Взаимодействия с участием карбонильных групп (C=O): наблюдаются в строке 7. BD (1) O4–C17 /122. RY*(1) C7 E(2) = 4033,96 ккал/моль. Один из атомов кислорода карбонильной группы (O4) донирует с своей σ(O-C) связи на соседний атом углерода (C7). Это типичное σ(O-C) → вакантная орбиталь взаимодействие, стабилизирующее карбонил. Многочисленные взаимодействия вида BD (1) O-C с RY* и BD* других атомов (например, O1–C9, O3–C10, O4–C23 с энергиями 200-1500 ккал/моль) показывают, как кислородные «мостики» перераспределяют плотность по всей молекуле.
Взаимодействия в ароматических/нена-сыщенных системах наблюдаются в строке 8. BD (1) O4–C23 /250. BD*(1) O4–C23 E(2) = 1378.42 ккал/моль. Здесь σ-связь O4– C23 взаимодействует с антисвязывающей орбиталью той же самой связи (BD* O4–C23). Это прямое указание на полярность и ослаб-ленность этой связи, что может иметь ключевое значение для реакционной способности (например, при раскрытии лактонного кольца). Взаимодействия между связями C-C аро-матических/ненасыщенных колец (например, C13–C14 с C13–C16, C14–C18 с C13–C16 с энергиями ~2000-3000 ккал/моль) демонстри- руют делокализацию электронной плотности по скелету молекулы.
Умеренные и слабые взаимодействия (E(2) < 1000 ккал/моль) важны для тонкой настройки геометрии и зарядового распределения. Взаимодействия типа π(C=C) → π\*(C=C) или **π(C=C) → RY\*** (например, строки 12, 13, 14) с энергиями 100-500 ккал/моль. Это классическая гиперконъюгация в ненасыщенных системах.
Ключевые реакционные центры: лактонный мотив (O4–C23): связь O4–C23 является одновременно и сильным донором, и сильным акцептором (взаимодействие 8/250). Это делает её потенциально слабым звеном, подверженным нуклеофильной атаке. Фурановое кольцо (C14, C18, C19, C20, C21), где атомы этого кольца (особенно C18, H29) участвуют в сильнейших донорных взаимодействиях. Двойная связь в фурановом кольце также вовлечена в стабилизирующую гиперконъюгацию. Карбонильные группы активно стягивают электронную плотность на себя, поляризуя связи C=O и делая карбонильный углерод электрофильным. Основной вклад в стабилизацию молекулы вносят не классические π-сопряжения, а многочисленные сильные σ → σ и σ → RY взаимодействия [2, 4, 5].
Выводы по результатам работы
Проведённое квантово-химическое моделирование методом DFT при анализе электронной структуры молекулы афлатоксина В1 с помощью метода естественных связывающих орбиталей (NBO) позволило выявить сильнейшие донорно-акцепторные взаимодействия, дестабилизирующие отдельные связи (O4–C23) и создающие реакционноспособные электрофильные центры, что является фундаментальной основой его механизма токсического действия. Наличие десятков взаимодействий с энергией в тысячи ккал/моль указывает на высокую степень внутримолекулярной делокализации заряда и напряженность в циклах. Это коррелирует с высокой реакционной способностью и токсичностью афлатоксина B1.


