Исследование влияния антимикробных соединений пряностей на молочнокислый процесс
Автор: Закрепина Е.Н., Носкова В.И.
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Рубрика: Технические науки
Статья в выпуске: 3 (59), 2025 года.
Бесплатный доступ
В статье приводятся результаты исследования динамики молочнокислого процесса при культивировании консорциума микроорганизмов йогуртовой закваски в присутствии экстрактов пряностей. Пряности в натуральном виде и их экстракты применяются в технологии молочных продуктов в качестве пищевых консервантов и пищевкусовых компонентов. Антимикробные свойства пряностей по отношению к условно-патогенным и патогенным микроорганизмам изучены, поэтому актуальным является изучение влияния антимикробных свойств пряностей на метаболические процессы различных видов молочнокислых микроорганизмов с целью выявления возможного торможения молочнокислого процесса. Для оценки активности обменных процессов у микроорганизмов в процессе ферментации образцов определяли электрохимические показатели.
Антимикробные свойства, пряности, фитохимические соединения, активная кислотность, титруемая кислотность, удельная электропроводность
Короткий адрес: https://sciup.org/149149264
IDR: 149149264 | УДК: 637.14.32 | DOI: 10.52231/2225-4269_2025_3_113
Analysis of antimicrobial spice property effects on the lactic acid process
The article presents the study results on the lactic acid process dynamics when cultivating the yoghurt starter microorganisms with spice extracts. Spices in their natural form as well as their extracts are used in dairy technology as food preservatives and food flavoring components. The antimicrobial properties of spices have been studied thoroughly with regard to opportunistic and pathogenic microorganisms; therefore it is relevant to study the effect of antimicrobial spice properties on the metabolic processes of various types of lactic acid microorganisms in order to identify possible inhibition of the lactic acid process. Electrochemical parameters have been determined to assess the activity of metabolic processes in microorganisms in the course of fermentation in the samples.
Текст научной статьи Исследование влияния антимикробных соединений пряностей на молочнокислый процесс
В технологии производства кисломолочных продуктов производные растительного сырья используются в качестве источников фитохимических веществ. Данные соединения проявляют антимикробные и антиокислительные свойства, а также придают молочным продуктам определенные органолептические свойства, поэтому применяются в пищевых технологиях в качестве натуральных консервантов и пищевкусовых компонентов [1].
Продукты переработки ароматического растительного сырья классифицируют как пряности, ароматические семена и травянистые растения [1, 2]. Пряности в натуральном виде и их экстракты чаще применяются в технологии молочных продуктов жидкой и пастообразной консистенции, например кисломолочных и сывороточных напитков. При производстве структурированных молочных продуктов, таких как творожные, плавленые и сычужные сыры используют в основном ароматические семена.
К пряностям относят душистый, черный, белый и стручковый перец, кассию, корицу, гвоздику, имбирь, мускатные цвет и орех, куркуму [3].
На качественный и количественный состав биологически активных веществ в растении значительное влияние оказывают его генетическое происхождениеиусловияпроизрастания,крометого,немаловажнуюроль имеют способы извлечения этих веществ из растительного сырья. Так, нативные экстракты, не подвергшиеся термообработке и воздействию процессов разделения и очистки, имеют более высокую биологическую активность за счет действия всего комплекса физиологически активных веществ растения [3, 4].
Антимикробная активность соединений из растительного сырья зависит в основном от способа получения пряностей (экстракция, сушка) и вида микроорганизмов. Соединениями, способными ингибировать микрофлору, являются терпены, алкалоиды, полифенольные соединения, а также флавоноиды, кумарины, фенольные кислоты, дубильные вещества [4, 5].
Антимикробные молекулы растений делятся на несколько классов в зависимости от их химической структуры и свойств: эфирные масла, фенольные соединения, алкалоиды, сапонины и пептиды [6]. Основные фитохимические антимикробные соединения пряностей представлены в таблице 1.
Таблица 1 – Основные фитохимические антимикробные соединения изучаемых пряностей [3–8]
|
Наименование пряности |
Основные фитохимические антимикробные соединения |
|
Куркума ( Curcuma longa ) |
Куркумен, куркуминоиды, фарнезен, фарнезол |
|
Имбирь обыкнове́нный ( Zīngiber officināle ) |
Куркумен, куркуминоиды, фарнезен, фарнезол, гингерол, шогаол |
|
Паприка ( Capsicumannuum ) |
Капсаицин, стероидные сапонины |
|
Гвоздика ( Syzygium aromaticum ) |
Эвгенол, галловая кислота, кариофиллен |
|
Корица ( Cinnamomum verum ) |
Полифенол, кумарин, эвгенол |
|
Бадьян ( Illicium verum) |
Анетол, кверцетин, кемпферол, рутин |
|
Кардамон ( Elettaria cardamomum ) |
Терпинеол и терпинилацетат лимонен, ментон, β-фелландрен, мирцен, сабинен |
|
Перец душистый ( Pimenta officinalis L. ) . |
Эвгенол, 1,8-цинеол, пинены, пара-цимен, лимонен, сесквитерпены и их производные |
|
Перец черный (Piper nigrum L. ) |
Терпены, α- и β-пинен, мирцен, α-фелландрен, лимонен, линалоол |
Флавоноиды синтезируются растениями в ответ на микробную инфекцию. По данным [9], такие флавоноиды, как апигенин, галангин, флавоновые и флавонолгликозиды, изофлавоны, флаваноны и халконы, обладают достаточно выраженной антибактериальной активностью по отношению к условно-патогенным микроорганизмам.
Количество антимикробных соединений может варьироваться в достаточно широком диапазоне. Среднее содержание фенолов (галловой кислоты) и общее содержание флавоноидов (катехина) на 100 г сырья для основных видов пряностей представлено в таблице 2 [1].
Таблица 2 – Содержание основных фитохимических соединений некоторых пряностей [1, 7]
|
Наименование пряности |
Содержание фитохимических соединений, мг/100г сырья фенолов (галловой флавоноидов кислоты) (катехина) |
|
|
Перец черный (Piper nigrum L. ) |
от 11,9 до 654 |
109 |
|
Гвоздика ( Syzygium aromaticum ) |
974 |
321 |
|
Бадьян ( Illicium verum) лат. |
819 |
277 |
|
Перец розовый ( Schinus molle L. ) |
932 |
108 |
В биотехнологии кисломолочных напитков для ферментирования молочных смесей традиционно применяются молочнокислые микроорганизмы, скорость развития которых и накопление молочной кислоты являются основными показателями, характеризующими молочнокислый процесс [10]. Биозащитный потенциал лактобактерий определяется скоростью их развития и продуцированием различных метаболитов [11], таких как молочная кислота, перекись водорода, супероксидиддисмутаза, бактериоцины и др. Данные метаболиты подавляют развитие посторонней микрофлоры, тем самым обеспечивая биозащиту готовой продукции [11]. Поэтому при разработке технологий производства кисломолочных продуктов необходимо создавать условия для наиболее активного протекания молочнокислого процесса.
Микроорганизмы образуют сложные биоценозы, при которых каждый из них находится в отношении стимулирования или угнетения со стороны других [12]. Так как антимикробные свойства пряностей по отношению к условно-патогенным и патогенным микроорганизмам достаточно изучены и доказаны [13], то актуальным является изучение влияния антимикробных свойств пряностей, применяемых при производстве молочных продуктов, на метаболические процессы различных видов молочнокислых микроорганизмов с целью выявления возможного торможения молочнокислого процесса [14].
Актуальность исследований. Изучение влияния антимикробных свойств экстрактов пряностей на консорциум микроорганизмов закваски при культивировании их в молочных средах как основы для производства кисломолочных напитков является актуальным направлением в биотехнологии.
Цель исследования – изучение антимикробных свойств пряностей, применяемых в технологиях производства молочных продуктов по отношению к заквасочной микрофлоре.
Практическая значимость состоит в возможности использовать результаты исследований при разработке технологии кисломолочных напитков с применением производных растительного сырья как источников фитохимических соединений в качестве натуральных консервантов.
Методика и методы исследования
Опыты проводили с водно-этанольными экстрактами пряностей, приготовленных из воздушно-сухого растительного сырья. Экстракцию осуществляли 70%-ным этиловым спиртом при соотношении сырья и экстрагента 1:5 настаиванием в течение 3 суток при комнатной температуре [15]. Применяли экстракты корицы, паприки и смеси пряностей для напитков. В состав смеси пряностей входят: имбирь, корица, бадьян, кардамон, перец душистый, гвоздика, перец черный. Выбор концентраций экстрактов пряностей для эксперимента обусловлен данными рецептур пищевых продуктов.
В стерильное обезжиренное молоко вносили производственную закваску для йогурта в количестве 2%. Рекомендуемая доза внесения производственной закваски составляет 3–5% [16, 17]. Количество закваски снижено в экспериментальных целях для изучения динамики молочнокислого процесса в присутствии пряностей с целью увеличения времени сквашивания. В качестве стартовых культур использовали бактериальный концентрат БК-Углич-СТБ производства «Экспериментальной биофабрики ВНИИМС», состоящий из Streptococcus thermophilus (вязкий) (StST) и Lactobacillus delbrueckii subsp. bulgari-cus (LbDB) в соотношении Тс:Пб=4:1 [18].
Далее в заквашенные образцы вносили экстракты пряностей по 0,5 мл и термостатировали при температуре 40±2 °С, оптимальной для развития йогуртовой закваски. В качестве контрольного использовали образец без внесения экстрактов пряностей.
Характер и скорость молочнокислого процесса изучали по изменению электрохимических показателей среды при культивировании молочнокислых микроорганизмов [18]. Определяли показатели, характеризующие интенсивность протекания молочнокислого процесса: активную кислотность (рН, ед.) по ГОСТ 32892-2014, титруемую кислотность (К, °Т) по ГОСТ Р 54669-2011, удельную электропроводность (УЭП, мСм/с) – кондуктометром-солемером «Эксперт-002-7» через равные промежутки времени до достижения титруемой кислотности 60 °Т (энергию кислотообразования, Эк, час), а затем измеряли эти же показатели до достижения требуемого значения титруемой кислотности для йогурта (75–80) °Т и предельной кислотности сквашенных сгустков.
Повторность опытов трехкратная. Для обработки экспериментальных данных применяли методы вариационной статистики «MicrosoftExcel».
Результаты исследований
К молочнокислым бактериям относят группу микроорганизмов, способных трансформировать углеводы до молочной кислоты как конечного продукта метаболизма, поэтому данный показатель является важным диагностическим признаком [16, 17].
Исследуемый консорциум микроорганизмов состоит из термофильного стрептококка и болгарской палочки. Streptococcus thermophilus – это отдельный вид стрептококков, способных в отличие от лактококков расти при повышенных температурах – 45°C. К основным биохимическим свойствам термофильного стрептококка относятся:
– способность сбраживать ограниченное количество углеводов (лактозу, фруктозу, сахарозу и глюкозу);
– не гидролизует аргинин;
– не ферментирует галактозу во время метаболизма лактозы;
– низкая протеолитическая активностью (является ауксотрофным по отношению к глутамину , цистеину, метионину и гистидину) [19].
Продуктыжизнедеятельности Streptococcus thermophilus оказывают позитивное воздействие на организм человека благодаря биосинтезу короткоцепочечных жирных кислот, конъюгированной линолевой кислоты, конъюгированной линоленовой кислоты; экзополисахаридов; γ-аминомасляной кислоты и других соединений [19].
При ферментации молока болгарской палочкой образуются внеклеточные полимеры-полисахариды, являющиеся углевод-белковыми комплексами, в состав углеводной части которых входят глюкоза, галактоза, рамноза, белковой части – ряд аминокислот, обеспечивающих вязкость и предотвращающих синерезис сквашенного продукта. Многим видам лактобацилл для развития необходимы витамины, например, для роста Lactobacillus bulgaricus требуется никотиновая кислота (В5), пантотенат (В3) и рибофлавин (В2) [20].
В таблицах 3, 4 и на рисунке 1 приведены электрохимические характеристики контрольного и модельных образцов, характеризующие интенсивность протекания молочнокислого процесса.
Таблица 3 – Результаты исследования электрохимических характеристик для контрольного образца и модельного образца с экстрактом корицы
|
Экспозиция, час |
Активная кислотность, ед. рН |
Удельная электропроводность, мСм/с |
||
|
Контроль |
Корица |
Контроль |
Корица |
|
|
Фон |
6,48±0,1 |
6,51±0,1 |
4,57±0,1 |
4,56±0,1 |
|
1 |
6,38±0,1 |
6,42±0,1 |
4,96±0,1 |
4,94±0,1 |
|
2 |
5,93±0,1 |
5,94±0,1 |
5,70±0,1 |
5,88±0,1 |
|
3 |
5,65±0,1 |
5,64±0,1 |
6,34±0,1 |
6,45±0,1 |
|
4 |
5,24±0,1 |
5,27±0,1 |
6,96±0,1 |
6,98±0,1 |
|
5 |
4,92±0,1 |
4,98±0,1 |
7,54±0,1 |
7,65±0,1 |
|
6 |
4,43±0,1 |
4,57±0,1 |
7,57±0,1 |
7,74±0,1 |
|
7 |
4,09±0,1 |
4,10±0,1 |
7,58±0,1 |
7,73±0,1 |
|
8 |
3,98±0,1 |
3,97±0,1 |
7,60±0,1 |
7,78±0,1 |
Таблица 4 – Результаты исследования электрохимических характеристик для модельных образцов с экстрактом паприки и экстрактом смеси пряностей
Активная кислотность, Удельная
Экспозиция, ед. рН электропроводность, мСм/с час Паприка Смесь Паприка Смесь
|
Фон |
6,47±0,1 |
6,45±0,1 |
4,58±0,1 |
4,61±0,1 |
|
1 |
6,35±0,1 |
6,31±0,1 |
4,98±0,1 |
4,97±0,1 |
|
2 |
5,92±0,1 |
5,92±0,1 |
5,90±0,1 |
5,83±0,1 |
|
3 |
5,65±0,1 |
5,66±0,1 |
6,50±0,1 |
6,41±0,1 |
|
4 |
5,36±0,1 |
5,30±0,1 |
7,04±0,1 |
7,00±0,1 |
|
5 |
4,89±0,1 |
4,93±0,1 |
7,58±0,1 |
7,64±0,1 |
|
6 |
4,44±0,1 |
4,57±0,1 |
7,61±0,1 |
7,70±0,1 |
|
7 |
4,05±0,1 |
4,10±0,1 |
7,74±0,1 |
7,74±0,1 |
|
8 |
3,99±0,1 |
3,91±0,1 |
7,80±0,1 |
7,84±0,1 |
Основными характеристиками молочнокислых микроорганизмов, применяемых в молочной отрасли, являются предельная кислотность, энергия кислотообразования и органолептические свойства сгустка [21, 22].
Как видно из данных (рисунок 1), динамика показателей у всех модельных образцов соотносится с контролем. Исследование динамики титруемой кислотности показало, что требуемое значение данного параметра (80 °Т) было достигнуто во всех образцах через 6 ч сквашивания. Несколько интенсивнее по сравнению с контро- лем молочнокислый процесс развивался в образцах с внесением экстрактов паприки и смеси пряностей – 85 °Т. Таким образом, β-галактозидазная активность консорциума заквасочных микроорганизмов не подавляется при внесении экстрактов изучаемых видов пряностей.
Значения предельной кислотности (см. рисунок ) для образцов составили: 120 °Т - контрольный образец, 122 °Т - модельный образец с экстрактом корицы, 123 °Т - модельный образец с экстрактом паприки и 125 °Т - модельный образец с экстрактом смеси пряностей для напитков, что соотносится со значением предельной кислотности для йогурта по литературным данным, которое должно находиться в
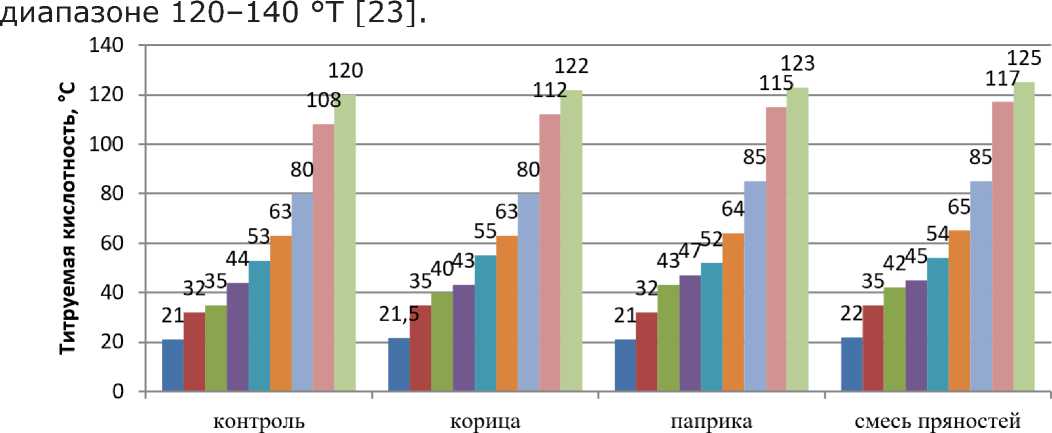
■ 0 час ■ 1 час ■ 2 час ■ 3 час ■ 4 час ■ 5 час ■ 6 час ■ 7 час ■ 8 час
Рисунок 1 – Динамика титруемой кислотности модельных образцов в процессе сквашивания
От показателя «активная кислотность» зависят: стабильность полидисперсной системы молока (термоустойчивость белков), условия роста микрофлоры, скорость образования метаболитов бактерий, активность ферментов. Данный параметр влияет на клеточный транспорт веществ, а также на скорость протекания ферментативных реакций, поэтому даже незначительные изменения рН значимо влияют на скорость роста микробных клеток [18].
Микроорганизмы также могут менять эти характеристики в процессе метаболизма для создания наиболее оптимальных условий для своего развития. На начальном этапе сквашивания активная кислотность всех образцов снижалась незначительно вследствие большой буферной емкости системы. Скорость снижения активной кислотности в первый час сквашивания составила, ед. рН: для контрольного образца – 0,10; для модельных образцов с экстрактами корицы – 0,09; паприки – 0,12; смеси пряностей – 0,14.
Далее эти показатели неуклонно снижались и практически не зависели от вида экстракта. Средняя скорость снижения активной кислотности во всех образцах была от 0,37 до 0,39 ед. рН в период от момента окончания индукционного периода до достижения значений 4,1-4,05 ед. рН, соответствующих титруемой кислотности образцов 108–117°Т. Далее наблюдали значительное снижение скорости кислотообразования и замедление молочнокислого процесса, снижение активной кислотности в единицу времени составило, ед. рН: для контрольного образца – 0,11; для модельных образцов с экстрактами корицы - 0,13; паприки - 0,06; смеси пряностей - 0,19, то есть молочная кислота подавляет рост молочнокислых бактерий.
Оценка скорости молочнокислого процесса по титруемой кислотности для окрашенных образцов молочных продуктов, например с добавлением таких пряностей как куркума, корица, паприка, имеет достаточно высокую погрешность, так как точка эквивалентности определяется визуально по изменению окраски смеси продукта с индикатором. В этих случаях необходимо применять автоматическое титрование с определением точки эквивалентности по величине рН. Также для оценки скорости молочнокислого процесса, в том числе и для окрашенных и непрозрачных сред, возможно применение кондуктометрического анализа, характеризуемого высокой точностью. Поэтому проводили измерения удельной электропроводимости (УЭП) модельных образцов в процессе сквашивания [24].
Удельная электропроводность раствора зависит от концентрации растворенных в нем низкомолекулярных веществ, УЭП молока обусловлена количеством катионов и анионов солей. Так как содержание минеральных солей в нормальном молоке колеблется в узком диапазоне 0,65-0,8%, то УЭП молока - величина постоянная [24]. В молоке присутствуют заряженные коллоидные частицы, скорость движения которых в электрическом поле зависит от отношения суммарного заряда частицы к массе. К ним относятся мицеллы казеина, а также сывороточные белки и глобулы молочного жира. В силу больших размеров и меняющегося заряда коллоидные частицы передвигаются медленно и несколько тормозят подвижность ионов, т. е. практически уменьшают электропроводность молока. Электропроводность повышается при нарастании кислотности молока, поэтому исследование динамики УЭП в процессе сквашивания образцов характеризует условия роста молочнокислых микроорганизмов [24].
Исследование динамики УЭП показало, что с увеличением количества молочной кислоты (нарастание титруемой кислотности) УЭП всех образцов увеличивается в среднем на 0,50–0,60 мСм/с до значений 7,54 мСм/с – контрольный образец, 7,65 мСм/с – образец с экстрактом корицы, 7,58 мСм/с – образец с экстрактом паприки и
7,64 мСм/с – образец с экстрактом смеси пряностей для напитков. На конечных этапах сквашивания при кислотности 80–85 °Т и выше наблюдали незначительное увеличение УЭП во всех исследуемых образцах в диапазоне 0,06-0,19 мСм/с, что связано с накоплением молочной кислоты, которая является сильным электролитом. При увеличении концентрации электролита межионное взаимодействие возрастает, что приводит к снижению скорости движения ионов и уменьшению удельной электропроводности раствора. При значении рН 4,6 образуется гелевая структура молока за счет потери устойчивости казеиновых мицелл, также повышается вязкость и усиливаются межионные взаимодействия коллоидных частиц, что также приводит к снижению электропроводности на конечном этапе сквашивания [18, 24].
Заключение
Исходя из результатов исследования, можно заключить, что экстракты корицы, паприки и смеси пряностей для напитков в исследуемых дозировках не оказывают негативного влияния на тестируемые штаммы Streptococcus thermophilus и Lactobacillus delbrueckii subsp. Bulgaricus . Таким образом, при выборе тех или иных видов пряностей в качестве пищевкусовых добавок, необходимо учитывать рекомендуемые нормативы.
Можно предположить, что отсутствие негативного влияния антимикробных веществ пряностей на молочнокислые микроорганизмы обусловлено особенностями метаболизма данных бактерий [25], например антибактериальные флавоноиды могут воздействовать на множество клеточных мишеней путем образования комплексов с белками за счет неспецифических свойств, таких как водородные связи и гидрофобные свойства, а также за счет образования ковалентных связей, то есть способ их антимикробного действия может быть связан с их способностью инактивировать микробные адгезины, ферменты, транспортные белки клеточной оболочки и так далее. Липофильные флавоноиды также могут разрушать микробные мембраны [9].
Патогенные и условно-патогенные микроорганизмы предпочитают слабощелочные и щелочные среды, а молочнокислые растут в кислых средах с низкими значениями рН от 3,5 до 4,2 единиц. В кислой и щелочной среде данные процессы протекают по-разному.
Исследование антимикробных свойств вкусо-ароматических натуральных добавок и подбор оптимальных доз и комбинаций противомикробных препаратов для разработки технологий новых видов молочных продуктов и продления сроков годности пищевых продуктов является перспективным направлением.


