Кожесохранная мастэктомия с одномоментной реконструкцией при комплексном лечении рака молочной железы с отеком кожи (cT4bN0-3M0, ycT0-4bN0-3M0)
Автор: Фокина Т.Ю., Зикиряходжаев А.Д., Волченко Н.Н., Сарибекян Э.К., Хугаева Ф.С., Максимов К.В., Дуадзе И.С., Усов Ф.Н., Кодзоева Д.Б., Захарова М.А., Замалдинов Н.Д., Занозина Е.А., Каприн А.Д.
Журнал: Вестник Российского научного центра рентгенорадиологии Минздрава России @vestnik-rncrr
Рубрика: Маммология
Статья в выпуске: 4 т.25, 2025 года.
Бесплатный доступ
Цель исследования. Улучшение качества жизни путем деэскалации хирургического лечения у больных раком молочной железы с отеком кожи (сT4b). Материалы и методы. Исследование представляет собой проспективный анализ 55 пациентов стадии cT4bN0-3M0. Всем пациентам до неоадъювантной лекарственной терапии (НАЛТ) проводили биопсию кожи молочной железы в области ареолы и проекции опухоли с целью исключения наличия раковых эмболов. Далее больные были разделены на три группы: в 1 й группе (n = 7) опухолевые эмболы в коже отсутствовали до НАЛТ и была проведена кожесохранная мастэктомия с одномоментной реконструкцией экспандером; во 2 й группе (n = 27) опухолевые эмболы в коже также отсутствовали и была выполнена мастэктомия; в 3 й группе (n = 21) были обнаружены опухолевые эмболы в коже и выполнена мастэктомия. В группах проведена сравнительная характеристика по критериям: гистологическое строение и молекулярно-биологический тип злокачественного образования, степень злокачественности (G), размер опухоли до и после лекарственного лечения, степень толщины кожи до и после НАЛТ, степень клинического ответа на НАЛТ, сроки ожидания хирургического лечения. Оценивалась частота поражения кожи молочной железы раковыми эмболами, степень клинического ответа опухоли по критериям RECIST 1.1 и динамика отека кожи, возможность выполнения кожесохранной мастэктомии с одномоментной реконструкцией экспандером, качество жизни пациенток с реконструкцией и без. Результаты. В 1 й группе полный клинический ответ в молочной железе составил 71,4%, во 2 й группе – 44,4%, в 3 й группе – 42,9%. Частичный клинический ответ в молочной железе в 1 й группе составил 28,6%, во 2 й группе 55,6%, в 3 й группе 47,6%. Отсутствие ответа на лекарственное лечение было лишь в группе с обнаруженными опухолевыми эмболами в коже и составило 9,5%. В 71,4% случаев опухолевые эмболы встречались сочетано в ареоле и в проекции кожи над опухолью. Медиана времени до проведения хирургического лечения в 1 й; во 2 й и в 3 й группе составили 32,7; 34,6; 35,2 соответственно. Заключение. Отсутствие локо-регионарного метастазирования в первой группе подтверждает возможность рассмотрения вопроса о выполнении кожесохранной мастэктомии с одномоментной реконструкцией экспандером при наличии благоприятных факторов – отсутствие раковых эмболов в коже при биопсии, купирование отека, объективный эффект на НАЛТ.
Рак молочной железы с отеком, биопсия кожи молочной железы, раковые эмболы в коже, кожесохранная мастэктомия с одномоментной реконструкцией экспандером
Короткий адрес: https://sciup.org/149150009
IDR: 149150009 | DOI: 10.24412/1999-7264-2025-4-223-237
Skin-Sparing Mastectomy with Immediate Reconstruction in the Treatment of Breast Cancer with Skin Edema (cT4b)
Purpose: To improve quality of life by de-escalating surgical treatment in patients with breast cancer presenting with skin edema (cT4b). Materials and Methods. This prospective study included 55 patients with stage cT4bN0–3M0 breast cancer. Prior to neoadjuvant systemic therapy (NAST), all patients underwent breast skin biopsy in the areolar region and over the tumor projection to exclude the presence of tumor emboli. Patients were stratified into three groups: Group 1 (n = 7), no tumor emboli detected and treated with skin-sparing mastectomy and immediate expander reconstruction, Group 2 (n = 27), no emboli detected and treated with mastectomy without reconstruction, Group 3 (n = 21), tumor emboli detected and treated with mastectomy. Comparative analysis across groups included histological and molecular subtype, tumor grade, tumor size before and after NAST, skin thickness before and after NAST, clinical response per RECIST 1.1, and time to surgery. Outcomes assessed comprised the frequency of tumor emboli in the skin, tumor response dynamics, feasibility of skin-sparing mastectomy with immediate reconstruction, and postoperative quality of life. Results. Complete clinical response in the breast was observed in 71.4% of Group 1, 44.4% of Group 2, and 42.9% of Group 3. Partial response rates were 28.6%, 55.6%, and 47.6%, respectively. Absence of response to NAST was noted only in Group 3 (9.5%). Tumor emboli were concurrently present in both the areola and the skin overlying the tumor in 71.4% of cases. Median time to surgery was 32.7 days (Group 1), 34.6 days (Group 2), and 35.2 days (Group 3). Conclusion. The absence of locoregional metastasis in Group 1 supports the feasibility of skin-sparing mastectomy with immediate expander reconstruction for selected patients who meet the following criteria: no tumor emboli on skin biopsy, resolution of skin edema, and a measurable response to NAST.
Текст научной статьи Кожесохранная мастэктомия с одномоментной реконструкцией при комплексном лечении рака молочной железы с отеком кожи (cT4bN0-3M0, ycT0-4bN0-3M0)
Рак молочной железы с отеком кожи (ОРМЖ) является наиболее агрессивной формой из злокачественных образований молочной железы. Лечение пациенток с таким диагнозом всегда носит комплексный характер и включает в себя несколько этапов: неоадъювантную лекарственную терапию (НАЛТ), хирургическое лечение и дистанционную лучевую терапию. При этом хирургический этап подразумевает удаление всей железы и регионарной клетчатки без возможности одномоментной реконструкции.
Общая 5-летняя выживаемость у пациенток с диагнозом ОРМЖ, получивших комплексное лечение, увеличилась до 70%, а 10- и 15-летняя — до 35% и 20–30% соответственно [1].
Известно, что при наличии РМЖ возможен отсев клеток рака в кожу. Чаще всего данный отсев можно обнаружить в области ареолы и в проекции опухоли на кожу.
В последние годы все чаще возникает вопрос о возможности выполнения кожесохранной мастэктомии с реконструкцией при установлении диагноза cT4b при планировании комплексного лечения. Перспектива выполнения кожесохранной мастэктомии с реконструкцией при установлении диагноза ОРМЖ напрямую зависит от наличия/отсутствия клеток рака в коже. При планировании мастэктомии данный фактор не имеет принципиального значения. Однако, при рассмотрении вопроса о реконструкции с экспандером, необходимо частичное сохранение кожи по периметру молочной железы. Нами была разработана методика диагностики наличия клеток рака в коже с гистологическим исследованием.
В 2018 году на Международном консенсусе «Программа исследований воспалительного рака молочной железы имени Моргана Уэлча» рекомендовано, кроме основных методов диагностики, рассмотреть вопрос биопсии кожи с двух участков толщиной от 2 до 8 мм из наиболее заметной области изменения цвета кожи молочной железы [2].
В исследовании, проведенном в Индии, Sharma и его коллегами были проанализированы истории болезни 111 пациенток с ОРМЖ, которые проходили лечение в период с января 2014 года по декабрь 2018 года [3]. Средний возраст пациенток на момент исследования составил 50 лет. До начала неоадъювантной полихимиотерапии (НАПХТ)
размер узлового образования в среднем достигал 7 см. После проведения патогистологического исследования средний размер образования уменьшился до 1 см. У 78 пациенток патоморфологический ответ после НАПХТ составил 50% и более, а у 43 из них — более 90%. В ходе окончательной гистопатологии у 57 (51,4%) пациенток было выявлено поражение кожи, а у 54 (48,6%) — нет. В исследовании было установлено, что у пациенток с ER-негативными опухолями и опухолями диаметром менее 1 см с большей вероятностью не наблюдалось поражения кожи (р = 0,006). Результаты этого исследования поднимают вопрос о возможности реконструктивных операций при значительном клиническом ответе при ОРМЖ.
Patel с соавторами из США провели ретроспективный анализ безрецидивной выживаемости пациенток, включенных в базу данных SEER-Medicare по неметастатическому ОРМЖ и проходивших лечение с 1991 по 2009 годы [4]. В данное исследование были включены женщины в возрасте ≥65 лет, у которых были полные данные о заболевании и проведенном лечении. Средний возраст на момент постановки диагноза составил 75,5 (диапазон 65–103) лет. В исследование были включены пациентки с различными суррогатными иммуногистохимическими подтипами, N0–N3, с проведенной тримодальной терапией, среди которых 1472 получили хирургическое лечение в объеме мастэктомии и 44 пациентки (3%) прошли одномоментную реконструкцию. Критериями отбора пациенток для одномоментной реконструкции стали более молодой возраст и низкий индекс коморбидности Чарлсона. Пациенты, перенесшие одномоментную реконструкцию молочной железы, были моложе по сравнению с теми, кто не перенес реконструкцию (в среднем 72,6 года против 75,6 лет, p = 0,008). При оценке через 1 год от окончания лечения в группе пациентов с одномоментной реконструкцией смертность от причин, связанных с РМЖ, составляла 21,1% при сравнении с группой пациентов без реконструкции — 20,9%, через 2 года показатели имели разницу — 30,7% и 32,6% соответственно. При оценке общей смертности показатели отличались значительнее: 1 год в группе с одномоментной реконструкцией 21,1%, а в группе без реконструкции — 27,9%, через 2 года показатели составили 33,1% и 43,8% соответственно. В многофакторном анализе, включающем КМЭ и значимые однофакторные показатели, КМЭ не была связана с высокой общей смертностью (ОС) (ОШ = 1,14, ДИ 0,71–1,76, p = 0,55). Независимыми предикторами ОС были возраст на момент постановки диагноза (p = 0.003), степень злокачественности опухоли (p = 0.005), отсутствие гормональных рецепторов (p < 0.001), количество пораженных лимфатических узлов (p < 0.001) и ответ на неоадъювантную химиотерапию (p = 0.006).
Низкодифференцированная/недифференцированная степень злокачественности опухоли и ER-отрицательный/PR-отрицательный статус были связаны с повышенным риском ОС. По сравнению с высокодифференцированной гистологической степенью, риск развития метастазов рака молочной железы в 3 раза выше при низкодифференцированной или недифференцированной степени злокачественности ОРМЖ (КР 3,19, ДИ 1,71–5,95, p = 0,005), а риск развития метастазов рака молочной железы в 2 раза выше при нелюминальном гормональном статусе опухоли (КР 2,01, ДИ 1,69–2,39, p = 0,0005). Таким образом, авторы пришли к выводу: поскольку продолжительность жизни населения в целом и пациентов с ОРМЖ в частности увеличивается, отказ от одномоментной реконструкции в случае инвазивного рака молочной железы с отеком кожи по историческим причинам может быть неоправданным и должен оставаться возможным вариантом при выборе объема в плане комплексного лечения [4].
В нидерландском исследовании Haarman и соавт. был проведен ретроспективный анализ историй болезни пациенток с диагнозом ОРМЖ. Сравнивалась выживаемость пациенток после проведения мастэктомии и после проведения органосохранных операций. В исследование было включено 1394 историй болезни пациенток, которые проходили комплексное лечение в 2005–2021 гг. Из них 1214 (87,1%) была выполнена мастэктомия, 180 (12,9%) — органосохранные операции. При многофакторном анализе пропорциональных рисков Кокса нет существенной разницы между мастэктомией и органосохранными 226
операциями с точки зрения общей выживаемости (ОР: 0,67, 95% ДИ 0,38-1,19, р = 0,171). В данном исследовании было показано, что органосохранные операции допустимы в плане комплексного лечения ОРМЖ [5].
С 2004 по 2015 гг. в Канаде проводилось исследование, участниками которого стали 4076 пациентов с ОРМЖ и отсутствием отдаленных метастазов. 388 (9,5%) была проведена мастэктомия с реконструкцией молочной железы и 3688 (90,5%) без неё. Средний возраст на момент постановки диагноза составил 55,1 ± 12,5 лет, средний размер опухоли составил 6,1 ± 5,0 см, у большинства пациенток были поражены регионарные лимфатические узлы (85,2%), опухоль имела высокую степень злокачественности (60,6%). Пациентки, которым была проведена немедленная реконструкция молочной железы, в среднем были моложе на момент постановки диагноза по сравнению с женщинами, которым реконструкция не проводилась (49,2 года против 55,7 лет, p < 0,0001). У этих женщин чаще был более высокий средний доход (p < 0,0001) и они чаще жили в мегаполисах (p < 0,0001). Между двумя группами не было различий в размере опухоли, её стадии, поражении регионарных лимфатических узлов, а также в статусе ER и PR. В рамках сопоставительного анализа 336 женщин, которым была выполнена немедленная реконструкция молочной железы, были сопоставлены с 1008 женщинами, которым реконструкция не проводилась. Соотношение составило 3:1. Анализ проводился на основе схожих демографических данных, характеристик опухоли и хирургического лечения. Результаты сопоставительного анализа показали, что 10-летняя выживаемость без рецидивов среди женщин, которые перенесли реконструкцию молочной железы (56,6%), и женщин, не перенесших реконструкцию (62,2%), была одинаковой (скорректированный ОР 0,96, 95% ДИ 0,79–1,16, p = 0,65). Это исследование подтвердило безопасность одномоментной реконструкции при ОПРЖ [6].
Цель исследования: у лучшение качества жизни путем деэскалации хирургического лечения у больных раком молочной железы с отеком кожи (сТ4Ь).
Материалы и методы
В период с 2023 по 2025 гг. проведено проспективное когортное контролируемое клиническое исследование на базе отделения онкологии и реконструктивно-пластической хирургии молочной железы и кожи МНИОИ им. П.А. Герцена — филиал ФГБУ «НМИЦ радиологии» Минздрава РФ.
Объектом исследования были 55 женщин, больных РМЖ стадии cT4bN0-3M0, которым до неоадъювантной лекарственной терапии (НАЛТ) проводилась биопсия кожи молочной железы из двух точек с целью исключения наличия раковых эмболов и рассмотрения возможности выполнения кожесохранной мастэктомии с одномоментной реконструкцией экспандером. Возраст больных от 31 до 79 лет. Средний возраст пациенток на момент хирургического лечения составил 51,4 ± 10,5 лет. Менструальный статус был сохранен у 53,6%, состояния менопаузы достигли 43,6% больных.
Общая когорта больных в зависимости от результата биопсии кожи была разделена на 2 группы: в 1-ю группу (N=34) вошли пациенты, у которых по результатам не обнаружены опухолевые эмболы до проведения НАЛТ. Во 2-ю группу (N=21) включены пациенты, у которых по результатам биопсии кожи были обнаружены опухолевые эмболы до проведения НАЛТ.
В общей сложности 55 пациенткам было выполнено 110 биопсий кожи из двух участков молочной железы. У 21 из них были обнаружены раковые клетки, что составило 38,2% от общего количества биопсий. В зависимости от локализации молочной железы, опухолевые эмболы были выявлены в следующих случаях: 71,4% — сочетано в ареоле и в области опухоли на коже, 19,1% — только в ареоле, 9,5% — только в области опухоли на коже (Табл. 1).
Табл. 1. Наличие раковых клеток в зависимости от места взятия биопсии
|
Локализация взятия биопсии кожи/ Skin Biopsy Site |
Количество (процент) выявленных опухолевых эмболов/ Number (%) of Detected Tumor Emboli |
|
Сочетание ареолы и кожи в проекции опухоли/Combination of areola and skin over the tumor |
15 (71,4%) |
|
Ареола/ Areola |
4 (19,1%) |
|
Кожа в проекции опухоли/ Skin over the tumor |
2 (9,5%) |
|
Всего/ Total: |
21 (100%) |
Мы провели сравнительный анализ клинико-морфологических характеристик пациентов с раковыми эмболами в коже и без них. Более подробные данные представлены в таблице 2. В первой группе наиболее часто встречались опухоли с тройным негативным подтипом (35,3%) и люминальным В, Her2/neu-негативным (35,3%). Люминальный В, Her2/neu-позитивный подтип составил 20,6%, а нелюминальный, Her2/neu-позитивный — 8,8%. Во второй группе наиболее часто встречались люминальные В, Her2/neu-негативные опухоли (57,1%), реже — тройной негативный (19,0%) и люминальный А (14,3%). При сравнении гистологических типов опухолей было выявлено, что инвазивный протоковый рак встречался у 28 (82,4%) пациентов из первой группы и у 17 (81%) из второй. Инвазивный дольковый рак наблюдался у 4 (11,8%) пациентов из первой группы и у 2 (9,5%) из второй. Другие формы встречались у 2 (5,9%) пациентов из первой группы и у 2 (9,5%) — из второй. В первой и второй группах преобладали умеренно дифференцированные опухоли (G2): 19 случаев (55,9%) и 14 случаев (66,7%), соответственно.
Табл. 2. Сравнительный анализ клинико-морфологических характеристик больных с наличием и отсутствием раковых эмболов в коже
|
Характеристики |
1-я группа /Group 1, n=34 2-я группа /Group 2, n=21 |
||
|
N |
% N |
% |
|
|
Биологический подтип /Biological subtype |
|||
|
Тройной негативный тип / Triple negative subtype |
12 |
35,3 4 |
19,0 |
|
Люминальный В Her2/neu негативный / Luminal B Her2/neu negative |
12 |
35,3 12 |
57,1 |
|
Люминальный В Her2/neu-позитивный / Luminal B Her2/neu positive |
7 |
20,6 1 |
4,8 |
|
Нелюминальный Her2/neu позитивный / Non-luminal Her2/neu positive |
3 |
8,8 1 |
4,8 |
|
Люминальный А/Luminal А |
0 |
0 3 |
14,3 |
|
Гистологический тип опухоли /Histological type of cancer |
|||
|
Инвазивный протоковый рак/Invasive ductal cancer |
28 |
82,4 17 |
81,0 |
|
Инвазивный дольковый рак/ Invasive lobular cancer |
4 |
11,8 |
2 |
9,5 |
|
Другие формы / Other types |
2 |
5,9 |
2 |
9,5 |
|
Степень злокачественности /Grade of malignancy |
||||
|
G1 |
0 |
0 |
0 |
0 |
|
G2 |
19 |
55,9 |
14 |
66,7 |
|
G3 |
15 |
44,1 |
7 |
33,3 |
Средний размер опухолевого узла во всех группах до начала НАЛТ, измеренный по максимальному диаметру, согласно данным ультразвукового исследования (УЗИ) и маммографии (ММГ), составил 40,1±8,1 мм. После НАЛТ, по данным УЗИ и маммографии, средний размер опухолевого узла снизился до 11,4±8,3 мм. Толщина кожи до и после НАЛТ (по данным ММГ) в первой группе составляла 5,5 мм и 2,8 мм соответственно. Во второй группе эти показатели были 13,6 мм и 4 мм. Размер узла до и после НАЛТ (по данным ММГ, в мм) в послеоперационном материале: в первой группе — 11,5 мм, во второй — 21,5 мм. Более подробные данные представлены в таблице 3.
Табл. 3. Динамика первичного узла и толщины кожи до и после НАЛТ
|
Характеристики |
1-я группа / Group 1, n=34 |
2-я группа / Group 2, n=21 |
|
Толщина кожи до НАЛТ (по ММГ в мм)/ Skin thickness before NAST (mammography, mm) |
5,5 |
13,6 |
|
Толщина кожи после НАЛТ (по ММГ в мм)/ Skin thickness after NAST (mammography, mm) |
2,8 |
4 |
|
Размер узла до НАЛТ (по ММГ в мм)/tumor size before NAST (mammography, mm) |
37,8 |
42,9 |
|
Размер узла после НАЛТ (по ММГ в мм)/ tumor size after NAST (mammography, mm) |
14,3 |
26,0 |
|
Размер узла в послеоперационном материале/Tumor Size in the Postoperative Specimen |
11,5 |
21,5 |
После НАЛТ специалисты оценивали, насколько уменьшилась опухоль по критериям RECIST 1.1, и наблюдали за состоянием отека кожи. Если после НАЛТ опухоль уменьшалась более чем на 50% от первоначального размера и отек полностью исчезал, то на следующем этапе лечения можно было проводить кожесохранную мастэктомию с одномоментной реконструкцией с помощью экспандера. После завершения лечения экспандер заменяли имплантатом.
В среднем период наблюдения составлял 11 месяцев, но он мог длиться от 12 до 27 месяцев. За это время в первой группе не было выявлено локальных и регионарных рецидивов. Однако во второй группе через четыре месяца после лечения у одной пациентки развился раковый лимфангоит.
Далее общая когорта больных в зависимости от результата биопсии кожи и объема хирургического вмешательства была разделена на 3 группы: в 1-ю группу (N=7) вошли пациентки, у которых по результатам биопсии кожи не обнаружены опухолевые эмболы до проведения НАЛТ и на втором этапе лечения выполнена кожесохранная мастэктомия с одномоментной реконструкцией экспандером. Во 2‑ю группу (N=27) включены пациенты, у которых по результатам биопсии кожи также не обнаружено опухолевых эмболов до проведения НАЛТ, но после проведения лекарственного лечения не был достигнут полный/частичный клинический ответ в молочной железе, либо сохранялись симптомы отека кожи, либо пациентка не желала реконструкцию. В данной группе была проведена мастэктомия. В 3‑ю группу (N=21) включены пациенты, у которых по результатам биопсии кожи были обнаружены опухолевые эмболы до проведения НАЛТ, в связи с чем данная группа расценивалась как онкологически неблагоприятная для проведения одномоментной реконструкции, и вне зависимости от клинического ответа на лекарственное лечение им была проведена мастэктомия. Процентное соотношение одномоментных реконструктивных операций и мастэктомий составило 12,7% и 87,3% соответственно. Дизайн исследования представлен на рисунке 1.
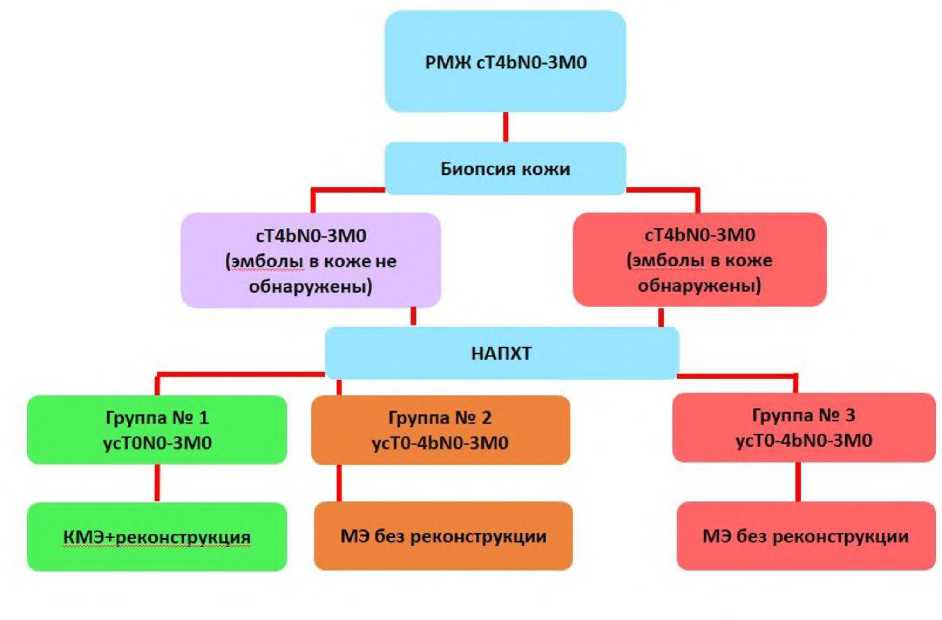
Рис. 1. Дизайн исследования.
Сравнительный анализ клинико-морфологических характеристик трех групп пациентов представлен в таблице 4. В первой группе чаще всего наблюдались опухоли с тройным негативным типом (в 57,1% случаев). Во второй группе этот тип был выявлен у 8 (29,6%) пациенток, а в третьей группе — у 4 (19,0%). Люминальный В, Her2/neu негативный подтип составил 28,6%, 37,0% и 57,1% в первой, второй и третьей группах соответственно. При сравнении гистологических типов опухоли выяснилось, что инвазивный протоковый рак встречался у всех 7 пациентов первой группы (100%), у 21 (77,8%) пациента второй группы и у 17 (81%) пациентов третьей группы. Инвазивный дольковый рак не наблюдался в первой группе, но был выявлен у 4 (14,8%) пациентов второй группы и у 2 (9,5%) пациентов третьей группы. Другие формы не были зафиксированы в первой группе, а во второй и третьей группах они наблюдались у 2 (7,4%) и 2 (9,5%), соответственно. В первой группе преобладали низкодифференцированные опухоли (G3), в то время как во второй и третьей группах чаще встречались умеренно дифференцированные опухоли (G2) (Табл. 4).
Табл. 4. Сравнительный анализ клинико-морфологических характеристик больных трех групп
|
Характеристики |
1-я группа / Group 1, n=7 |
2-я группа / Group 2, n=27 |
3-я группа / Group 3, n=21 |
|||
|
N |
% |
N |
% |
N |
% |
|
|
Биологический подтип /Biological subtype |
||||||
|
Тройной негативный тип / Triple negative subtype |
4 |
57,1 |
8 |
29,6 |
4 |
19,0 |
|
Люминальный В Her2/neu негативный / Luminal B Her2/neu negative |
2 |
28,6 |
10 |
37,0 |
12 |
57,1 |
|
Люминальный В Her2/neu позитивный / Luminal B Her2/neu positive |
1 |
14,3 |
6 |
22,2 |
1 |
4,8 |
|
Нелюминальный Her2/neu позитивный / Non-luminal Her2/neu positive |
0 |
0 |
3 |
11,2 |
1 |
4,8 |
|
Люминальный А/ Luminal А |
0 |
0 |
0 |
0 |
3 |
14,3 |
|
Степень злокачественности /Grade of malignancy |
||||||
|
G1 |
0 |
0 |
0 |
0 |
0 |
0 |
|
G2 |
3 |
42,9 |
16 |
59,3 |
14 |
66,7 |
|
G3 |
4 |
57,1 |
11 |
40,7 |
7 |
33,3 |
Средний размер опухолевого узла, измеренный по максимальному диаметру с помощью УЗИ и МРТ, во всех группах до начала НАЛТ составил 40,1±8,1 мм. После проведения НАЛТ средний размер узла уменьшился до 11,4±8,3 мм. Отек кожи, измеряемый с помощью МРТ, до начала НАЛТ в основной группе был 5 мм, а после лекарственного лечения — 1,8 мм. Во второй группе отек кожи до НАЛТ составлял 5,5 мм, а после — 3,4 мм. В третьей группе эти показатели были равны 13,6 мм и 4 мм соответственно. Размеры узла до и после НАЛТ (по данным МРТ, в миллиметрах) в послеоперационном материале: в первой группе — 32,6 мм, 0 мм и 2,4 мм соответственно; во второй группе — 37,8 мм, 14,3 мм и 11,5 мм соответственно; в третьей группе — 42,9 мм, 26,0 мм и 21,5 мм соответственно. Более детальные данные представлены в таблице 5.
Табл. 5. Динамика первичного узла и толщины кожи до и после НАЛТ в трех группах
|
Характеристики |
1-я группа / Group 1, n=7 |
2-я группа / Group 2, n=27 |
3-я группа / Group 3, n=21 |
|
Толщина кожи до НАЛТ (по ММГ в мм)/ Skin thickness before NAST (mammography, mm) |
5 |
5,5 |
13,6 |
|
Толщина кожи после |
1,8 |
3,4 |
4 |
|
НАЛТ (по ММГ в мм)/ Skin thickness after NAST (mammography, mm) |
|||
|
Размер узла до НАЛТ (по ММГ в мм)/ tumor size before NAST (mammography, mm) |
32,6 |
37,8 |
42,9 |
|
Размер узла после НАЛТ (по ММГ в мм)/ tumor size after NAST (mammography, mm) |
0 |
14,3 |
26,0 |
|
Размер узла в послеоперационном материале/ Tumor Size in the Postoperative Specimen |
2,4 |
11,5 |
21,5 |
Степень клинического ответа на НАЛТ, оцениваемая по критериям RECIST 1.1, показала, что во всех трёх группах наблюдались случаи частичного и полного клинического ответа. Однако только в третьей группе были зафиксированы два случая (9,5%) без ответа на лекарственную терапию. Ни в одной из групп не было отмечено отрицательной динамики на фоне проводимого лечения. Более подробные данные представлены в таблице 6.
Табл. 6. Характеристика степени клинического ответа на НАЛТ
|
Клинический ответ/Clinical response |
Объем хирургического лечения/ Type of Surgery Кожесохранная Мастэктомия без Мастэктомия без мастэктомия с реконструкции (не реконструкции реконструкцией обнаружены (обнаружены экспандером (не опухолевые эмболы в опухолевые эмболы в обнаружены коже)/ Mastectomy коже)/ Mastectomy опухолевые without reconstruction without reconstruction эмболы в коже)/ (no tumor emboli in the (tumor emboli in the Skin-sparing skin) (n=27) skin) (n=21) mastectomy with expander reconstruction (no tumor emboli in the skin) (n=7) |
|
сCR |
5/7 (71,4%) 12/27 (44,4%) 9/21(42,9%) |
|
cPR |
2/7 (28,6%) 15/27 (55,6%) 10/21 (47,6%) |
|
cNR |
0/7 (0%) 0/27 (0%) 2/21 (9,5%) |
|
Отрицательная динамика/progression |
0/7 (0%) 0/27 (0%) 0/21 (0%) |
В своей диссертации на тему «Стратегия хирургического лечения местнораспространённого рака молочной железы после неоадъювантной лекарственной терапии» А.В. Петровский пришёл к выводу, что увеличение интервала между НАЛТ и операцией более 42 дней может негативно сказаться на шансах достижения полного лечебного патоморфоза (ОР 0,668, p = 0,011), особенно у пациентов с люминальным иммунофенотипом. Кроме того, увеличение интервала до хирургического лечения значительно снижает показатели безрецидивной выживаемости (р = 0,015) [7]. В нашем исследовании медиана времени до хирургического вмешательства составила 34,6 дня в 232
общей популяции. В первой группе этот показатель был равен 32,7 дня, во второй — 34,6, а в третьей — 35,2. Таким образом, большинству пациенток хирургическое лечение было проведено в сроки от 4 до 6 недель в соответствии с клиническими рекомендациями. Более детальные данные представлены в таблице 7.
Табл. 7 . Сроки ожидания операции с момента окончания НАЛТ
|
Сроки |
1-я группа / Group 1, n=7 |
2-я группа / Group 2, n=27 |
3-я группа / Group 3, n=21 |
|||
|
N |
% |
N |
% |
N |
% |
|
|
Менее 4 недель/Less than 4 weeks |
3 |
42,9 |
7 |
25,9 |
6 |
28,6 |
|
От 4 до 8 недель/From 4 to 8 weeks |
3 |
42,9 |
19 |
70,4 |
13 |
61,9 |
|
От 8 и более недель/8 weeks or more |
1 |
14,2 |
1 |
3,7 |
2 |
9,5 |
При морфологическом исследовании операционного материала во всех 55 случаях не было обнаружено опухолевых клеток в краях раны. Это свидетельствует о том, что операции были выполнены радикально, независимо от выбранного метода хирургического вмешательства: кожесохранной мастэктомии или мастэктомии. После операции всем пациентам продолжали комплексное лечение в соответствии с клиническими рекомендациями Ассоциации онкологов России (АОР). Оно включало лекарственную терапию, подобранную с учетом молекулярно-биологического типа опухоли, а также дистанционную лучевую терапию на переднюю грудную стенку со стороны поражения, сформированную молочную железу и зоны регионарного лимфооттока.
Результаты
За средний период наблюдения в 11 месяцев локо-регионарных рецидивов в 1-й и во 2-й группе не отмечено. В то время как в 3-й группе через 4 месяца после лечения развился раковый лимфангоит. Появление отдаленных метастазов диагностировано у 3 пациенток: у 1 пациентки из основной группы в подвздошную кость через 14 месяцев после окончания лечения, у 1 из 1-й контрольной группы в легкое через 8 месяцев после окончания лечения, у 1 в легкое во 2-й контрольной группе через 6 месяцев после окончания лечения. У 2 пациенток из 1-й контрольной группы за время исследования наступил летальный исход, связанный с метастазированием в легкие и головной мозг. Более подробно данные приведены в таблице 8.
Табл. 8. Отдаленные результаты лечения
|
Результаты |
1-я группа / Group 1, n=7 |
2-я группа / Group 2, n=27 |
3-я группа / Group 3, n=21 |
|||
|
N |
% |
N |
% |
N |
% |
|
|
Локо-регионарный рецидив/Locoregional recurrence |
0 |
0 |
0 |
0 |
1 |
4,8 |
|
Отдаленные метастазы/Distant metastases |
1 |
14,3 |
1 |
3,7 |
1 |
4,8 |
|
Летальный исход/Death |
0 |
0 |
2 |
7,4 |
0 |
0 |
В нашей работе для оценки качества жизни мы также использовали шкалы глобального статуса жизни и здоровья из опросника EORTC QLQ-C30 V.3, который предназначен для онкологических больных. Больные из первой группы показали хорошие результаты по всем исследуемым параметрам. Эта разница между группами оказалась статистически значимой. Результаты анализа анкеты EORTC QLQ-C30 представлены в таблице 9.
Табл. 9. Показатели глобального статуса здоровья и качества жизни исследуемых больных РМЖ после хирургического лечения (EORTC QLQ-C30)
|
Показатели |
1-группа |
2-группа |
3-группа |
Р |
|
|
М 95% ДИ |
M |
95% ДИ |
M 95% ДИ |
||
|
Статус здоровья |
87 77-91 |
73 |
65-76 |
72 63-75 |
<0,05 |
|
Качество жизни |
90 86-94 |
74 |
71-78 |
75 73-79 |
<0,05 |
Заключение
Таким образом, в рамках нашего проспективного исследования, учитывая относительно небольшую выборку пациентов и ограниченный период наблюдения, мы не можем с высокой степенью достоверности оценить окончательные результаты безрецидивной и общей выживаемости. Однако предварительный анализ, проведённый при среднем периоде наблюдения в 11 месяцев, показал отсутствие локо-регионарного метастазирования в первой группе. Это позволяет рассмотреть возможность выполнения кожесохранной мастэктомии с одномоментной реконструкцией экспандером при наличии благоприятных факторов, таких как отсутствие раковых эмболов в коже при биопсии, купирование отёка и объективный эффект на лучевую терапию. Окончательные выводы будут сделаны после накопления статистически значимого количества наблюдений.
Вклад авторов. Фокина Т.Ю.: сбор и статистическая обработка данных, написание текста, Зикиряходжаев А.Д.: научное редактирование, Волченко Н.Н.: научное редактирование, Сарибекян Э.К.: научное и техническое редактирование, Хугаева Ф.С.: научное редактирование, Максимов К.В.: научное редактирование, Дуадзе И.С.: научное редактирование, Усов Ф.Н.: научное редактирование, Кодзоева Д.Б.: оформление библиографии, Захарова М.А.: сбор и обработка данных, Замалдинов Н.Д.: сбор и обработка данных, Занозина Е.А.: сбор и обработка данных, Каприн А.Д.: концепция и дизайн исследования.
Финансирование. Это исследование не получило внешнего финансирования.
Декларация по этике . Исследование было проведено в соответствии с Хельсинкской декларацией и одобрено независимым советом по этике при МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России (выписка № 1040 из протокола № 117 от 30.08. 2024).
Заявление об информированном согласии. Информированное согласие было получено от всех субъектов, участвующих в исследовании.


