Механохимическое получение пищевой добавки, содержащей витамин D и хелатированные формы кремния
Автор: Бычков А.Л., Решетникова П.А., Трофимова Е.Г., Бычкова Е.С., Ломовский О.И.
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Пищевая биотехнология
Статья в выпуске: 4 (90), 2021 года.
Бесплатный доступ
Системный дефицит витамина D и соединений кремния в организме человека приводит к многочисленным негативным последствиям прежде всего в области функционирования опорно-двигательного аппарата: даже в отсутствие недостатка соединений кальция и фосфора, которые принято считать основными костеобразующими веществами, ухудшается минерализация костей, увеличивается вероятность падений и переломов, возникают боли в мышцах. Исходя из известных механизмов физиологического действия витамина D и кремния на организм человека в данной работе сделано предположение, что пищевая добавка, содержащая холекальциферол и водорастворимые хелатированные формы кремния, будет обладать синергетическим эффектом. Было показано, что при помощи твердофазной механохимической обработки в оптимальном режиме из рисовой лузги и зеленого чая получается продукт, содержащий водорастворимые хелатированные соединения кремния с равновесной концентрацией до 24 мг/л. Оптимальным режимом, характеризующимся высокой устойчивостью к нестабильностям технологического процесса, получения из рисовой лузги и зеленого чая продукта, содержащего хелатированные соединения кремния, является скорость вращения ротора полупромышленной центробежно-роликовой мельницы-активатора RM-50 равная 1200 об./мин при скорости подачи сырья в зону обработки равной 43 кг/час. Полученный опытный образец был использован в качестве твердой матрицы - основы для нанесения холекальциферола и получения биологической активной добавки к пище. Рассчитанные количества добавки, необходимые к употреблению для восполнения суточной потребности организма в витамине D, показали целесообразность использования растворимых желатиновых капсул.
Кремний, хелатированные формы кремния, диоксид кремния, витамин d, механохимия, остеопороз
Короткий адрес: https://sciup.org/140290648
IDR: 140290648 | УДК: 664.48 | DOI: 10.20914/2310-1202-2021-4-190-196
Mechanochemical production of a food supplement containing vitamin D and chelated forms of silicon
Systemic deficiency of vitamin D and silicon compounds in the human body leads to numerous negative consequences, primarily in the field of the functioning of the musculoskeletal system: even in the absence of a lack of calcium and phosphorus compounds, which are considered to be the main bone-forming substances, bone mineralization substances, the likelihood of falls and fractures increases, muscle pain occurs. Based on the known mechanisms of the physiological action of vitamin D and silicon on the human body, it was assumed in this work that a food supplement containing cholecalciferol and water-soluble chelated forms of silicon will have a synergistic effect. It was shown that using solid-phase mechanochemical treatment in the optimal mode, a product containing water-soluble chelated silicon compounds with an equilibrium concentration of up to 24 mg / l is obtained from rice husks and green tea. The optimal mode, characterized by high resistance to instabilities of the technological process, obtaining a product containing chelated silicon compounds from rice husk and green tea, is the rotor speed of the RM-50 semi-industrial centrifugal roller mill-activator equal to 1200 rpm at a feed rate of processing area equal to 43 kg / h. The resulting prototype was used as a solid matrix - the basis for applying cholecalciferol and obtaining a biologically active food supplement. The calculated amounts of the supplement required for consumption to replenish the body's daily need for vitamin D have shown the advisability of using soluble gelatin capsules.
Текст научной статьи Механохимическое получение пищевой добавки, содержащей витамин D и хелатированные формы кремния
Адекватное потребление витамина D во многом зависит от возраста человека, сопутствующих заболеваний и использования некоторых лекарственных препаратов. Постоянный и
носящий системный характер дефицит витамина D может привести к увеличению частоты развития патологии многих органов и систем организма [1]: гипокальциемии, гиперпаратиреоза, а также гипофосфатемии, при которой ухудшается минерализация костей. Клиническими проявлениями For citation
This is an open access article distributed under the terms of the Creative Commons Attribution 4.0 International License дефицита витамина D также являются слабость и мышечная боль, не зависящая от возраста [2, 3]. Однако, функции витамина D не ограничены только контролем кальций-фосфорного обмена, он также влияет и на другие физиологические процессы в организме, например, на модуляцию клеточного роста, нервно-мышечную проводимость, воспалительные процессы. Чаще всего человек сталкивается с последствиями дефицита витамина D при затрудненной ходьбе, сложностях передвижения и поддержания равновесия, при увеличении количества падений, в том числе, сопровождающихся переломами [4, 5].
В отличие от витамина D, роль которого в организме в значительной мере изучена, количество исследований, которые указывают на важность соединений кремния как необходимого компонента для развития костной ткани, в настоящее время не столь велико. Известны работы, в которых показано, что кремний присутствует во всех тканях организма, но ткани с наибольшей концентрацией данного элемента – это кости, сухожилия и другие соединительные ткани. Исследования in vitro показали, что кремний стимулирует синтез коллагена 1 типа и дифференцировку остеобластов [6]. Исследования на лабораторных животных показали, что кремний на физиологическом уровне улучшает включение кальция в структуру кости [7, 8]. Концентрация кремния в остеоиде в 25 раз больше, чем в прилегающих областях, и содержание кремния постепенно снижается по мере роста кальцификации. Одно из объяснений этому состоит в том, что кремний делает поверхность кости более электроотрицательной, а минерализация костей происходит в электроотрицательных областях, возникающих при сжатии.
На диете без добавления кремния животные отстают в росте, у них ухудшается состояние соединительной ткани и костей [9]. Измерения массы и прочности костей на многочисленных модельных животных продемонстрировали благотворное влияние добавок кремния для увеличения плотности костной ткани и уменьшения хрупкости костей [10, 11].
Кроме того, соединения кремния могут выступать в роли доставщика биологически вышеперечисленных биологически активных соединений [12, 13]. Это связано с тем, что соединения кремния концентрируются в определенных местах – опухоли, раны, пораженные участки мышц [14].
В большинстве стран не нормируется уровень потребления и содержание кремния в продуктах питания, но были найдены суточные пограничные значения для детей и взрослых, которые составили 27 мг и 29 мг в сутки, соответственно [15, 16]. При недостаточном поступлении в организм человека (при ежедневном потреблении менее 5 мг) начинается развиваться дефицит кремния.
Наиболее перспективным возобновляемым источником биогенного диоксида кремния считается рисовая шелуха (лузга), содержащая более 20 масс.% аморфного диоксида кремния [17]. Диоксид кремния расположен на поверхности частиц рисовой шелухи и может вступать в реакции комплексообразования с природными или искусственно синтезированными молекулами, обладающими хелатными группировками [18]. С точки зрения концепции зеленой химии привлекательным сырьем выглядит биомасса (лист) зелёного чая, содержащего 8 различных катехинов, обладающих хелатными группировками [19, 20].
Поэтому целью работы стало создание комплексной добавки, содержащей несколько факторов, участвующих в остеогенезе и минерализации: витамин D и кремний в биологически доступной растворимой форме. Данные компоненты, вероятно, должны усиливать действия друг друга, как, например, витамин D и витамин K совместно участвуют в производстве и активации остеокальцина [21]. В качестве метода для проведения реакции хелатообразования была выбрана механохимическая обработка как экологически чистый, безрастворный и безотходный способ проведения реакции между твердофазными реагентами неорганической, органической и даже полимерной природы [22–24].
Материалы и методы
В работе использовались следующие материалы и реактивы: лузга риса Oryza sativa (L.) (сорт “Лидер”, Кызылординская область, Республика Казахстан), зеленый чай Camelia sinensis (L.) (ТУ 9191–003–00570186–04, Краснодарский край, Россия), водный раствор холекальцифе-рола 0.375 мг/мл (ООО «Гротеск», Россия), (NН4) 2 МоО 4 (99,5%, Россия), серная кислота (99,9%, Россия), Nа 2 SiО 3 (99%, Россия), пирокатехол (99%, Alfa Aesar), ацетат аммония (98%, Россия), аскорбиновая кислота (99%, Россия).
Определение влажности исходного сырья и продуктов переработки проводили гравиметрически по методике ГОСТ 18134–3:2015, используя автоматический анализатор влажности Radwag WPS 50SХ (Польша).
Получение хелатированного кремния проводили механохимически по технологии, широко применяемой в переработке растительного сырья [25]. Для этого смесь, состоящую из 85% рисовой лузги и 15% зеленого чая обрабатывали в полупромышленной центробежной роликовой мельнице-активаторе «RM-50» (ИХТТМ СО РАН, Новосибирск), оснащенной водяным охлаждением и блоком управления, контролирующем энергозатраты на проведение процесса [26]. Режим работы мельницы-активатора следующий: производительность 50 кг/час, скорость вращения ротора 550–1500 об./мин. Температура в зоне обработки не превышала благодаря охлаждению проточной водопроводной водой 65–70 °C. В результате получался тонкоизмельченный порошок серо-зелёного цвета, который использовали в качестве матрицы для нанесения витамина D.
Определение содержания хелатированных форм кремния в растворе проводилось следующим образом. Исследуемые образцы суспендировались в 0,05 М ацетатном буфере (гидромодуль 1000) при 25о С в течение 4 часов при постоянном перемешивании на термостатируемой магнитной мешалке. После растворения образцы центрифугировались для получения надосадочной жидкости (5000 об./мин, 15 минут). Аликвота надосадочной жидкости (350 мкл) переносилась в пластиковую пробирку, куда добавлялись 150 мкл раствора молибдата аммония (0,5 М). Спустя 10 минут (комнатная температура, без перемешивания) в пробирку добавлялись 300 мл раствора восстановителя (0,4 М раствор аскорбиновой кислоты) и 3,25 мл воды. Спустя 30 минут (комнатная температура, периодическое встряхивание пробирок) измерялась оптическая плотность растворов на длине волны 810 нм (относительно кюветы с дистиллированной водой). Концентрация хелатированных форм кремния находилась из калибровочной прямой, построенной с использованием ГСО кремния № 8934–2008 в аналогичных условиях.
Нанесение витамина D на продукт, содержащий хелатированные формы кремния проводили при комнатной температуре. Для этого к 30 г. продукта механохимической обработки, содержащего хелатированные формы кремния медленно, по каплям и при постоянном перемешивании добавляли сначала 30 мл раствора холекальциферола 0.375 мг/мл и, затем, 5 мл дистиллированной воды. Полученную влажную смесь равномерно распределяли по поддону для лиофильной сушки и замораживали при температуре -18о C. После замораживания образец сушили в лиофильной сушилке Иней-4 (Институт биологического приборостроения, Россия). Температура конденсора -47,3 °C, давление над образцом в конце процесса сушки до 0,03 мм. рт. ст. Полученный продукт, содержащий витамин D и хелатированные формы кремния, измельчали в ступке, хранили в вакуумной упаковке при температуре -18о C и использовали в последующих экспериментах. Концентрацию колекальцифе-рола определяли общепринятым хроматографическим методом [27].
Результаты и обсуждение
Наиболее важным критерием, обуславливающим успешность внедрения механохимической технологии, является энергоэффективность процесса механохимической обработки. Следует особенно тщательно подбирать режимы работы оборудования, чтобы не допускать перерасхода энергии, приводящего к излишнему разогреву материала, разложению реагентов и целевых веществ, особенно, если идёт речь о термически нестабильных молекулах биологического происхождения.
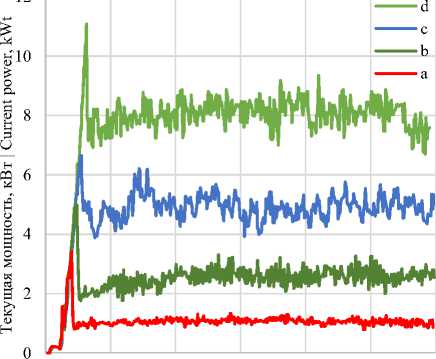
С целью контроля энергозатрат на проведение механохимического хелатирования кремния были проведены эксперименты, в которых при постоянной скорости подачи сырья с помощью высокоскоростного ватт-метра регистрировались кривые энергопотребления (рисунок 1).
0 10 20 30 40 50 60
Время, c | Time, s
Рисунок 1. Примеры кривых энергопотребления центробежно-роликовой мельницы-активатора RM-50. При различной частоте вращения ротора (a – 550 об./мин, b – 900 об./мин, c – 1200 об./мин, d – 1500 об./мин).
Figure 1. Examples of energy consumption curves of the RM-20 centrifugal roller mill-activator at different rotor speed (a – 550 rpm, b – 900 об./мин rpm, c – 1200 rpm, d – 1500 rpm)
Полученные после интегрирования кривых энергопотребления результаты показывают, что энергопотребление мельницы-активатора неравномерно зависит от частоты вращения ротора, и дальнейшая оптимизация процесса требует проведения эксперимента с различной скоростью подачи сырья (производительностью мельницы).
Таблица 1.
Зависимость скорости вращения ротора и удельных энергозатрат на проведение механохимической обработки от частоты подаваемого на двигатель электрического тока
Table 1.
Dependence of the rotor speed and specific energy consumption for mechanochemical treatment on the frequency of the electric current supplied to the motor
|
Частота электрического тока, Гц Electric current frequency, Hz |
Частота вращения ротора, об./мин Rotation frequency of the rotor, rpm |
Затраты энергии на вращение без обработки сырья, кВт Energy consumption for rotation without treatment of raw materials, kW |
Затраты энергии на вращения во время механохимической обработки сырья, кВт Energy consumption for rotation during mechanochemical treatment of raw materials, kW |
|
20 |
550 |
2,7 |
5,0 |
|
30 |
900 |
5,5 |
7,1 |
|
40 |
1200 |
9,5 |
10,3 |
|
50 |
1500 |
14,5 |
18,7 |
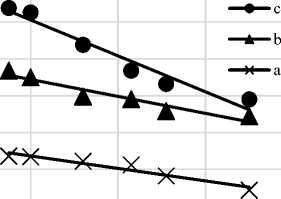
Анализ продуктов механохимической обработки рисовой шелухи, содержащей аморфный кремнезем, с биомассой зеленого чая, содержащего комплекс катехинов, приводит к существенному увеличению равновесной концентрации хелатированных форм кремния в растворе (рисунок 2).
20 40 60 80
Скорость подачи сырья, кг/час Feed rate of raw material, kg/h
Рисунок 2. Зависимость равновесной концентрации водорастворимых хелатированных форм кремния в зависимости от условий механохимической обработки (a, b, c – 900, 1200 и 1500 об./мин, соответственно)
Figure 2. Dependence of the equilibrium concentration of water-soluble chelated forms of silicon depending on the conditions of mechanochemical treatment (a, b, c – 900, 1200 and 1500rрm, respectively)
Исходя из стоимости электроэнергии, затрачиваемой на получение продукта, а также минимального наклона кривой (свидетельство стабильности протекающего процесса), оптимальным режимом получения продукта, содержащего хелатированные формы кремния, выбрана скорость вращения ротора 1200 об./мин и производительность мельницы-активатора 43 кг/час. В данных условиях получается продукт с равновесной концентрацией водорастворимых форм хелатированного кремния 24 мг/л.
В таблице 2 приведен расчёт количества добавки, необходимого к употреблению для восполнения суточной потребности организма в витамине D [28–30].
Таблица 2.
Количество пищевой добавки, необходимое для восполнения суточной потребности организма человека в витамине D
Table 2. The amount of dietary supplement required to the daily requirement of the human body for vitamin D
|
Категория населения Population category |
Суточная норма потребления витамина D, мкг Daily intake of vitamin D, μg |
Количество добавки для восполнения суточной потребности, мг The amount of supplement to replenish the daily requirement, mg |
|
Дети 4–10 лет Children 4–10 years old |
38 |
186 |
|
Дети 10–16 лет Children 10–16 years old |
50 |
245 |
|
Взрослые Adult |
15–20 |
74–99 |
|
Космонавты Cosmonauts |
100 |
490 |
Видно, что рассчитанные количества добавки удобны для применения в виде желатиновых растворимых капсул (размер капсулы № 3, ёмкость одной капсулы около 250 мг полученной добавки).
Заключение
Показано, что оптимальным режимом получения из рисовой лузги и зеленого чая продукта, содержащего хелатированные формы кремния, является скорость вращения ротора центробежно-роликовой мельницы-активатора (тип RM-50) равная 1200 об./мин при производительности 43 кг/час. Данный режим характеризуется высокой устойчивостью к нестабильностям технологического процесса и приводит к получению продукта, содержащего до 24 мг/л водорастворимых хелатированных форм кремния. Полученный продукт был использован в качестве твердой матрицы для нанесения витамина D и получения биологической активной добавки к пище. Рассчитанные количества добавки, необходимые к употреблению для восполнения суточной потребности организма в витамине D, показали целесообразность использования растворимых желатиновых капсул.
Работа была выполнена при поддержке гранта Российского научного фонда № 19–73–10074 “Энергетические аспекты механохимической переработки полимеров растительного сырья”.
Список литературы Механохимическое получение пищевой добавки, содержащей витамин D и хелатированные формы кремния
- Amrein K., Scherkl M., Hoffmann M. et al. Vitamin D deficiency 2.0: an update on the current status worldwide // European Journal of Clinical Nutrition. 2020. V. 74. P. 1498-1513. doi: 10.1038/s41430-020-0558-y
- Caballero-García A., Córdova-Martínez A., Vicente-Salar N. et al. Vitamin D, its role in recovery after muscular damage following exercise //Nutrients. 2021. V. 13. № 2336. doi: 10.3390/nul3072336
- Buruiana A., Nedeltcheva-Petrova E., Nicoleta D., Olaru M. et al. Vitamin D and extraskeletal effects // Romanian Journal of Medical Practice. 2017. V. 12. P. 33-37. doi: 10.37897/RJMP.2017.1.6
- Ling Y., Xu F., Xia X., Dai D. et al. Vitamin D supplementation reduces the risk of fall in the vitamin D deficient elderly: An updated systematic review and meta-analysis//Clinical Nutrition. 2021. V. 40. P. 5531-5537. doi: 10.1016/j.clnu.2021.09.031
- Sim M, Zhu K., Lewis J., Hodgson J. et al. Association between vitamin D status and long-term falls-related hospitalization risk in older women // Journal of the American Geriatrics Society. 2021. V. 69. P. 3114-3123. doi: 10.1111/jgs.17442
- Reffitt D.M., Ogston N., Jugdaohsingh R. et al. Orthosilicic acid stimulates collagen type 1 synthesis and osteoblastic differentiation in human osteoblast-hke cells in vitro //Bone. 2003. V. 32. P. 127-135. doi: 10.1016/s8756-3282(02)00950-x
- Hott M., de Pollak C., Modrowski D., Marie P.J. Short-term effects of organic silicon on trabecular bone in mature ovariectomizedrats//Calcified Tissue International. 1993. V. 53. P. 174-179. doi: 10.1007/BF01321834
- Giganti M., Tresoldi I., Masuelli L., Modesti A. et al. Fracture healing: From basic science to role of nutrition // Frontiers in bioscience (Landmark edition). 2014. V. 19. P. 1162-1175. doi: 10.2741/4273x
- Chappell H., Jugdaohsingh R., Powell J. Physiological silicon incorporation into bone mineral requires orthosilicic acid metabolism to Si044- // Journal of the Royal Society Interface. 2020. V. 17. doi: 10.1098/rsif.2020.0145
- Sahin K., Onderci M., Sahin N. et al. Dietary arginine silicate inositol complex improves bone mineralization in quail//Poultry Science. 2006. V. 85. P. 486-492. doi: 10.1093/ps/85.3.486.
- Kim M.H., Bae Y.J., Choi M.K., Chung Y.S. Silicon supplementation improves the bone mineral density of calcium-deficient ovariectomized rats by reducing bone resorption // Biological Trace Element Research. 2009. V. 128. P. 239-247. doi: 10.1007/sl2011-008-8273-x.
- Quintanar-Guerrero D., Ganem-Quintanar A., Nava-Arzaluz M.G., Piñón-Segundo E. Silica xerogels as pharmaceutical drug carne //Expert Opinion on Drug Delivery. 2009. V. 5. P. 485-498. doi: 10.1517/17425240902902307
- Seleem M.N., Munusamy P., Ranjan A., Alqublan H. et al. Silica-antibiotic hybrid nanoparticles for targeting intracellular pathogens //Antimicrobial Agents and Chemotherapy. 2009. V. 10. P. 4270. doi: 10.1128/AAC.00815-09
- Lu J., Liong M., Li Z., Zink J. et al. Biocompatibility, biodistribution, and drug-delivery efficiency of mesoporous silica nanoparticles for cancer therapy in animals // Small. 2010". V. 6. P. 1794-1805. doi: 10.1002/smll.2010d0538
- Jugdaohsingh R. Silicon and bone health // The Journal of Nutrition, Health and Aging. 2007. V. 11. P. 99-110.
- Rondanelli M., Faliva M., Peroni G., Gasparri C. et al. Silicon: a neglected micronutrient essential for bone health // Experimental Biology and Medicine. 2021. V. 246. P. 1500-1511. doi: 10.1177/1535370221997072
- Goodman B.A. Utilization of waste straw and husks from rice production: a review // Journal of Bioresources and Bioproducts. 2020. V. 5. P. 143-162. doi: 10.1016/j.jobab.2020.07.001
- Shapolova E., Lomovsky O. Mechanochemical solubilization of silicon dioxide with polyphenol compounds of plant origin//Russian Journal of Bioorgamc Chemistry. 2013. V. 39. P. 765-770. doi: 10.1134/S1068162012070175
- Nameyrra Z., Md Nesran Z. Shafie N. Farah S., et al. Iron chelation properties of green tea epigallocatechin-3-gallate (EGCG) in colorectal cancer cells: analysis on Tfr/Fth regulations and molecular docking // Evidence-based Complementary and Alternative Medicine. 2020. V. 2020. № 7958041. doi: 10.1155/2020/7958041
- Wang H., Wang C., Zou Y., Hu J. et al. Natural polyphenols in drug delivery systems: current status and future challenges // Giant. 2020. V. 3. № 100022. doi: 10.1016/j.giant.2020.100022
- Ushiroyama T., Ikeda A., Ueki M. Effect of continuous combined therapy with vitamin K2 and vitamin D3 on bone mineral density and coagulofibrinolysis function in postmenopausal women // Maturitas. 2002. V. 41. P. 211-221. doi: 10.1016/s0378-5122(01)00275-4
- Effaty F., Ottenwaelder X., Friscic T. Mechanochemistry in transition metal catalyzed reactions // Current Opinion in Green and Sustainable Chemistiy. 2021. V. 32. № 100524. doi: 100524. 10.1016/j.cogsc.2021.100524
- Thorpe J., O'Reilly D., Friscic T., Damha M.J. Frontispiece: mechanochemical synthesis of short DNA fragments // Chemistiy. 2020. V. 26. doi: 10.1002/chem.202084163
- Chen Y., Mellot G., Luijk D., Creton C. et al. Mechanochemical tools for polymer materials // Chemical Society Reviews. 2021. V. 50. P. 4100^140. doi: 10.1039/D0CS00940G
- Bychkov A., Podgorbunskikh E., Bychkova E., Lomovsky O. Current achievements in the mechanically pretreated conversion of plant biomass // Biotechnology and Bioengineering. 2019. V. 116. P. 1231-1244. doi: 10.1002/bit.26925
- Bychkov A.L., Buchtoyarov V.A., Lomovsky O.I. Mechanical pretreatment of corn straw in a centrifugal roller mill // Cellulose Chemistry and Technology. 2014. V. 48. P. 545-551.
- Babat N., Turkmen Y. Determination of serum vitamin D3 level by high performance liquid chromatography (HPLC) in patients with coronary artery actasia // Cardiology and Cardiovascular Medicine. 2020. V. 4. P. 097-104. doi: 10.26502/fccm.92920107
- Клинические рекомендации "Дефицит витамина D у взрослых". М.: Министерство здравоохранения Российской Федерации, 2016.
- Haimi M., Kremer R. Vitamin D deficiency/insufficiency from childhood to adulthood: Insights from a sunny country // Occupational and Environmental Medicine. 2017. V. 75. № A35. doi: 10.1136/oemed-2018-ISEEabstracts.86
- Shrivastava B., Aryan R., Tiwari A., Tiwari L. et al Comparative study of rise of vitamin D in hypovitaminosis D babies after two different dosage recommendations // International Journal of Contemporary Pediatrics. 2019. V. 6. P. 230-232. doi: 10.18203/2349-3291.ijcp20185218


