Метаболические и нейрохимические изменения в головном мозге при хроническом стрессе и его коррекции ресвератролом и сертралином, при изначально тревожном поведении
Автор: Цейликман В.Э., Шатилов В.А., Жуков М.С., Щербаков И.В., Антонова А.С., Минеева А.А.
Рубрика: Медицина
Статья в выпуске: 3 (31), 2025 года.
Бесплатный доступ
При использовании модели предаторного хронического стресса на половозрелых самцах крыс линии Wistar с изначально тревожным поведением были выявлены особенности в метаболических и нейрохимических процессах в головном мозге. Основные признаки, определяющие изначально тревожное поведение и стресс-индуцированные изменения, были выявлены по результатам поведенческого теста «Приподнятый крестообразный лабиринт» (ПКЛ). При хроническом предаторном стрессе было установлено незначительное снижение индекса тревожности, снижение концентрации серотонина миндалевидном теле и гиппокампе, а также изменения в показателях перекисного окисления липидов в тканях мозга [1; 4] (рис. 1-6). Внутрибрюшинное введении ресвератрола в концентрации 50 мг/кг привело к значительному повышению индекса тревожности, имеющего беспокойный характер, и к возвращению ряда нейрохимических и метаболических показателей до контрольных значений [8; 21]. Совместное применение сертралина с ресвератролом (10 мг/кг, 50 мг/кг, соответственно) привело к аналогичному поведенческому эффекту, но снизив иммобилизацию, при этом не изменив нейрохимические и более слабо влияя на метаболические показатели. Полученные результаты исследования представляют собой практический и теоретический интерес в рамках коррекции стресс-индуцированных нарушений при изначально тревожном поведении и изучения сравнительных механизмов действия ресвератрола и сертралина [5; 6].
Приподнятый крестообразный лабиринт, индекс тревожности, хронический предаторный стресс, тревожное поведение, ресвератрол, сертралин, серотонин, перекисное окисление липидов, нейропротекция
Короткий адрес: https://sciup.org/170211529
IDR: 170211529 | УДК: 616-092.9
Metabolic and neurochemical changes in the brain under chronic stress and its correction with resveratrol and sertraline, in initially anxious behavior
When using a model of pre-adolescent chronic stress in sexually mature male Wistar rats with initially anxious behavior, features in metabolic and neurochemical processes in the brain were revealed. The main features defining initially anxious behavior and stress-induced changes were revealed by the results of the behavioral test “Elevated plus maze” (EPM). In chronic pre-stress, a slight decrease in the anxiety index, a decrease in the concentration of serotonin in the amygdala and hippocampus, and changes in the indicators of lipid peroxidation in brain tissues were found [1; 4] (Fig. 1-6). Intraperitoneal administration of resveratrol at a concentration of 50 mg/kg led to a significant increase in the anxiety index, which had a restless nature, and to the return of a number of neurochemical and metabolic indicators to control values [8; 21]. Combined use of sertraline with resveratrol (10 mg/kg, 50 mg/kg, respectively.
Текст научной статьи Метаболические и нейрохимические изменения в головном мозге при хроническом стрессе и его коррекции ресвератролом и сертралином, при изначально тревожном поведении
Введение. В настоящее время хронический стресс представляет собой одну из наиболее актуальных проблем современной нейробиологии и психофармакологии, оказывая глубокое воздействие на структуру и функции центральной нервной системы [7; 15]. В отличие от острого стресса, который может быть адаптивным, длительное воздействие стрессорных факторов приводит к де-задаптивным изменениям в работе гипоталамо-ги-пофизарно-надпочечниковой оси и формированию патологических состояний [20].
Особенно уязвимыми к воздействию хронического стресса являются ключевые структуры мозга, включая гиппокамп и префронтальную кору, которые играют критическую роль в процессах обучения, памяти и эмоциональной регуляции [15; 18]. Нейробиологические исследования последних лет выявили, что хронический стресс индуцирует каскад патологических изменений: от нарушений нейротрансмиттерных систем до структурных пе- рестроек дендритных сетей и снижения нейрогенеза [7; 17].
Хронический стресс оказывает многофакторное повреждающее воздействие на молекулярные механизмы нейропластичности. Гиперактивация гипоталамо-гипофизарно-надпочечниковой оси приводит к избыточной продукции глюкокортикоидов, которые через геномные и негеномные механизмы подавляют экспрессию BDNF, нарушают процессы синаптогенеза и индуцируют атрофические изменения дендритного дерева [20].
Префронтальная кора и гиппокамп характеризуются наибольшей уязвимостью к стрессорным воздействиям вследствие высокой плотности глюкокортикоидных рецепторов и интенсивной метаболической активности [15]. Морфометрические исследования демонстрируют выраженные атрофические изменения в этих структурах при хронических стрессорных состояниях: укорочение и упрощение дендритного дерева, снижение плот- ности дендритных шипиков, уменьшение объема нейропиля [18].
Миндалевидное тело, напротив, обнаруживает гипертрофические изменения при хроническом стрессе, что может лежать в основе гиперактивации эмоциональных реакций и формирования тревожно-фобических расстройств [17; 18]. Дисбаланс между атрофией префронтально-гиппокампальных структур и гипертрофией амигдалы рассматривается как ключевой патогенетический механизм стресс-ассоциированных психических расстройств [7].
Метаболические изменения в мозге при хроническом стрессе характеризуются повышением активности окислительных процессов и накоплением продуктов перекисного окисления липидов [1; 2]. Параллельно наблюдается активация воспалительных процессов с участием микроглии и выбросом провоспалительных цитокинов, что усугубляет нейродегенеративные процессы [10; 19].
Нейрохимические аспекты хронического стресса включают дисбаланс моноаминергических систем, прежде всего серотонинергической, дофаминергической и норадренергической. Снижение активности серотонинергической передачи рассматривается как ключевой механизм развития депрессивных состояний и тревожных расстройств [4; 23].
В поисках эффективных методов коррекции стресс-индуцированных нарушений особое внимание привлекают природные соединения с ней-ропротекторными свойствами [8; 21]. Ресвератрол, природный полифенол, содержащийся в кожуре винограда, демонстрирует многообещающие результаты в экспериментальных моделях стресса [13; 22]. Механизмы его действия включают антиоксидантную активность, противовоспалительное действие и модуляцию сигнальных путей SIRT1 и AMPK [8; 19].
Наряду с природными соединениями, важную роль в коррекции стресс-индуцированных нарушений играют селективные ингибиторы обратного захвата серотонина (СИОЗС), среди которых сертралин занимает особое место благодаря своему благоприятному профилю безопасности и эффективности [5; 6].
Цель исследования: изучить влияние хронического стресса на метаболические и нейрохимические изменения в головном мозге у животных с изначально тревожным поведением и оценить корректирующие эффекты ресвератрола и сертралина.
Материалы и методы исследования. Исследование проведено на 20 половозрелых самцах крыс линии Wistar массой 220–280 г в возрасте 8–10 недель, полученных из питомника лабораторных животных. Для нивелирования различных половых особенностей переноса стресса исследование проводилось исключительно на самцах в летний период [16; 23]. Животные содержались в одинаковых стандартных условиях вивария при температуре 22±2°C, относительной влажности 50–65% и естественном световом режиме 12:12 ч (свет/темнота) с началом светового периода в 07:00. Крысы размещались группами по 5 особей в поликарбонат-ных клетках размером 60×40×20 см с подстилкой из древесной стружки, которая менялась дважды в неделю. Кормление осуществлялось стандартным рационом, состоящим из злаковых культур. Доступ к воде был неограниченным через автоматические поилки. За 7 дней до начала экспериментов проводили акклиматизацию животных к условиям вивария с ежедневным контролем массы тела и общего состояния.
Все процедуры, выполняемые в ходе исследования, были выполнены в соответствии с регламентом декларации ЕС от 2010 г. об использовании лабораторных животных и этическими нормами по гуманизации работы с лабораторными животными.
Дизайн исследования и формирование групп. Исходя из целей эксперимента было сформировано 4 группы животных:
1-я группа — «Контроль» (n=5), которая не подвергалась никакому стрессированию;
2-я группа — «Тревожно-фобические расстройства (ТФР)» (n=5), которая подвергалась стресси-рованию методом предаторного стресса;
3-я группа — «ТФР+Сертралин» (n=5), получавшая сертралин и ресвератрол (дозировка 10 мг/кг и 50 мг/кг, соответственно) в виде внутрибрюшинных инъекций на фоне хронического стресса;
4-я группа — «ТФР+Ресвератрол» (n=5), получавшая ресвератрол (дозировка 50 мг/кг) в виде внутрибрюшинных инъекций на фоне хронического стресса.
Воспроизведение модели хронического стрес-сирования. Стрессорный стимул в виде пропитанного кошачьей мочой абсорбирующего материала (100 мл мочи на 50 г материала) помещали в перфорированные контейнеры и размещали в домашних клетках животных. Количество кошачьей мочи и количество опилок в емкости было стан- дартизировано для обеспечения воспроизводимости результатов.
Экспозиция проводилась ежедневно в течение 10 минут на протяжении 10 суток в период с 9:00 до 11:00. Контейнеры размещали в центральной части клетки на расстоянии 15 см от углов для обеспечения равномерного распределения одоранта. После каждой экспозиции контейнеры удаляли, а клетки проветривали в течение 30 минут.
Фармакологические вмешательства. Группы «ТФР+Ресвератрол» и «ТФР+Сертралин» получали соответствующие препараты в виде внутрибрюшинных инъекций, которые начинались после периода стрессирования и продолжались в течение последующих 7 дней.
Поведенческое тестирование. Оценка поведенческой активности проводилась на 24-й день эксперимента с использованием теста «Приподнятый крестообразный лабиринт» (ПКЛ).
Установка представляла собой крестообразную конструкцию, приподнятую на высоту 60 см над полом, состоящую из двух открытых рукавов (50×10 см) и двух закрытых рукавов (50×10×40 см), соединенных центральной платформой (10×10 см). Поверхность выполнена из серого пластика с нескользящим покрытием.
Видеофиксация поведенческой активности проводилась с помощью камеры в разрешении 1080p при 60 кадрах в секунду в течение 5 минут для каждого животного.
Каждое животное помещали в центр лабиринта головой к открытому рукаву и наблюдали в течение 5 минут. Регистрировали следующие параметры:
-
• Время пребывания в открытых и закрытых рукавах (сек)
-
• Количество заходов в открытые и закрытые рукава (критерий: все четыре лапы в рукаве) (шт)
-
• Количество свешиваний (шт)
-
• Количество актов грумминга (шт)
-
• Количество выглядываний из закрытых рукавов (шт)
-
• Количество актов замирания (фризинг) продолжительностью >2 сек (шт)
-
• Общую двигательную активность (пройденная дистанция)
Рассчитывали индекс тревожности как интегральный показатель оценки состояния экспериментальных животных. Расчёт проводили по формуле: ИТ = 1 — [(время в открытых рукавах/общее время) + (заходы в открытые рукава/общее количество заходов)]/2 [22].
Забор и подготовка биологического материала. Через 24 часа после завершения поведенческого тестирования животных подвергали эвтаназии диэтиловым эфиром с последующим забором крови. Головной мозг извлекали в течение 2 минут и подвергали экстренной заморозки при -80°C, предварительно отобрав следующие структуры:
-
• Гиппокамп (полные билатеральные образцы)
-
• Префронтальную кору (области Cg1, Cg3, IL, PrL)
-
• Миндалевидное тело (центральное и базолатеральное ядра)
Оценка концентрации серотонина. Содержание серотонина определяли флюориметрическим методом с помощью «ФЛЮОРАТ-02-АБЛФ-Т» (производства Люмекс, Россия), по реакции с о-ф-талевым диальдегидом. Для исследования головного мозга использовали 10% гомогенат объѐмом 1 мл. Флюоресценцию оценивали при длинах волн 360 и 480 нм [4].
Оценка активности моноаминооксидазы. Каталитическую активность МАО определяли в митохондриальных мембранах, выделенных из головного мозга лабораторных животных. Активность МАО-Б определяли фотометрическим методом. В качестве субстрата использовали бензиламина гидрохлорид, в ходе окислительного дезаминирования образуется одна молекула бензальдегида. Для остановки реакции использовали семикарбазид на хлорной кислоте, который одновременно останавливает ферментативную активность и образует, взаимодействуя с альдегидом, соответствующие семикарбазоны. Регистрацию образовавшихся продуктов осуществляли на спектрофотометре СФ-56 («ОКБ Спектр» Россия), по поглощению при длине волны 278 нм.
МАО-активность стандартизуют по количеству белка в пробе и выражают в наномолях продукта (бензальдегида) на 1 мг белка за 1 минуту. Для определения концентрации общего белка в митохондриальных суспензиях использовали микробиуретовый метод. Для определения концентрации общего белка измерения проводили при длине волны 330 нм.
Расчёт активности производили по формуле: Акт.МАО=(dА*Uраст)/(0,012*h*min*C)
dА — полученная оптическая плотность (опыт-контроль)
U раст — объем получившегося конечного раствора h — толщина кюветы min — время инкубации
C — концентрация общего белка
0,012 — коэффициент угла наклона калибровочного графика [4].
Оценка уровня перекисного окисления липидов. Для определения уровня перекисного окисления липидов (ПОЛ) использовался спектрофотометрический метод. Данный методический подход основан на феномене перегруппировки двойных связей в диеновые коньюгаты при переокисле-нии полиненасыщенных жирных кислот, сопровождающейся появлением максимума поглощения при 230–238 нм, что позволяет судить о содержании гидроперекисей в липидном экстракте по величине его оптической плотности при этих длинах волн. Окислительная деструкция липидных гидроперекисей сопровождается появлением ещё одного максимума в спектре поглощения при 260–290 нм. В качестве экстрагента использовалась смесь гептана и изопропилового спирта, что позволило разделять липидную вытяжку на фазы различной полярности путём добавления воды. При этом верхняя (гептановая) фаза сосредотачивает большую часть триацилглицеридов (резервных липидов), в то время как водноспиртовая фаза содержит основное количество мембранных фосфолипидов (структурных липидов).
Оценка производили с помощью спектрофотометра СФ-56 Спектр, Россия. Измерение проводилась на длинах волн 220, 232 и 278. По индексам 232/220 определялись первичные продукты, по 278/220 нм вторичные продукты ПОЛ соответственно [1].
Статистическая обработка данных. Статистическую обработку проводили с использованием программных пакетов Statistica 13.05.0.17. и Past 4.06b. Нормальность распределения проверяли тестом Шапиро-Уилка. Межгрупповые сравнения проводили однофакторным дисперсионным анализом (ANOVA) с последующим апостериорным тестом Тьюки для множественных сравнений. Для анализа корреляций использовали коэффициент корреляции Спирмена. Различия считали статистически значимыми при p<0.05, при p 0,1-0,05 различия считались на уровне тенденции.
Результаты исследования
Анализ поведенческих показателей в тесте ПКЛ. Комплексная оценка поведенческой активности животных в приподнятом крестообразном лабиринте выявила значительные изменения основных параметров тревожности под воздействи- ем хронического предаторного стресса и различную эффективность фармакологической коррекции [22; 23] Индекс тревожности (И.Т.), согласно литературным данным, соответствует умеренному уровню тревожности. В группе ТФР наблюдалось снижение И.Т., однако статистически значимых различий с группой контроль обнаружено не было (рис. 1). Применение комбинации сертралина и ресвератрола способствовало повышению И.Т, достоверно превышая значения группы ТФР (p<0,05). Группа ТФР+Ресв. демонстрировала И.Т. статистически достоверное повышение показателей по отношению к группе ТФР (p<0,01).
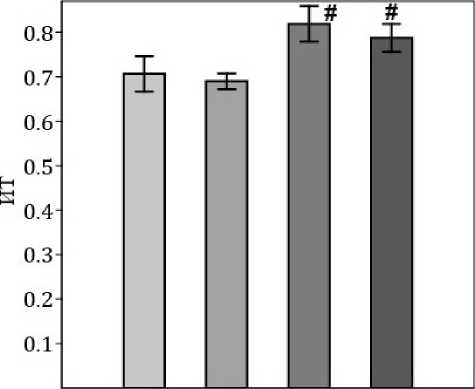
Контроль ТФР ТФР + С ТФР + Р
Рис. 1. Индекс тревожности по группам исследования. # — достоверные различия с группой ТФР
Fig. 1. Anxiety index by study group. # — significant differences with the TFR group
Наиболее выраженные изменения в количестве переходов в тёмные рукава наблюдались в группе ТФР+Ресв., что было статистически достоверно выше показателей всех остальных групп (p<0,001), свидетельствуя об активации общей двигательной активности (рис. 2).
Группа ТФР демонстрировала статистически достоверное снижение количества переходов в светлые рукава по сравнению с контрольной группой (p<0,001). Снижение данного показателя является классическим признаком повышенной тревожности. Ресвератрол частично восстановил уровень исследовательской активности, однако данная коррекция не достигла статистически значимого уровня (рис. 3).
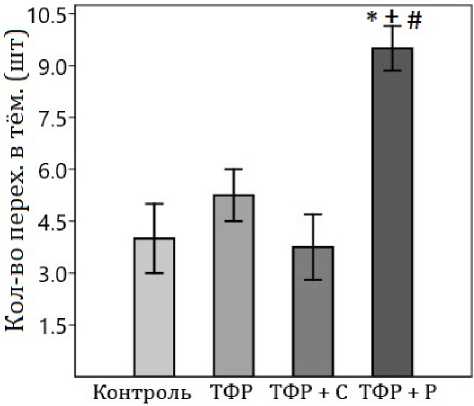
Рис. 2. Количество переходов в темные рукава по группам исследования. * — статистически достоверные различия с группой контроль; # — статистически достоверные различия с группой ТФР; + — статистически достоверные различия с группой ТФР + С
Fig. 2. Number of transitions to dark sleeves by study group. * — statistically significant differences with the control group; # — statistically significant differences with the TFR group; + — statistically significant differences with the TFR + C group
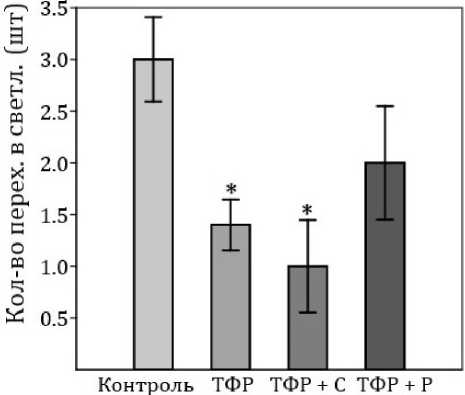
Рис. 3. Количество переходов в светлые рукава по группам исследования. * — статистически достоверные различия с группой контроль
Fig. 3. Number of transitions to light sleeves by study group. * — statistically significant differences with the control group
Нейрохимические изменения в структурах головного мозга. Анализ концентрации серотонина в различных структурах головного мозга выявил неоднородные изменения в зависимости от исследуемого региона и применяемого фармако- логического вмешательства. В префронтальной коре наблюдались наиболее выраженные изменения концентрации серотонина. В группе ТФР отмечено статистически достоверное снижение концентрации серотонина по сравнению с контрольной группой (p<0,001). Наиболее выраженный корректирующий эффект наблюдался в группе ТФР+Ресв., где концентрация серотонина составила. Сертралин в свою очередь не повлиял на данный показатель (p<0,01) (рис. 4).
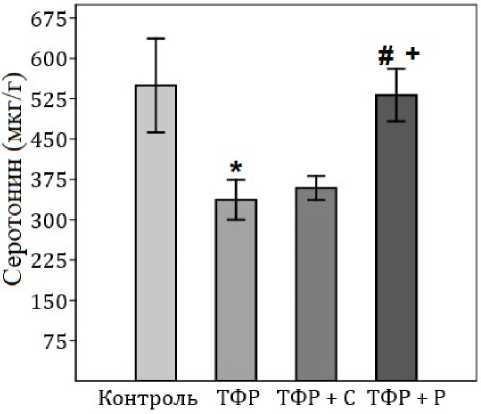
Рис. 4. Концентрация серотонина в префронтальной коре по группам исследования * — статистически достоверные различия с группой контроль;
# — статистически достоверные различия с группой ТФР; + — статистически достоверные различия с группой ТФР + С
Fig. 4. Serotonin concentration in the prefrontal cortex by study group * — statistically significant differences with the control group; # — statistically significant differences with the TFR group; + — statistically significant differences with the TFR + C group
В гиппокампе было обнаружено снижение концентрации серотонина в группах ТФР относительно контроля. Сертралин и ресвератрол, в свою очередь, не повлияли на данный показатель (рис. 5).
Моноаминооксидаза Б — это фермент, отвечающий за метаболизм моноаминов-нейротрансмиттеров, в частности серотонина, является одной из мешеней действия ресвератрола. Хронический предаторный стресс, сам по себе, не вызывал изменений в активности данного фермента. Однако терапия как сертралином, так и ресвератролом приводила к статистически достоверному повышению значений данного показателя (рис. 6.). Что согласуется с данными литературы.
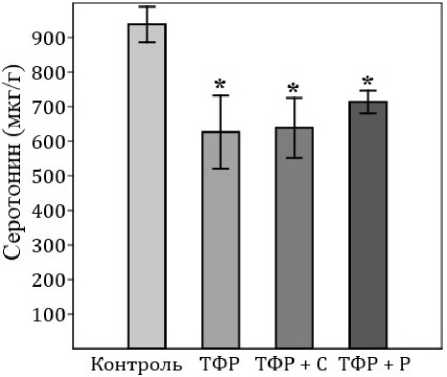
Рис. 5. Концентрация серотонина в гиппокампе по группам исследования. * — статистически достоверные различия с группой контроль
Fig. 5. Serotonin concentration in the hippocampus by study group. * — statistically significant differences with the control group
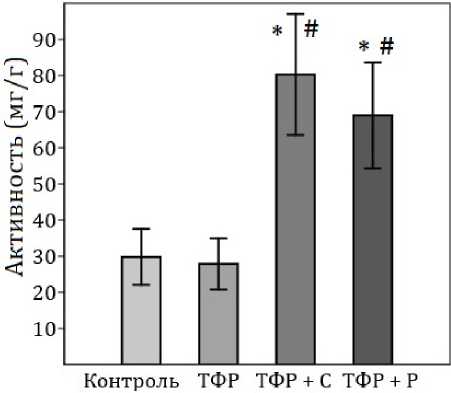
Рис. 6. Активность фермента МАО-Б в мозге мг/г* — статистически достоверные различия с группой контроль; # — статистически достоверные различия с группой ТФР
Fig. 6. MAO-B enzyme activity in the brain, mg/g* — statistically significant differences with the control group; # — statistically significant differences with the TFR group
Окислительные процессы в мозговой ткани. Исследование показателей перекисного окисления липидов в ткани головного мозга выявило значительные изменения в различных фракциях ПОЛ под воздействием хронического предаторного стресса и фармакологической коррекции.
Первичные продукты ПОЛ неструктурных компонентов (232/220 нм). Группа ТФР демонстриро- вала статистически достоверное снижение данного показателя, что может свидетельствовать об истощении липидных субстратов окисления. Сертралин, как и ресвератрол, восстанавливал данный показатель до значений группы контроля, что отражается статистически достоверным повышением по отношению к группе ТФР (рис. 7 А). Данное увеличение может быть сопряжено с усилением активности фермента МАО-Б.
В изопропиловой фазе наблюдались аналогичные тенденции: контроль (рис. 7 Б).
Вторичные продукты ПОЛ неструктурных компонентов (278/220 нм). Ресвератрол усиливал ПОЛ неструктурных компонентов в гептановой фазе (рис. 8 А).
ТФР, как и действие препаратов, не сказывались на уровне ПОЛ неструктурных компонентов в изопропиловой фазе (рис. 8 Б).
Полученные данные свидетельствуют о двухфазном характере окислительных процессов в мозговой ткани при хроническом стрессе. Снижение первичных продуктов ПОЛ в группе ТФР может отражать истощение легкоокисляемых липидных фракций на фоне длительного окислительного стресса, в то время как накопление вторичных продуктов указывает на хронический характер окислительного повреждения.
Обсуждение. Полученные результаты исследования выявили существенные метаболические и нейрохимические отклонения, связанные с поведенческой активностью, нарушениями серотонинергической передачи и окислительными процессами в головном мозге при моделировании хронического предаторного стресса у животных с изначально тревожным поведением [23; 24].
Региональная специфичность воздействия хронического предаторного стресса на серотонинергическую систему головного мозга подтверждается различной степенью выраженности изменений в префронтальной коре и амигдале [15; 18] (рис. 4, 5). Префронтальная кора демонстрировала наибольшую уязвимость к стрессорному воздействию, что согласуется с современными представлениями о роли данной структуры в регуляции эмоциональных состояний и стресс-реактивности [7; 15].
Парадоксальное снижение индекса тревожности в группе ТФР (рис. 1) может отражать развитие депрессивно-подобного поведения с элементами ан-гедонии, что часто наблюдается при длительном стрессорном воздействии [3; 6]. Это предположение подтверждается значительным снижением ис-
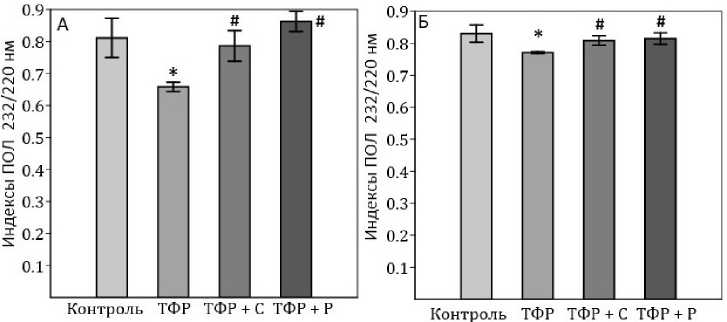
Рис. 7. Первичные продукты ПОЛ неструктурных компонентов (232/220 нм): А — гептановая фаза, Б — изопропиловая фаза. * — статистически достоверные различия с группой контроль; # — статистически достоверные различия с группой ТФР
Fig. 7. Primary products of POL of non-structural components (232/220 nm): A — heptane phase, B — isopropyl phase. * — statistically significant differences with the control group; # — statistically significant differences with the TFR group
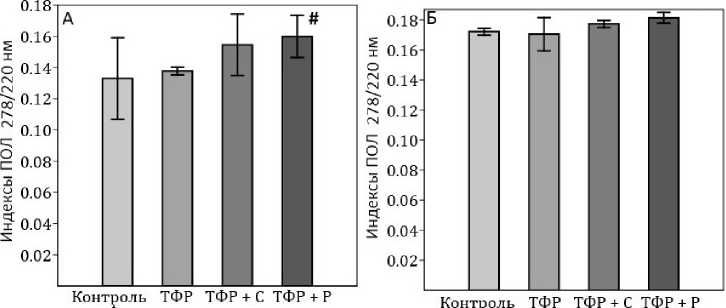
Рис. 8. Вторичные продукты ПОЛ неструктурных компонентов (278/220 нм): А — гептановая фаза, Б — изопропиловая фаза. # — статистически достоверные различия с группой ТФР
Fig. 8. Secondary products of POL of non-structural components (278/220 nm): A — heptane phase, B — isopropyl phase. # — statistically significant differences with the TFR group следовательской активности в открытых рукавах лабиринта (рис. 3) при сохранности общей локомоторной активности (рис. 2).
Двухфазный характер изменений показателей перекисного окисления липидов (рис. 6, 7) отражает сложность адаптивных процессов при хроническом стрессе [1; 2]. Снижение первичных продуктов ПОЛ может свидетельствовать об истощении липидных субстратов окисления или компенсаторной активации антиоксидантных систем, в то время как накопление вторичных продуктов указывает на хронический характер окислительного повреждения.
Сравнительный анализ эффективности фармакологической коррекции выявил преимущества ресвератрола перед сертралином в использованных дозах [8; 21]. Ресвератрол продемонстрировал комплексное нейропротекторное действие, включающее восстановление серотонинергической передачи в префронтальной коре (рис. 4), активацию общей двигательной активности (рис. 2) и частичное восстановление исследовательского поведения (рис. 3) [8; 13]. Механизмы действия ресвератрола могут включать прямое антиоксидантное действие, модуляцию сигнальных путей SIRT1 и AMPK, а также противовоспалительные эффекты [8; 19; 22].
Недостаточная эффективность сертралина в использованной дозе может быть связана с особенностями модели стресса, необходимостью более длительного курса терапии или индивидуальными особенностями серотонинергической системы у животных с изначально тревожным поведением [5; 6].
Ограничения исследования. Исследование имеет ряд ограничений, которые следует учиты- вать при интерпретации результатов. Во-первых, использование исключительно самцов не позволяет экстраполировать результаты на женскую популяцию, у которой механизмы стресс-реактивности и фармакологического ответа могут существенно различаться вследствие влияния половых гормонов [12; 16].
Во-вторых, временные рамки исследования ограничены периодом острых эффектов терапии. Долгосрочные эффекты комбинированной терапии, включая возможность предотвращения рецидивов и формирования устойчивых адаптивных изменений, требуют дополнительного изучения.
В-третьих, использованная модель хронического стресса, несмотря на высокую валидность, может не полностью отражать гетерогенность клинических проявлений тревожно-депрессивных расстройств у человека [3; 5]. Необходимы дополнительные исследования на других экспериментальных моделях для подтверждения универсальности выявленных закономерностей.
Заключение. Проведенное исследование продемонстрировало, что хронический предаторный стресс у животных с изначально тревожным поведением приводит к комплексным нарушениям нейрохимических процессов в головном мозге, характеризующимся региональной специфичностью изменений серотонинергической системы, двухфазными нарушениями процессов перекисного окисления липидов и развитием депрессивно-подобного поведения [23; 24].
Префронтальная кора является наиболее уязвимой структурой к воздействию хронического стресса, демонстрируя максимальное снижение концентрации серотонина, что коррелирует с выраженностью поведенческих нарушений [7; 15].
Ресвератрол в дозе 50 мг/кг продемонстрировал выраженные нейропротекторные эффекты, превосходящие по эффективности сертралин в аналогичной дозе [8; 21]. Механизмы действия ресвератрола включают восстановление серотонинергической передачи, нормализацию показателей перекисного окисления липидов и улучшение поведенческих параметров [8; 13; 22].
Полученные результаты открывают перспективы для разработки новых терапевтических подходов к коррекции стресс-индуцированных нарушений на основе природных соединений с нейропро-текторными свойствами и обосновывают целесообразность дальнейших исследований ресвератрола как потенциального антидепрессанта и анксиолитика [8; 21; 22].


