Мезенхимные стромальные клетки костного мозга и их роль в формировании опухолевой ниши при онкогематологических заболеваниях
Автор: Чубарь А. В., Семенова Н. Ю., Ругаль В. И., Бессмельцев С. С., Котова А. В., Масленникова И. И., Иволгин Д. А., Енукашвили Н. И.
Журнал: Вестник гематологии @bulletin-of-hematology
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.15, 2019 года.
Бесплатный доступ
Мезенхимные стромальные клетки (МСК) являются одними из ключевых компонентов ниши гемопоэтической стволовой клетки. Несмотря на многочисленные исследования, посвящённые фенотипу и дифференцировке МСК в костном мозге (КМ), данные об их функционировании в организме ограничены. Функциональная пластичность этих клеток находит применение в терапии. Особый интерес МСК КМ представляют в связи с их ролью в развитии гематологических заболеваний. В обзоре рассматриваются фенотипические особенности МСК КМ, вопросы их гетерогенности и иерархии, а также их роль в формировании опухолевого микроокружения.
Мезенхимные стромальные клетки, костный мозг, микроокружение, ниша гемопоэтических стволовых клеток
Короткий адрес: https://sciup.org/170172531
IDR: 170172531
Bone marrow mesenchymal stromal cells and their role in forming tumor microenvironment of oncohematological diseases
Mesenchymal stromal cells are one of the main components of hemopoietic niche. Despite numerous studies on the phenotype and differentiation of MSCs in the bone marrow (BM), our knowledge on their functioning in vivo especially on the MSC role in tumor microenvironment is limited. The phenotypic characteristics of MSC CM, issues of their heterogeneity and hierarchy, as well as their role in the formation of the tumor microenvironment are discussed.
Текст обзорной статьи Мезенхимные стромальные клетки костного мозга и их роль в формировании опухолевой ниши при онкогематологических заболеваниях
колонии на культуральном пластике и обладали способностью к дифференцировке в хондрогенном и остеогенном направлениях. В 1991 году Каплан предложил термин «мезенхимные стволовые клетки» для МСК, дающих начало различным клеткам мезодермального происхождения и способных к самообновлению [2]. В 2005 году Междуна- родное общество клеточной терапии (МОКТ, ISCT — The International Society for Cellular Therapy) предложило называть такие клетки мультипотентными мезенхимными стромальными клетками (мМСК), так как лишь часть популяции соответствует критериям истинных стволовых клеток [3, 4]. Простота выделения и культивирования, способность к дифференцировке в различных направле-ниях,синтез различных биологически активных веществ открыли большие возможности к использованию МСК в регенеративной терапии. Однако на сегодняшний день большая часть информации об МСК была получена in vitro, а представление о функционировании и особенностях этих клеток in vivo весьма ограничено. Кроме того,сравнение результа-тов,полученных в разных экспериментах,ос-ложняется гетерогенностью популяции МСК костного мозга (МСК КМ), внутри которой можно выделить как клетки с характеристиками стволовых, так и клетки, вставшие на путь дифференцировки. В настоящем обзоре рассматриваются данные о происхождении, гетерогенности и фенотипе МСК КМ.
Распространение МСК
В 2006 году МОКТ представило критерии, определяющие МСК: 1) адгезия к культуральному пластику 2) определённый фенотип: CD105+, CD73+ и CD90+, CD45–, CD34–, CD14–, CD11b–, CD79–, CD19- и HLA-DR- 3) способность к дифференцировке in vitro в остеобласты, хондроциты и адипоциты [4]. Однако такое определение оказалось достаточно широким. Помимо КМ,МСК могут быть выделены из множества других органов и тканей, включая жировую ткань, пупочный канатик, периферическую кровь, сердце, лёгкие [5,6]. Все эти клетки соответствуют принятым критериям МСК. Для объяснения практически повсеместного нахождения МСК существует три предположения: 1) МСК развиваются в каждом органе или ткани независимо 2) МСК связаны с определёнными тканями,но способны циркулировать посредством кровеносного русла в другие органы и ткани 3) МСК — это циркулирующие клетки крови [7]. Стоит отметить, что несмотря на общую схожесть, МСК разных органов и тканей имеют различия,об-условленные влиянием локальной ниши [8]. Owen в работе 1988 года [9] предполагал, что
МСК КМ являются частью всех стромальных клеток организма, вписываясь в иерархическую модель, в основе которой находятся плюрипотентные стволовые клетки, дающие начало тканеспецифичным стволовым клеткам уже с ограниченными потенциями,в том числе МСК КМ,которые,в свою очередь,дают начало коммитированным предшественникам. Такие предшественники будут дифференцироваться в конкретные типы стромальных клеток в зависимости от действия ниши. Схема дифференцировки МСК КМ с тех пор изменилась благодаря новым данным, а повсеместное распространение МСК связывается с их периваскулярной локализацией [10–13].
Что касается циркуляции МСК, то хотя их можно выделить из периферической крови, вопросы вызывает характер этого явления — временный или постоянный [14]. Показано многократное увеличение числа МСК в крови крыс в условиях гипоксического стресса [15]. В условиях in vitro гипоксия индуцирует про-лиферацию,миграцию и проангиогенный эффект МСК КМ,что отражает возможную роль МСК в микроокружении опухоли, для которого характерна пониженная концентрация кислорода [16, 17].
Фенотип МСК
Одним из ключевых вопросов литературы о МСК является вопрос о том,как данные,по-лученные in vitro, соотносятся с условиями in vivo. Фенотип МСК КМ неоднороден и изменяется в культуре, что не позволяет с уверенностью утверждать, что в организме эти клетки экспрессируют те же маркеры и с той же интенсивностью [18,19]. Набор антигенов, предложенный МОКТ для определения МСК,не является специфическим только для именно стволовых клеток, в эту же популяцию попадают и стромальные клетки. В связи с этим ведётся активный поиск других маркеров МСК, среди которых CD271 [20], SCA-1 (МСК антиген-1), Stro-1, молекулы интегри-нов CD49a, CD51, CD146 [21–25]. Однако эти маркеры также могут присутствовать на поверхности других клеток (Stro-1, к примеру, экспрессируют эритробласты [26]), поэтому более надёжным представляется использование их в комбинации с другими положительными и отрицательными маркерами панели, предложенной МОКТ в 2006 г.
Основная часть МСК КМ не окрашивается маркерами плюрипотентных клеток. Однако с использованием маркеров плюрипотентных клеток, в том числе SSEA-4, Oct4 и Nanog, все же было выделено несколько популяций МСК, обладающих свойствами плюрипотентности (способность давать производные всех зародышевых листков, то есть эктодермы, мезодермы и энтодермы): APC, IA I, use [27–29] и другие.
IA I (от marrow-isolated adult multilineage inducible cells, индуцибельные взрослые клетки костного мозга с мульти-линейным потенциалом) были получены при культивировании на фибронектине и в условиях пониженной концентрации кислорода. Для этих клеток характерна дифференцировка в нервные клетки (производные эктодермы)и панкреатические клетки (производные энтодермы) в соответствующих условиях [27].
use (multilineage differentiating stress enduring, устойчивые к стрессу с мультили-нейным потенциалом дифференцировки) — субпопуляция клеток, среди особенностей которых можно выделить устойчивость к стрессовым воздействиям,низкую скорость пролиферации и образование М-кластеров, подобных кластерам эмбриональных стволовых клеток. use были выделены как из аспирата КМ, так и из культур фибробластов кожи человека [28].
Субпопуляция APC (multipotent adult progenitor cells, мультипотентные взрослые прогениторные клетки)— это очень небольшая популяция в составе пула МСК, состоящая из быстро делящихся клеток,способных давать начало клеткам трёх зародышевых листков, в том числе при инъекциях в раннюю бластоцисту [29].
В отличие от описанных субпопуляций, обладающих свойствами плюрипотентных клеток, PC (mesodermal progenitors cells, мезодермальные прогениторные клетки) дают начало только производным мезодермы (мезенхимным и эндотелиальным клеткам), то есть обладают свойством мультипотент-ности. Клетки этой субпопуляции по некоторым данным экспрессировали Oct-4, Nanog, SSEA-4, а также обладали альдегиддегидроге-назной активностью, характерной для гематопоэтических предшественников,но не зрелых МСК). PC способны к дифференцировке в МСК и эндотелий,причём полученные МСК не могут быть обратно дифференцированы в PC [30].
Таким образом, в популяции МСК КМ содержатся клетки с признаками плюрипотентности, однако их количество крайне малое, поэтому, в целом, МСК КМ являются мульти-потентными клетками, не способными давать производные энтодермы и эктодермы. Что касается вышеописанных субпопуляций МСК КМ с маркерами плюрипотентности, разобщённость полученных данных не даёт возможности соотнести эти субпопуляции друг с другом или чётко обозначить их взаимосвязь в линии развития МСК.
Показано существование стволовых клеток с мезенхимным фенотипом, но другого эмбрионального происхождения: например, стволовые клетки нервного гребня [31,32]. Для части клеток нервного гребня показана миогенная дифференцировка, индуцированная определёнными условиями культивирования [33]. В настоящий момент её возможность in vivo остаётся сомнительной, к тому же ей противоречит тот факт,что миогенное и остеогенное направление дифференцировки разделяются ещё в эмбриогенезе [34]. Однако показано,что гингивиальные фибробласты (одна из разновидностей МСК) способны к дифференцировке в миогенные фибриллы [35]. На сегодняшний день существуют протоколы дифференцировки МСК как КМ, так и других органов, в другие типы клеток, включая кардиомиоциты [36,37], нейроны [38], гепатоциты [39], клетки поджелудочной железы [40]. Таким образом, МСК являются очень пластичными клетками,а направление их дифференцировки определяется локальной концентрацией специфических факторов.
Гетерогенность МСК КМ в зависимости от условий культивирования
Гетерогенность МСК КМ была описана достаточно рано. В работе 1981 года авторы описывали морфологическое различие МСК в культуре и выявили два типа клеток: клетки 1 типа имели фибробластоподобную мор-фологию,активно делились и давали начало клеткам 2 типа. Клетки 2 типа были крупными, плоскими и имели эпителиоподобную форму. 1 тип обозначили как быстро обновляющиеся клетки, а 2 — как зрелые МСК [41]. Гетерогенность культивированных МСК КМ связывается с множеством факторов, среди которых техника получения, плотность высевания, время культивирования, состав сред и сывороток, а также различия между донорами [42–45]. Именно способ получения МСК КМ,а не пол или возраст считается определяющим различия культур, так как показана неоднородность материала из двух аспиратов одного донора,взятых в один момент времени [46,47]. В работе по изучению способности к остеогенной дифференцировкt МСК КМ здоровых доноров способность формировать кость in vivo терялась уже на 1–3 пассажах у разных доноров, при этом активность щелочной фосфатазы,как маркера остеогенной дифференцировки, не изменялась значительно, зато была отмечена разница в скорости пролиферации [48].
Различие по таким базовым характери-стикам,как размер,потенциал к остеогенной дифференцировке, форма клеток, способность к адгезии,наблюдается не только между клетками одной культуры МСК, но и внутри колонии, состоящей из потомков одной клетки, то есть КОЕф (или клон) [49]. Owen, описывая КОЕф,выделяет клетки с высоким потенциалом к самообновлению и мультипо-тентной дифференцировке и клетки с ограничением этих характеристик [9]. В качестве причин такой внутриклональной гетерогенности в настоящее время указываются спонтанная дифференцировка [47], высокая плотность клеток в колонии [51], длина теломер [50], возможное возникновение мутаций [52]. Для колоний МСК может быть характерна обратимая дифференцировка в центральной области колонии, где в сравнении с периферическими клетки слабее экспрессируют гены регуляции клеточного цикла и активнее — внеклеточного матрикса [53]. Если изменчивость внутри культуры МСК КМ можно объяснить наличием различных субпопуляций из более и менее коммитированных предшественников, то причины внутриклональной изменчивости требуют дальнейшего изучения, в том числе в целях практического применения МСК. Для обхода стадии культивирования МСК в некоторых исследованиях используется метод флуоресцентного сортинга, недостатком которого можно считать гораздо меньшее количество получаемого материала, достаточное только для небольших экспериментальных работ [54, 55].
Различие МСК по способности к дифференцировке
По отношению к дифференцировке клоны МСК КМ могут быть трипотентными, бипо-тентными и унипотентными. Ранее обсуждалась линейная модель дифференцировки МСК КМ, в которой трипотентные клетки постепенно теряли способность к адипоген-ной и хондрогенной дифференцировке, превращаясь в остеопрогениторные клетки [10]. В другой работе, исследовавшей дифференцировку клонов МСК КМ, выявлялись иные бипотентные предшественники, кроме остео-хондрогенных, а также унипотентные хондрогенные и адипогенные клоны. Интересно, что при этом наиболее часто встречающимися клонами были трипотентные, остео-хондрогенные и остеогенные. Фракция трипотентных МСК КМ состояла из быстро делящихся клеток, активно экспрессирующих CD146. Самым редким типом ожидаемо оказался адипогенно-хондрогенный предшественник, что позволяет сделать выводы о влиянии локальной ниши, факторы которой определяют направление дифференцировки мультипотентного предшественника [11]. Однако описаны случаи длительного (более полугода) непрерывного культивирования без утраты способности к дифференцировке в трёх направлениях [56].
Происхождение и периваскулярный характер расположения МСК
По локализации в КМ МСК можно разделить на периваскулярные (большинство) и находящиеся в районе эндоста. Такое расположение при этом соответствует распределению CD146: высокий уровень экспрессии наблюдается в МСК вблизи сосудов, а низкий уровень или отсутствие экспрессии во второй группе клеток. Обе группы при этом объединяла экспрессия CD271 и контакт с CD34+ГСК [57]. Периваскулярное расположение МСК позволяет объяснить повсеместное расположение МСК в организме. Так как помимо МСК в контакте с сосудами находятся перициты и адвентициальные клетки, исследователей заинтересовал вопрос о взаимосвязи всех трёх типов клеток. Исходя из данных литературы, всю совокупность взглядов можно свести к нескольким предположениям: 1)
МСК — это перициты [58] 2) Перициты — это предшественники МСК [59] 2) МСК — это адвентициальные клетки [60, 61] 3) Адвентициальные клетки — это предшественники перицитов, а перициты это предшественники МСК [62] 4) МСК — это не перициты и не адвентициальные клетки, а отдельный тип клеток [7]. Ввиду наличия фактов, подтверждающих каждую из приведённых гипотез, можно предположить, что внутри МСК можно выделить достаточно пластичные субпопуляции, иерархия и взаимоотношения которых требуют дальнейшего прояснения.
В пользу идентичности МСК и перицитов или адвентициальных клеток говорит наличие общих маркеров и способность дифференцироваться при индукции в трёх направлениях. Адвентициальные клетки также экспрессируют CD271, CD146, способны к мультипотентной дифференцировке [60]. При добавлении в культуральную среду ан-гиопоэтина-2 в адвентициальных клетках усиливается экспрессия генов маркеров перицитов, что позволило предположить их дифференцировку в перициты [63].
Перициты так же, как и МСК, способны к дифференцировке в трёх направлениях, имели сходный иммунофенотипический профиль CD146+/CD34-/CD-45–/CD56– [64]. Перициты и МСК демонстрируют сходный характер экспрессии генов, отличающий их от фибробластов [65]. Тем не менее, некоторые авторы, использующие мышиные модели, отвергают тождественность МСК и перицитов из-за недостаточной пластичности послед-них:перициты сохраняют свои свойства даже при индукции дифференцировки [66]. Как маркер, отличающий перициты и МСК, был предложен десмин,который в КМ синтезируют гладко-мышечные клетки, но не МСК [62]. Интересным представляется вопрос о взаимосвязи перицитов и группы МСК, расположенных в эндосте и отличающихся от периваскулярной фракции.
Другое направление исследований, касаю-щихсяМСК,связаноспоискомраннегообщего предшественника мезенхимных и эндотелиальных клеток. В качестве таковых описаны мезоангиобласт из эмбриональной аорты и мезенхимоангиобласт, полученный с помощью эмбриональных стволовых клеток. Мезоангиобласты — это стволовые клетки, ассоциированные с сосудами, участвующие в постнатальном формировании тканей мезодермы [67]. Мезенхимоангиобласт в культуре образует мезенхимные клетки с промежуточной эндотелиальной стадией, причём при определённых условиях можно получить три направления дифференцировки: МСК, перициты и гладко-мышечные клетки (Рисунок 1) [68].
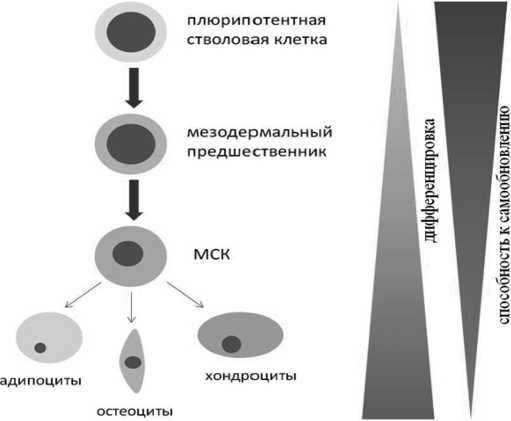
Рисунок 1. Схема дифференцировки МСК.
Исследования последних лет обращаются к идее ангиогенного происхождения МСК, что подтверждается удачными опытами дифференцировки МСК в эндотелиальные клетки и обнаружением маркеров эндотелия, таких как CD31, CD34, рецептор к фактору роста эндотелия сосудов (VEGF), фактор фон Виллебранда [7]. В то же время дифференцировка МСК в условиях культуры может не вызывать повышения экспрессии маркеров эндотелия, поэтому существование такого пути in vivo вызывает сомнения [56, 69].
В качестве источника части пула МСК рассматривается нейроэктодерма, так как МСК экспрессируют рецептор к фактору роста нейронов [70]. В настоящее время интенсивно изучаются стволовые клетки нервного гребня, приобретающие мезенхимный фенотип и участвующие в эмбриогенезе в формировании всех органов и тканей головы и шеи, а также участвующие в формировании миокарда [71].
Роль МСК в формировании опухолевого микроокружения
В настоящее время всё большее внимание уделяется вопросу о роли ниши костного мозга (КМ) в опухолеобразовании и развитии ранних рецидивов [72]. Если основной функцией МСК в здоровом КМ является поддержка гемопоэза,то при взаимодействии с раковыми клетками изменяется как фенотип,так и функции МСК — они начинают поддерживать рост опухоли и обеспечивают защиту от иммунной системы (Рисунок 2) [73–75].
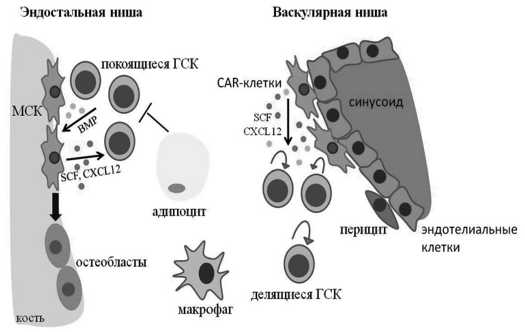
Рисунок 2. Схематическое строение гемопоэтической ниши костного мозга.
Например, при остром миелоидном лейкозе (ОМЛ) показано снижение экспрессии таких генов, как Cxcl12, Angptl1, необходимых в поддержке ГСК [76]. Сокультивирова-ние бластов от больных ОМЛ с МСК здоровых доноров повысило выживаемость бластных клеток в присутствии цитарабина, причём ключевуюроль вэтомигралипрямые контакты между клетками [77]. В культурах МСК КМ, полученных от больных множественной миеломой (ММ), наблюдался фенотип стареющих клеток, характеризующийся увеличением размера клеток,активным синтезом ассоциированной со старением β-галактозидазы, снижением способности к пролиферации и остеогенной дифференцировке [75, 78, 79]. Под действием опухолевых клеток МСК могут дифференцироваться в опухоль-ассоцииро-ванные фибробласты (ОАФ). МСК и ОАФ имеют сходный фенотип и набор синтезируемых цитокинов. Отличие ОАФ в резком повышении уровня синтеза таких молекул, как VEGF и интерлейкин-10, а также в экспрессии та- ких маркеров, как гладко-мышечный актин, десмин,рецептор к фактору роста тромбоцитов (PDGF) [80,81]. ОАФ также поддерживают рост опухоли,а их появление может быть признаком ухудшения прогноза лечения.
Взаимодействие МСК КМ с опухолью может осуществлятьсячерез прямые межклеточные контакты и посредством выделения цитокинов и экзосом,содержащих различные белки и РНК [82,83]. Считается, что, как и в случае нормального гемопоэза, при взаимодействии с раковыми клетками главной особенностью МСК КМ является синтез специфических цитокинов, преобразующих микроокружение и выделяемых под контролем раковых клеток [84,85]. Так, при ММ одним из ключевых факторов, индуцирующим рост опухоли, является интерлейкин-6 (ИЛ-6), который выделяется МСК КМ под действием фактора FGF-β, который в свою очередь синтезируют клетки ММ при контакте с ИЛ-6 [86].
Другими особенностями МСК КМ, благоприятными для развития опухоли, являются их проангиогенный эффект и иммуносупрессивные свойства, позволяющие раковым клеткам избегать реакций иммунной системы. МСК КМ оказывают влияние на пролиферацию Т и В-клеток, могут ингибировать активацию дендритных клеток [87]. Хотя для очага опухоли характерны условия гипоксии, в КМ при этом можно наблюдать повышенную васкуляризацию, кроме того, КМ считается привлекательным для заселения раковыми клетками в том числе в связи с большим количеством сосудов [88]. Для МСК КМ при этом характерно повышение уровня синтеза таких проангиогенных молекул, как VEGF, фактор роста фибробластов-β (FGF-β) и трансформирующий ростовой фактор-β (TGF-β). Плотность сосудов в очаге опухоли считается одним из прогностических факторов, определяющих исход лечения [89]. При ММ VEGF индуцирует повышение экспрессии в миеломных клетках нескольких протоонкогенов [90]. Поэтому существует необходимость в разработке препаратов, нацеленных на ограничение сосудообразования в опухоли. МСК КМ могут являться одной из мишеней подобного лечения [74].
МСК опухоли отличаются от здоровых доноров не только фенотипически, но и генетически. В работе по изучению генома МСК КМ больных ММ выявлялись участки с повышенной мутабельностью, где можно предпо- ложить наличие генов,важных в прогрессии заболевания. При этом мутации МСК необязательно идентичны таковым в опухолевых клетках [91]. Другой причиной гематологических заболеваний может быть экспрессия эндогенных ретровирусов, представляющих из себя не кодирующие последовательности генома и в норме молчащие [92,93]. Активация транскрипции таких областей показана при разных видах рака,в том числе лейкемии, где наблюдалось повышение экспрессии последовательности HERV-K [94].
МСК КМ могут играть роль на разных стадиях развития опухоли [95,96]. Концепция преметастатической ниши предполагает, что ниша специфически изменяется ещё до появления опухолевых клеток за счёт сигналов, попадающих в КМ [97,98]. На ранних стадиях возникновение и рост опухоли могут быть связаны с уже имеющимся нарушением гемопоэза или поддержкой мутантного клона,ко-торый может иметь некое конкурентное преимущество, причины которого пока неясны. Существует предположение,что в некоторых случаях возникновение опухоли может быть связано с дефектами в стромальных клетках, что показано в случае миелодиспластическо-го синдрома [99,96]. Так как популяцию МСК КМ можно считать относительно стабильной по локализации, в отличие от гемопоэтических предшественников, возможно формирование колоний МСК, несущих мутации, в определённом участке КМ, где они будут поддерживать рост мутантного гемопоэтического клона [100].
Исcледования взаимодействий опухолевых клеток и их стромального окружения в КМ необходимо для разработки новых методов лечения и преодоления резистентности, причины которой зачастую неясны. Име- ющиеся на данный момент формы терапии опухолей, локализованных в КМ, могут иметь эффект на раковые клетки, но не на клетки микроокружения, которое остаётся изменённым даже после проведённого лечения, что может приводить к ранним рецидивам [79]. В литературе рассматривается такой способ лечения заболеваний в КМ,при котором МСК используются как вектор для доставки растворимых факторов в микроокружение опухоли. Это связано с миграцией МСК в области воспаления согласно градиенту специфических хемокинов, например VEGF, интерлейкин-8, PDGF и других [101,82].
Заключение. Таким образом, МСК КМ представляют собой гетерогенную популяцию клеток, в составе которой есть как небольшое число плюрипотентных клеток,так и частично коммитированные предшественники. Основным направлением дифференцировки МСК КМ является остеогенное,однако при определённых культуральных условиях МСК демонстрируют высокий уровень пластичности, дифференцируясь в другие типы клеток,что является перспективным направлением регенеративной терапии. Гетерогенность МСК КМ при культивировании требует более детального изучения их фенотипа и происхождения, в том числе и для разработки новых методов регенеративной терапии. МСК КМ играют важную роль в патогенезе различных гемопоэтических заболеваний, являясь частью опухолевого микроокружения, черты которого могут сохраняться и после проведённой терапии. Дальнейшее изучение МСК КМ как части стромы,поддерживающей развитие опухоли,необходимо для разработки методов лечения и предотвращения развития ранних рецидивов и резистентности к лечению.
Список литературы Мезенхимные стромальные клетки костного мозга и их роль в формировании опухолевой ниши при онкогематологических заболеваниях
- Friedenstein A., Chailakhjan R., Lalykina K. The development of fibroblast colonies in monolayer cultures of guinea-pig bone marrow and spleen cells // Cell Tissue Kinet.— 1970.— Vol. 3, N4.— P. 393-403.
- Caplan A. Mesenchymal stem cells // J. Orthop. Res.— 1991.—Vol. 9, N5.— P. 641-650.
- Horwitz E. M., Le Blanc K., Dominici M. et al. Clarification of the nomenclature for MSC: The International Society for Cellular Therapy position statement // Cytotherapy.— 2005.— Vo.7, N5.— P. 393-395.
- Dominici M., Le Blanc K., Mueller I. et al. Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement// Cytotherapy.— 2006.— Vol. 8, N4.—P. 315-317.
- Galderisi U., GiordanoA. The gap between the physiological and therapeutic roles of mesenchymal stem cells // Medicinal Research Reviews.— 2014.—Vol. 34, N5.—P. 1100-1126.
- da Silva Meirelles L., Chagastelles P. C., Nardi B. Mesenchymal stem cells reside in virtually all postnatal organs and tissues // J. Cell Sci.— 2006.— Vol. 119, N11.— P. 2204-2211
- Pacini S., Petrini I. Are MSCs angiogenic cells? New insights on human nestin-positive bone marrow-derived multipotent cells // Front. Cell Dev. Biol.— 2014.—Vol. 2.— 11 p.
- Al-Nbaheen M., Vishnubalaji R., Ali D. et al. Human stromal (mesenchymal) stem cells from bone marrow, adipose tissue and skin exhibit differences in molecular phenotype and differentiation potential // Stem Cell Rev.— 2013.— Vol. 9.— P. 32-43.
- Owen M. Marrow stromal stem cells // Journal of Cell Science — 1988.— Suppl. 10.— P. 63-76.
- MuragliaA., Cancedda R., Quarto R. Clonal mesenchymal progenitors from human bone marrow differentiate in vitro according to a hierarchical model // J. Cell Sci.— 2000.—Vol. 113 — P. 1161-1166.
- Russell K. C., PhinneyD. G., Barrilleaux B. L. et al. In Vitro High-Capacity Assay to Quantify the Clonal Heterogeneity in Trilineage Potential of Mesenchymal Stem Cells Reveals a Complex Hierarchy of Lineage Commitment // Stem Cells.— 2010.—Vol. 28.— P. 788-798.
- BakshD., SongL., Tuan R. S. Adult mesenchymal stem cells: characterization, differentiation, and application in cell and gene therapy // J. Cell. Mol. Med.— 2004.—Vol. 8, N3.— P. 301-316.
- Bianco P., Robey P. G., Saggio I., Riminucci M. "Mesenchymal" Stem Cells in Human Bone Marrow (Skeletal Stem Cells): A Critical Discussion of Their Nature, Identity, and Significance in Incurable Skeletal Disease // Hum. Gene Ther.— 2010.— Vol. 21, N9.— P. 1057-1066.
- Xe Q, Wan C, Li G. Concise review: Multipotent Mesenchymal Stromal Cells in Blood // Stem Cells.— 2007.— Vol. 25.— P. 69-77.
- Bonnet P., Delorme B., Lopez A. et al. Multipotential Mesenchymal Stem Cells Are Mobilized into Peripheral Blood by Hypoxia // Stem Cells.— 2006.—Vol. 24, N10.— P. 2202-2208.
- БуравковаЛ. Б., КапланскийА. С., Андреева Е. Р. и др. Особенности формирования костной мозоли у крыс после введения в область перелома мультипотентных мезенхимальных стромальных клеток, культивированных при различном содержании кислорода // Клеточная трансплантология и тканевая инженерия.— 2009.—Т. IV, № 3.— С. 52-56.
- Rankin E.B., NarlaA., Park J. K., Lin S. et al. Biology of the Bone Marrow Microenvironment and Myelodysplastic Syndromes // Mol. Genet. Metab.— 2015.—Vol. 116, N1-2.— P. 24-28.
- Pal B., Das B. In vitro Culture of Naive Human Bone Marrow Mesenchymal Stem Cells: A Stemness Based Approach // Front. Cell Dev.— 2017.—Vol. 5.— 19 p.
- Айзенштадт А. А., Енукашвили Н. И., ЗолинаТ. Л. и др. Сравнение пролиферативной активности и фенотипа МСК, полученных из костного мозга, жировой ткани и пупочного канатика // Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова.— 2015.— Т. 7, № 2.—С. 14-22.
- KufiS., KufiZ., KreyenbergH. et al. CD271 antigen defines a subset of multipotent stromal cells with immunosuppressive and lymphohematopoietic engraftment-promoting properties // Haematologica.— 2010.— Vol. 95, N4.— P. 651-659.
- Simmons P.J., Torokstorb B. Identification of stromal cell precursors in human bone-marrow by a novel monoclonal-antibody, Stro-1 // Blood.— 1991.—Vol.78, N1.—P. 55-62.
- Sobiesiak M., Sivasubramaniyan K., Hermann C. et al. The mesenchymal stem cell antigen MSCA-1 is identical to tissue non-specific alkaline phosphatase // Stem Cells Dev.— 2010.—Vol. 19, N5.— P. 669-677.
- Deschaseaux F., Gindraux F., Saadi R. et al. Direct selection of human bone marrow mesenchymal stem cells using an anti-CD49a antibody reveals their CD45med, low phenotype // Br. J. Haematol.— 2003.—Vol. 122, N3.—P. 506-517.
- Pinho S., LacombeJ., Hanoun M. et al. PDGFR alpha and CD51 mark human Nestin+ sphere-forming mesenchymal stem cells capable of hematopoietic progenitor cell expansion //J. Exp. Med.— 2013.— Vol. 210, N7.—P. 1351-1367.
- Tormin A., Li O., Brune J. C. et al. CD146 expression on primary nonhematopoietic bone marrow stem cells is correlated with in situ localization // Blood.— 2011.—Vol. 117, N19.— P. 5067-5077.
- Jones E., Schäfer R. Where is the common ground between bone marrow mesenchymal stem/stromal cells from different donors and species? // Stem Cell Res. Ther.— 2015.— Vol. 6, N1.— 143 p.
- D'Ippolito G., Diabira S., Howard G. A., Menei P., Roos B. A., Schiller P. C. Marrow-isolated adult multilineage inducible (MIAMI) cells, a unique population of postnatal young and old human cells with extensive expansion and differentiation potential // J. Cell Sci.— 2004.—Vol. 117, N14.— P. 2971-81.
- KurodaY., Kitada M., Wakao S. et al. Unique multipotent cells in adult human mesenchymal cell populations // Proc. Natl. Acad. Sci. USA.— 2010.—Vol. 107, N19.— P. 8639-8643.
- JiangY., Jahagirdar B. N., Reinhardt R. L., et al. Pluripotency of mesenchymal stem cells derived from adult marrow // Nature.— 2002.—Vol.418.—P. 41-49.
- Petrini M., Pacini S., Trombi L., et al. Identification and purification of mesodermal progenitor cells from human adult bone marrow // Stem Cells Develop.— 2009.—Vol. 18, N6.—P. 857-866.
- IsernJ., Garcia-Garcia A., MartinA. M. et al. The neural crest is a source of mesenchymal stem cells with specialized hematopoietic stem cell niche function // Elife. — 2014.—Vol.3.— e03696.
- Morikawa S., MabuchiY., Niibe K. et al. Development of mesenchymal stem cells partially originate from the neural crest // Biochem. Biophys. Res. Commun.— 2009.— Vol. 379, N4.— P. 1114-1119.
- Bani-Yaghoub M., KendallS. E., Moore D. P. et al. Insulin acts as a myogenic differentiation signal for neural stem cells with multilineage differentiation potential // Development.— 2004.—Vol. 131, N17.— P. 4287-4298.
- Bianco P., Robey P. G., Saggio I., Riminucci M. "Mesenchymal" Stem Cells in Human Bone Marrow (Skeletal Stem Cells): A Critical Discussion of Their Nature, Identity, and Significance in Incurable Skeletal Disease // Hum. Gene Ther.— 2010.—Vol. 21, N9.— P. 1057-1066.
- ZorinV. L., PulinA.A., Eremin 1.1. et al. Myogenic potential of human alveolar mucosa derived cells // Cell Cycle.— 2017.—Vol. 16, N6.—P. 545-555.
- Szaraz P., GratchY. S., Iqbal F., Librach C. L. In vitro differentiation of human mesenchymal stem cells into functional cardiomyocyte-like Cells // J. Visual Exp. JoVE.— 2017.—Vol. 126.— e55757.
- Qian Q, Qian H, ZhangX, et al. 5-azacytidine induces cardiac differentiation of human umbilical cord-derived mesenchymal stem cells by activating extracellular regulated kinase // Stem Cells Dev.— 2012.— Vol. 21, N1.—P. 67-75.
- Sanchez-Ramos J. R. Neural cells derived from adult bone marrow and umbilical cord blood // J. Neurosci. Res.— 2002.—Vol. 69, N6.— P. 880-893.
- Shu S. N., Wei L., WangJ. H. et al. Hepatic differentiation capability ofrat bone marrow-derived mesenchymal stem cells and hematopoietic stem cells // World J. Gastroenterol.— 2004.—Vol. 10, N19 — P. 2818-2822.
- Chen L. B., Jiang X. B., Yang L. Differentiation of rat marrow mesenchymal stem cells into pancreatic islet beta-cells // WorldJ. Gastroenterol.— 2004.—Vol. 10, N20.— P. 3016-3020.
- Mets T, VerdonkG.In vitro aging of human bone marrow derived stromal cells // Mech. Ageing Dev.— 1981.— Vol. 16, N1.— P. 81-89.
- Sivasubramaniyan K, Ilas DC, Harichandan A, et al. Bone marrow-harvesting technique influences functional heterogeneity of mesenchymal stem/stromal cells and cartilage regeneration // Am. J. Sports Med.— 2018.— Vol. 46, N14.— P. 3521-3531.
- Siegel G., Kluba T., Hermanutz-Klein U. et al. Phenotype, donor age and gender affect function of human bone marrow-derived mesenchymal stromal cells // BMC Med.— 2013.—Vol. 11.— 146 p.
- Siddappa R., Licht R., van Blitterswijk C. et al. Donor variation and loss of multipotency during in vitro expansion of human mesenchymal stem cells for bone tissue engineering // J. Orthop. Res.— 2007.— Vol. 25, N8.—P. 1029-1041.
- Bara J. J., Richards R. G., Alini M., Stoddart M. J. Concise review: Bone marrow-derived mesenchymal stem cells change phenotype following in vitro culture: Implications for basic research and the clinic // Stem cells.— 2014.— Vol. 32, N7.— P. 1713-1723.
- Sakaguchi Y., Sekiya I., Yagishita K. et al. Suspended cells from trabecular bone by collagenase digestion become virtually identical to mesenchymal stem cells obtained from marrow aspirates // Blood.— 2004.— Vol. 104, N9.— P. 2728-2735.
- DiGirolamo C.M., Stokes D., Colter D. et al. Propagation and senescence of human marrow stromal cells in culture: a simple colony-forming assay identifies samples with the greatest potential to propagate and differentiate // Br. J. Haematol.— 1999.—Vol. 107, N2.—P. 275-281.
- Agata H., Asahina I., Watanabe N. et al. Characteristic change and loss of in vivo osteogenic abilities of human bone marrow stromal cells during passage // Tissue Eng. PartA.— 2010.—Vol. 16, N2.— P. 663-673.
- Rennerfeldt D. A., Van Vliet K. J. Concise Review: When colonies are not clones: evidence and implications of intracolony heterogeneity in mesenchymal stem cells // Stem Cells.— 2016.—Vol. 34, N5.— P. 1135-1141.
- Baxter M.A., Wynn R. F., Jowitt Sn. et al. Study of telomere length reveals rapid aging of human marrow stromal cells following in vitro expansion // Stem Cells.— 2004.— Vol. 22, N5.— P. 675-682.
- Neuhuber B., Swanger S.A., Howard L. et al. Effects of plating density and culture time on bone marrow stromal cell characteristics // Exp. Hematol.— 2008.—Vol. 36, N9.— P. 1176-1185.
- Estrada J., Torres Y., Benguria A. et al. Human mesenchymal stem cell-replicative senescence and oxidative stress are closely linked to aneuploidy // Cell Death Dis.— 2013.—Vol. 4.— e691.
- YlostaloJ., BazhanovN., Prockop D. J. Reversible commitment to differentiation by human multipotent stromal cells in single cell-derived colonies // Exp. Hematol.— 2008.—Vol. 36, N10.— P. 1390-1402.
- Jones E. A., KinseyA. E., EngishA. et al. Isolation and characterization of bone marrow multipotential mesenchymal progenitor cells // Arthritis & Rheumatism.— 2002.—Vol. 46, N12.— P. 3349-3360.
- LiuL., CheungT.H., CharvilleG.W., RandoT. A.Isolation of skeletal muscle stem cells by Fluorescence-Activated Cell Sorting // Nat. Protoc.— 2015.—Vol. 10, N10.—P. 1612-1624.
- АйзенштадтА.А., СказинаМ.А., КотелевскаяЕ.А. и др. Характеристики мезенхимных стромаль-ных клеток пупочного канатика человека при длительном культивировании in vitro // // Вестник Северо-Западного государственного медицинского университета им. И.И. Мечникова.— 2015.— Т. 10, №1.—С. 11-19.
- Tormin A., Li O., Brune J. C. et al. CD146 expression on primary nonhematopoietic bone marrow stem cells is correlated with in situ localization // Blood.— 2011.—Vol. 117, N19.— P. 5067-5077.
- PéaultB.Are mural cells guardians of stemness? from pluri- to multipotency via vascular pericytes // Circulation.— 2012.—Vol. 125, N1.—P. 12-13.
- Caplan A. I. New MSC: MSCs as pericytes are sentinels and gatekeepers // J. Orthop. Res.— 2017.—Vol. 35, N6.—P. 1151-1159.
- Sacchetti B., FunariA., Michienzi S. et al. Self-renewing osteoprogenitors in bone marrow sinusoids can organize a hematopoietic microenvironment // Cell.— 2007.—Vol. 131, N2.— P. 324-336.
- Jones E., McGonagle D. Human bone marrow mesenchymal stem cells in vivo // Rheumatology.— 2008.— Vol. 47, N2.—P. 126-131.
- de Souza L. E., Malta T. M., Kashima Haddad S., Covas D. T. Mesenchymal stem cells and pericytes: to what extent are they related? // Stem cells Dev.— 2016.—Vol. 25, N24.— P. 1843-1852.
- Corselli M., Chen C. W., Sun B., Yap S. et al. The tunica adventitia of human arteries and veins as a source of mesenchymal stem cells // Stem Cells Dev.— 2012.—Vol. 21, N8.— P. 1299-1308.
- Crisan M., Yap S., Casteilla L. A perivascular origin for mesenchymal stem cells in multiple human organs // Cell Stem Cell.— 2008.—Vol. 3, N3.— 301 p.
- Covas D. T., Panepucci R.A., Aparecida M. Fontes AM, et al. Multipotent mesenchymal stromal cells obtained from diverse human tissues share functional properties and gene-expression profile with CD146+ perivascular cells and fibroblasts // Experimental Hematology.— 2008.— Vol. 36, N5.— P. 642-654.
- Guimaräes-Camboa N., Cattaneo P., Sun Y et al. Pericytes of multiple organs do not behave as mesenchymal stem cells in vivo // Cell Stem Cell.— 2017.— Vol. 20, N3.— P. 345-359.
- Minasi M. G., Riminucci M., De Angelis L. et al. The meso-angioblast: a multipotent, self-renewing cell that originates from the dorsal aorta and differentiates into most mesodermal tissues // Development.— 2002.— Vol. 129, N11.— P. 2773-2783.
- Slukvin 1.1., Kumar A. The mesenchymoangioblast, mesodermal precursor for mesenchymal and endothelial cells // Cell Mol. Life Sci.— 2018.
- Fan W., Crawford R., Xiao Y. The ratio of VEGF/PEDF expression in bone marrow mesenchymal stem cells regulates neovascularization // Differentiation.— 2011.—Vol. 81, N3.— P. 181-191.
- Quirici N., Soligo D., Bossolasco P. et al. Isolation of bone marrow mesenchymal stem cells by anti-nerve growth factor receptor antibodies // Exp. Hematol.— 2002.—Vol. 30, N7.— P. 783-791.
- TakashimaY., EraT., Nakao K. et al. Neuroepithelial cells supply an initial transient wave of MSC differentiation // Cell.— 2007.—Vol. 129, N7.— P. 1377-1388.
- Семенова Н. Ю., Бессмельцев С. С., Ругаль В. И. Биология ниши гемопоэтических стволовых клеток // Клиническая онкогематология. Фундаментальные исследования и клиническая практика.— 2014.— Т. 7, № 4.— С. 501-510.
- Kudo-Saito C. Cancer associated mesenchymal stem cells aggravate tumor progression // Front. Cell Dev. Biol.— 2015.—Vol. 3.— 23 p.
- Xu S., De Veirman K., De Becker A. et al. Mesenchymal stem cells in multiple myeloma: a therapeutical tool or target? // Leukemia.— 2018.—Vol. 32, N7.—P. 1500-1514.
- André T., Meuleman N., Stamatopoulos B. et al. (2013) Evidences of early senescence in multiple myeloma bone marrow mesenchymal stromal cells // PLoS ONE.— 2013.— Vol. 8, N3.— e59756.
- Xiao P., Heshmati Y., Bouderlique T. et al. Mesenchymal stromal cells, instigator or suppressor for the development of MLL-AF9 induced acute myeloid leukemia? // Blood.— 2016.—Vol. 2, N12.— P. 1488-1488.
- Ito S., BarrettA.J., DutraA. et al. Long term maintenance of myeloid leukemic stem cells cultured with unrelated human mesenchymal stromal cells // Stem Cell Res.— 2015.—Vol.14, N1.— P. 95-104.
- ЧубарьА. В., Семенова Н. Ю., Ругаль В. И. и др. Изменение морфо-функциональных характеристик мезенхимных стромальных клеток костного мозга у больных множественной миеломой // Сборик материалов всероссийской конференции «StemCellBio-2018: фундаментальная наука как основа клеточных технологий».— С. 113-114.— Тезисы устного доклада.
- Ругаль В. И., Бессмельцев С. С., Семенова Н. Ю. и др. Характеристика микроокружения костного мозга при множественной миеломе до и после терапии // Сибирский научный медицинский журнал.— 2019 —Т. 39, № 1.— С. 112-118.
- Paunescu V., Bojin F. M., Tatu C. A. et al. Tumour-associated fibroblasts and mesenchymal stem cells: more similarities than differences // J. Cell Mol. Med.— 2011.—Vol. 15, N3.—P. 635-646.
- Shiga K., Hara M., Nagasaki T. et al. Cancer-Associated Fibroblasts: Their Characteristics and Their Roles in Tumor Growth // Cancers.— 2015.—Vol. 7, N4.—P. 2443-2458.
- Khan M., Adil SER., Olson A. L. The role of mesenchymal stem cells in oncology and regenerative medicine // Future Oncol.— 2017.— Vol. 13, N9.— P. 821-831.
- Laurenzana I., LamorteD., TrinoS. et al. Extracellular Vesicles: A New Prospective in Crosstalk between Microenvironment and Stem Cells in Hematological Malignancies // Stem Cells Int.—2018.—Vol. 2018.— ID9863194.
- Sun Z., Wang S., Zhao R. C. The roles of mesenchymal stem cells in tumor inflammatory microenvironment // Journal of Hematology & Oncology.— 2014.— Vol. 7.— 14 p.
- Reagan M. R., Rosen C. J. Navigating the bone marrow niche: translational insights and cancer-driven dysfunction // Nat. Rev. Rheumatol.— 2016.—Vol. 12, N3.—P. 154-168.
- Bisping G., Leo R., Wenning D. et al. Paracrine interactions ofbasic fibroblast growth factor and interleukin-6 in multiple myeloma // Blood.— 2003.—Vol. 101, N7.— P. 2775-2783.
- Han Z., JingY., Zhang S. et al. The role of immunosuppression of mesenchymal stem cells in tissue repair and tumor growth // Cell Biosci.— 2012.— Vol.2.— 8 p.
- Dong X., Han Z. C., Yang R. Angiogenesis and antiangiogenic therapy in hematologic malignancies // Critical Reviews in Oncology/Hematology.— 2007.—Vol. 62.—P. 105-118.
- Pruneri G., Ponzoni M., Ferreri A. J.M. et al. Microvessel density, a surrogate marker of angiogenesis, is significantly related to survival in multiple myeloma patients // British Journal of Haematology.— 2002.— Vol. 118, N3.—P. 817-820.
- Palumbo A. P., Pileri A., Dianzani U. et al. Altered expression of growth-regulated protooncogenes in human malignant plasma cells // Cancer Res.— 1989.—Vol. 49, N17.—P. 4701-4704.
- Garayoa M., Garcia J. L., SantamariaC. et al. Mesenchymal stem cells from multiple myeloma patients display distinct genomic profile as compared with those from normal donors // Leukemia.— 2009.—Vol. 23, N8.—P. 1515-1527.
- IwabuchiH., KakiharaT., KobayashiT. et al. A Gene Homologous to human endogenous retrovirus overexpressed in childhood acute lymphoblastic leukemia // Leukemia & Lymphoma.— 2004.—Vol. 45, N11.—P. 2303-2306.
- Patzke S., Lindeskog M., Munthe E., Aasheim H. C. Characterization of a novel human endogenous retrovirus, HERV-H/F, Expressed in Human Leukemia Cell Lines // Virology.— 2002.— Vol. 303, N1.— P. 164-173.
- Depil S., Roche C., Dussart P., Prin L. Expression of a human endogenous retrovirus, HERV-K, in the blood cells of leukemia patients // Leukemia.— 2002.—Vol. 16, N2.— P. 254-259.
- Bergfeld S. A., DeClerck Y. A. Bone marrow-derived mesenchymal stem cells and the tumor microenvironment // Cancer Metastasis Rev.— 2010.— Vol. 29, N2.— P. 249-261.
- Aanei C. M., Catafal L. C. Evaluation of bone marrow microenvironment could change how myelodysplastic syndromes are diagnosed and treated // CytometryA.— 2018.—Vol. 93, N9.— P. 916-928.
- ManierS., SaccoA., LeleuX., GhobrialI.M. et al. Bone marrow microenvironment in multiple myeloma progression // J. Biomed. Biotechnol.— 2012.— 157496 p.
- SceneayJ., Mark J. Smyth M. J., MollerA. The pre-metastatic niche: finding common ground // Cancer Metastasis Rev.— 2013.—Vol. 32, N3-4.—P. 449-464.
- Raaijmakers M. H.G.P., Mukherjee S., Guo S. et al. Bone progenitor disfunction induces myelodysplasia and secondary leukaemia // Nature.— 2010.— Vol. 464.— P. 852-857.
- Hoggatt J., KfouryY., Scadden D. T. Hematopoietic stem cell niche in health and disease // Annu Rev. Pathol.— 2016.— Vol. 11.— P. 555-581.
- Tehrani R. M., Verdi J., Noureddini M. et al. Mesenchymal stem cells: A new platform for targeting suicide genes in cancer // J. Cell Physiol.— 2018.—Vol. 233.— P. 3831-3845.


