Оптимизация условий инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae
Автор: Калинина Ирина Валерьевна, Фаткуллин Ринат Ильгидарович, Науменко Екатерина Евгеньевна
Рубрика: Биохимический и пищевой инжиниринг
Статья в выпуске: 4 т.10, 2022 года.
Бесплатный доступ
Целью настоящего исследования стал поиск рациональных режимов инкапсуляции биологически активного вещества рутина в живые клетки дрожжей Saccharomyces cerevisiae. Рутин является одним из наиболее хорошо изученных флавоноидов. Более известный как витамин Р в экспериментальных исследованиях рутин демонстрирует антиоксидантные, противомикробные, противовоспалительные, антидиабетические, антиадипогенные, нейропротекторные и другие свойства. Вместе с тем рутин, как и многие другие флавоноиды, является веществом нестабильным, склонным к окислительной деградации и активно вступающим в химические реакции со снижением или потерей биоактивных свойств. Для минимизации указанных проблем предложено использование технологии инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae. В данном исследовании процесс инкапсуляции вели с применением методов простой диффузии в живые клетки Saccharomyces cerevisiae. Для этого использовали режимы инкапсуляции в условиях термостатируемого встряхивателя, продолжительность процесса достигала 24 часов. В задачи исследования входила оценка влияния температурного и временного факторов на эффективность инкапсуляции рутина в клетки дрожжей. Использовались температурные режимы 28; 32 и 37 °С. Эффективность инкапсуляции определяли через 8, 16 и 24 часа после начала эксперимента. Проведенные исследования показали, что оба варьируемых фактора оказывают существенное влияние на эффективность загрузки биологически активного вещества в клетки дрожжей. Установлена прямая зависимость показателя эффективность инкапсуляции как от температуры, так и от продолжительности процесса. Вместе с тем, было отмечено, что использование температуры инкапсуляции 37 °С приводит к тому, что во второй временной отрезок 16-24 ч эффективность инкапсуляции снижается в сравнении с аналогичным периодом времени при температуре 32 °С. С использованием двухфакторного регрессионного анализа при проведении процедур оптимизации был установлен наиболее рациональный режим инкапсуляции рутина в клетки дрожжей, который составил 22 ч при температуре 33,8 °С.
Рутин, инкапсуляция, дрожжи saccharomyces cerevisiae, температура, продолжительность инкапсуляции
Короткий адрес: https://sciup.org/147239406
IDR: 147239406 | УДК: 664.8.038+663 | DOI: 10.14529/food220408
Optimization of rutin encapsulation conditions in Saccharomyces cerevisiae yeast cells
The aim of this study was to find rational modes of encapsulation of the biologically active substance rutin in living cells of the yeast Saccharomyces cerevisiae. Rutin is one of the most well studied flavonoids. Better known as vitamin P, rutin has shown antioxidant, antimicrobial, anti-inflammatory, antidiabetic, antiadipogenic, neuroprotective, and other properties in experimental studies. At the same time, rutin, like many other flavonoids, is an unstable substance, prone to oxidative degradation and actively entering into chemical reactions with a decrease or loss of bioactive properties. To minimize these problems, it is proposed to use the technology of rutin encapsulation in Saccharomyces cerevisiae yeast cells. In this study, the encapsulation process was carried out using simple diffusion techniques into living cells of Saccharomyces cerevisiae. For this, encapsulation modes were used under the conditions of a thermostatically controlled shaker; the duration of the process reached 24 hours. The aim of the study was to evaluate the influence of temperature and time factors on the efficiency of rutin encapsulation in yeast cells. The temperature conditions used were 28 °C, 32 °C and 37 °C. Encapsulation efficiency was determined 8, 16 and 24 hours after the start of the experiment. Studies have shown that both variable factors have a significant impact on the efficiency of loading biologically active substances into yeast cells. A direct dependence of the encapsulation efficiency index both on temperature and on the duration of the process has been established. However, it was noted that the use of an encapsulation temperature of 37 °C leads to the fact that in the second time period of 16-24 hours, the encapsulation efficiency decreases compared to the same time period at a temperature of 32 °C. Using two-way regression analysis during the optimization procedures, the most rational mode of rutin encapsulation in yeast cells was established, which was 22 hours at a temperature of 33.8 °C.
Текст научной статьи Оптимизация условий инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae
Развитие новых научных знаний в области биохимии, биотехнологии, пищевой технологии и в смежных областях подтверждает гипотезу о том, что питание, помимо своей основной функции, играет важную роль в поддержании здоровья человека и минимизации рисков возникновения неинфекционных заболеваний. На этом принципе основана концепция функционального питания. Компоненты, которые обеспечивают функциональное питание, чаще всего представляют собой витамины, минеральные вещества, ненасыщенные жирные кислоты, про-, пре- и синбиотики, а также минорные биологически активные соединения [1–5].
Минорные биологически активные вещества, среди которых растительные полифенолы, в последнее время привлекают большое внимание как потенциальные пищевые ингредиенты функциональной направленности [1, 5, 7, 15–18]. Класс флавоноидов наиболее богат такими веществами, которые в том числе достаточно хорошо изучены. Среди представителей биологически активных веществ (БАВ) – флавоноидов: рутин, куркумин, кверцетин, дигидрокверцетин и другие.
Клинические исследования, проведенные в отношении флавоноидов показывают, что многие из указанных соединений обладают способностью снижать риск развития рака, диабета, сердечно-сосудистых и других дегенеративных заболеваний. Тем не менее, исследования многих флавоноидов по химиопрофилактике рака in vivo не оправдали ожиданий. Основной причиной является их плохая растворимость во многих растворителях и в воде, биодоступность при пероральном приеме и неспособность пройти барьер в виде жестких воздействий процесса желудочнокишечного переваривания [6, 8–10, 19, 20].
Для обеспечения стабильности биологически активных соединений или улучшения их технологической пригодности для пищевых производств, а также увеличения биодоступности для организма человека требуется разработка новых решений. В качестве такого решения может выступать инкапсуляция – процесс, при котором БАВ защищаются материалом носителя при образовании капсул в микрометровом или нанометровом масштабе [3, 5, 8, 11, 17, 19].
Одним из экономически доступных видов инкапсуляции БАВ можно рассматривать использование в качестве защитной капсулы дрожжевой клетки, в частности Saccharomyces cerevisiae .
Клеточная стенка дрожжей состоит из внутреннего слоя несущих полисахаридов, выступающих в качестве каркаса и защитного наружного слоя маннопротеинов. Основным полисахаридом, несущим нагрузку, является разветвленный 1,3-β-глюкан. Благодаря наличию боковых цепей молекулы 1,3-β-глюкана и гибкой спиралевидной форме, отдельные молекулы β-глюкана могут связываться только локально через водородные связи, что приводит к образованию трехмерной сети, очень эластичной и способной пропускать молекулы разного размерного ряда. Полисахариды клеточной стенки дрожжей функционируют как каркас для внешнего слоя гликопротеинов. В совокупности эти гликопротеины ограничивают проницаемость клеточной стенки для макромолекул, и наоборот, они способны пропускать малые молекулы. Плазматическая же мембрана клеточной стенки дрожжей состоит в основном из липидов и белков примерно в равных пропорциях. Мембранные белки отвечают за регуляцию транспорта растворенных веществ в клетку и из нее, а также препятствуют свободной диффузии растворенных веществ из клетки. Некоторые авторы утверждают, что свойства мембраны клеточной стенки схожи липосомами, что дает осно- вание предполагать возможность инкапсуляции в клетки дрожжей гидрофобных веществ, в том числе флавоноидов [12].
Целью настоящего исследования была оценка влияния температуры и продолжительности процесса инкапсуляции на динамику эффективности загрузки гидрофобного антиоксиданта рутина в живые клетки дрожжей Saccharomyces cerevisiae.
Материалы и методы
Объекты исследования
В качестве биологически активного соединения был выбран флавоноид рутин (3', 4', 5,7-тетрагидрокси-флавон-3β-D-рутинозид), который представляет собой полифенол, обычно встречающийся в различных растениях, включая цитрусовые плоды, яблоки, помидоры и абрикосы [13].
Рутин, также известный как витамин Р, состоит из агликона кверцетина и дисахарида рутинозы, связанного с кверцетином в положении 3 С-кольца (рис. 1).
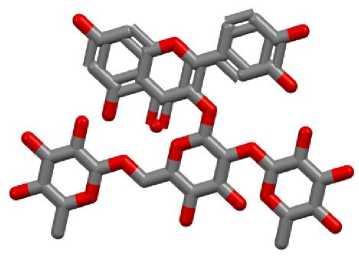
Рис. 1. Пространственная структура молекулы рутина [1 313]
На сегодняшний день известно более 130 фармацевтических препаратов, содержащих в своем составе рутин. Среди установленных фармакобиологических свойств рутина можно выделить антиоксидантные, противомикроб-ные, противовоспалительные, антидиабетические, антиадипогенные, нейропротекторные и другие [14, 19, 20].
Условия инкапсуляции
Инкапсуляцию рутина в дрожжевые клетки проводили в водной среде при соотношении компонентов дрожжи:рутин, равной 5:1 по массе. Использовался гидромодуль 1:100.
Инкапсуляцию проводили в термостатируемом встряхивателе при 200 об/мин, в двух температурных режимах 28; 32 и 37 °С в течение 24 часов.
Контроль эффективности инкапсуляции проводили в 3 временных точках, через каждые 8 часов.
Номенклатура показателей и методы анализа
Морфологическая структура образцов рутина была получена с применением просвечивающей электронной микроскопии высокого разрешения (Jeol JEM-2100), увеличение ×5000 .
Количественное содержание рутина определяли при взаимодействии с хлоридом алюминия спектрофотометрически по методике государственной фармакопеи XIV.
Эффективность инкапсуляции (ЭИ) определяли, как отношение БАВ, инкапсулированных, к количеству БАВ, оставшемуся на поверхности клеток дрожжей.
Эффективность инкапсуляции в % рассчитывали по формуле:
Xl-XO
ЭИ (%) = ×100, (1)
где X 1 – общее содержание БАВ (после процедуры разрушения капсул), мг; X 0 – содержание неинкапсулированного БАВ, мг; X 2 – количество БАВ, добавленное при инкапсуляции, мг.
Поиск оптимальных режимов инкапсуляции вели при использовании двухфакторного регрессионного анализа с использованием программного продукта MatCad.
Результаты исследования и их обсуждение
Результаты микроскопии рутина (рис. 2) показывают, что БАВ представляет собой скопление частиц в разном размерном диапазоне, в том числе достаточно крупных кристаллических частиц, склонных к агломерации.
В таблице представлены данные о физико-химических свойствах БАВ, имеющих решающее значение для оценки фармакологического потенциала вещества.
В литературе встречаются противоречивые данные о способности клеток дрожжей сорбировать частицы разного размера. Эластичность β-глюкановой сетки дает возможность предположить способность рутина проникать через нее. Вместе с тем, следующий барьер на пути БАВ – фосфолипидная мембрана – может быть менее проницаема для частиц крупного размера [12, 15].

Рис. 2. Морфология частиц рутина ( ×5000 )
Физико-химические свойства рутина [13]
|
Свойство |
Значение |
|
Растворимость в воде |
12,8 г/л |
|
log P |
–0,54 |
|
Количество акцепторов водорода |
21 |
|
Количество доноров водорода |
13 |
|
Количество бензойных колец |
6 |
Многие исследования показывают, что эффективность инкапсуляции биологически активных веществ в клетки дрожжей во многом определяется диффузионными процессами, эффективность которых, в том числе, зависит от растворимости инкапсулируемого вещества [11, 12, 15].
С учетом низкой растворимости рутина, около 1 %, принципиальное влияние может оказать повышение температуры инкапсуляции и увеличение продолжительности самого процесса.
Исследованиями, проведенными ранее, было установлено, что растворимость рутина в воде значительно увеличивается при повышении температуры более 70 °С. И уже через 30– 35 мин значение растворимости рутина превышает указанное в таблице более чем на 40 %.
Вместе с тем, такой температурный диапазон неприемлем для роста и развития дрожжевых клеток. По этой причине в данном исследовании мы осуществляли поиск оптимальных условий инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae, используя двухфакторный регрессионный анализ.
Оценка динамики процесса инкапсуляции рутина в дрожжи Saccharomyces cerevisiae представлена на рис. 3. Полученные данные свидетельствуют о значительной вариабельности процесса инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae. Установлено, что на эффективность инкапсуляции оказывают влияние оба оцениваемых фактора: температура и продолжительность процесса инкапсуляции.
Весомый вклад в повышение эффективности инкапсуляции внес временной фактор. Наблюдается четкая положительная зависимость роста эффективности инкапсуляции от продолжительности ведения процесса.
Так, через 24 часа значения эффективности инкапсуляции увеличивается по отношению к значениям в 8 часовой отметке, не зависимо от температуры. Положительное влияние продолжительности процесса инкапсуляции на его эффективность являлось ожидаемым и согласуется с данными, представленными в литературе. Определяется это, вероятно, вкладом двух факторов: постепенным увеличением доли растворенного рутина и ростом биомассы дрожжей, способных инкапсулировать биологически активные вещества.
Вместе с тем, было установлено, что в промежуток 8–16 ч процесс инкапсуляции протекал с более высокой эффективностью, чем во второй период (16–24 ч). (удалила)
Биосорбция органических веществ клетками дрожжей может быть представлена следующими стадиями: миграция органических соединений из жидкого раствора в пограничный слой частиц дрожжей; поверхностная диффузия внутрь клеток дрожжей; диффузии в поры биомассы; биосорбция активных центров внутри клеток [11]. Вероятно, каждый из этих этапов характеризуется собственными значениями удельной скорости и эффективности инкапсуляции, что требует дальнейшего изучения.
Положительное влияние повышения температуры на процесс инкапсуляции было отмечено в период 8–16 ч. Однако во второй временной отрезок эффективность инкапсуляции рутина при температуре 37 °С снижается в сравнении с температурным режимом 32 °С. Объяснением данному факту может быть то, что оптимальным температурным режимом для роста дрожжей Saccharomyces cerevisiae является диапазон 30–32 °С. Согласно литературным данным кратковременное увеличение температуры до сверхоптимальных значений (37–40 °С) может стимулировать рост дрожжевой массы, при этом длительное воздействие таких температур угнетает жизнедеятельность дрожжей.
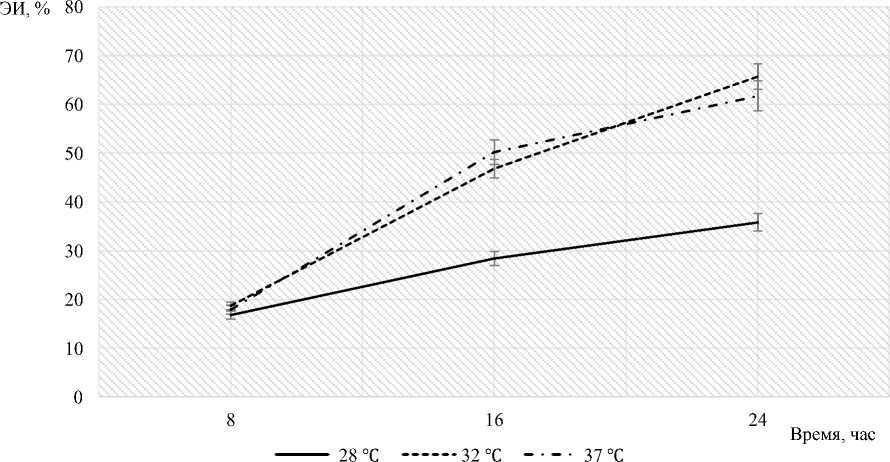
Рис. 3. Динамика процесса инкапсуляции образцов рутина в клетки дрожжей
Проведение процедуры оптимизации позволило установить оптимальное сочетание двух факторов: температуры и продолжительности процесса инкапсуляции. Установлено, что наиболее высокие значения эффективности инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae достигаются при 23,7 часа и 33,8 °С (рис. 4).
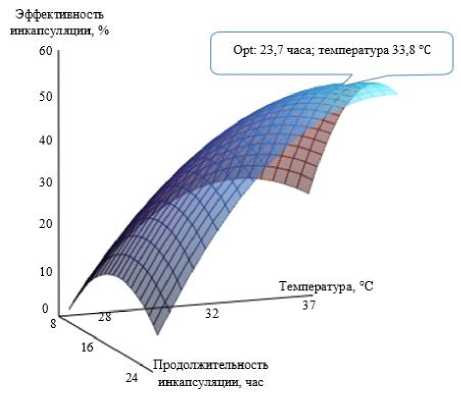
Рис. 4. Зависимость эффективности инкапсуляции рутина от температуры и продолжительности процесса
С учетом физического смысла величин в качестве рационального режима был принят режим инкапсуляции: температура 33 °С и длительность процесса 24 часа. Установлен- ный режим инкапсуляции был отработан, фактическая эффективность инкапсуляции составила 64,8 %.
Заключение
Таким образом, проведенные исследования подтвердили возможность инкапсуляции рутина в живые клетки дрожжей Saccharo-myces cerevisiae методом простой диффузии. Вместе с тем, эффективность инкапсуляции рутина, даже при значительных временных затратах, не достигала 65 %. Такие результаты могут объясняться низкой растворимостью флавоноида в воде, его склонностью к полимеризации и агломерации частиц.
Вместе с тем, для увеличения загрузки БАВ в клетки дрожжей целесообразно варьировать и временной режим процесса.
В качестве перспективного подхода для повышения эффективности инкапсуляции рутина в клетки дрожжей может также рассматриваться предварительное микроструктурирование БАВ.
Кроме того, следует оценить влияние соотношения БАВ:дрожжи на эффективность процесса инкапсуляции, а также более глубоко оценить термодинамические закономерности процесса инкапсуляции минорных биологически активных веществ полифенольной природы в клетки дрожжей Saccharomyces cerevisiae . Все это составляет основу будущих исследований.
Список литературы Оптимизация условий инкапсуляции рутина в клетки дрожжей Saccharomyces cerevisiae
- Бурлакова Е.Б. Антиоксиданты. Термины и определения / В.М. Мисин, Н.Г. Храпова, А Ю. Завьялов. М.: Изд-во РУДН, 2010. 63 с.
- Глобальный план действий по профилактике неинфекционных заболеваний и борьбе с ними на 2013-2020 гг. [Электронный ресурс]. URL: https://www.who.int/nmh/publications/ncd-action-plan/ru.
- Калинина И.В. Повышение биоактивности дигидрокверцетина на основе ультразвуковой микронизации / И.В. Калинина, И.Ю. Потороко, Р.И. Фаткуллин и др. // Технология и товароведение инновационных пищевых продуктов. 2019. № 1(54). С. 27-33.
- Нилова Л.П. Оптимизация ассортимента хлебобулочных изделий на основе анализа структуры потребительского рынка в г. Санкт-Петербурге и Челябинске / Л.П. Нилова, Н.В. Науменко, И.В. Калинина, К.Ю. Маркова // Вестник ЮУрГУ. Сер.: Экономика и менеджмент. 2011. Вып. 17, № 8(225). С. 183-189.
- Потороко И.Ю. Антиоксидантные свойства функциональных пищевых ингредиентов, используемых при производстве хлебобулочных и молочных продуктов, их влияние на качество и сохраняемость продукции / И.Ю. Потороко, А.В. Паймулина, Д.Г. Ускова и др. // Вестник ВГУИТ. 2017. Т. 79, № 4. С. 143-151. DOI: 10.20914/2310-1202-2017-4-143-151.
- Фаткуллин Р.И. и др. Влияние ультразвукового микроструктурирования биологически активных веществ на эффективность процесса их инкапсуляции / Р.И. Фаткуллин, И.В. Калинина, А.К. Васильев и др. // Вестник ЮУрГУ. Серия «Пищевые и биотехнологии». 2021. Т. 9, № 4. С. 100-107. DOI: 10.14529/food210411
- Шатнюк Л.Н. Инновационные ингредиенты для обогащения хлебобулочных изделий // Кондитерское и хлебопекарное производство. 2016. № 7-8(166). С. 41-45.
- Agati G., Azzarello E., Pollastri S., Tattini M. Flavonoids as antioxidants in plants: location and functional significance // Plant Sci., 2012, vol. 196 (3), pp. 67-76. DOI: 10.1016/ j.plantsci.2012.07.014
- Chen G.-L. Total phenolic, flavonoid and antioxidant activity of 23 edible flowers subjected to in vitro digestion / G.-L. Chen, S.-G. Chen, Y.-Q. Xie, F. Chen, Y.-Y. Zhao et al. // Journal of Functional Foods. 2015. Vol. 17. Р. 243-259. DOI: 10.1016/j.jff.2015.05.028
- Chua L.S. A review on plant-based rutin extraction methods and its pharmacological activities // J. Ethnopharmacol. 2013. V. 150. DOI: 10.1016/j.jep.2013.10.036
- Dardelle G. et al. Flavor encapsulation and flavor release performances of a commercial yeast-based delivery system // Food Hydrocolloids. 2007. V. 21. P. 953-960. DOI: 10.1016/ j.foodhyd.2006.12.013
- De Nobel, J.; Klis, F.; Priem, J.; Munnik, T.; Van den Ende, H. The glucanase-soluble mannoproteins limit cell wall porosity in Saccharomyces cerevisiae // Yeast 6. 1990. P. 491-499. DOI: 10.1002/yea.320060606
- FooDB [Electronic resource]. URL: http://foodb.ca.
- Fang Z.; Bhandari B. Encapsulation of polyphenols - A review // Trends Food Sci. Tech. 2010. V. 21. P. 510-523. DOI: 10.1016/j.tifs.2010.08.003
- Guorong S., Liqun R., Huazhong Y., Hua X., Hua Y., Runa Ji. Stabilization and encapsulation of photosensitive resveratrol within yeast cell // International Journal of Pharmaceutics. 2008. V. 349, Iss. 1-2. P. 83-93. DOI: 10.1016/j.ijpharm.2007.07.044
- González-Centeno R. et al. Effect of power ultrasound application on aqueous extraction of phenolic compounds and antioxidant capacity from grape pomace (Vitis vinifera L.): Experimental kinetics and modeling // Ultrasonics Sonochemistry. 2015. V. 22. P. 506-514. DOI: 10.1016/j.ultsonch.2014.05.027
- Potoroko I.Yu. et al. Sonochemical Micronization of Taxifolin Aimed at Improving Its Bioavailability in Drinks for Athletes // Человек. Спорт. Медицина. 2018. Т. 18, № 3. Р. 90-100. DOI: 10.14529/hsm180309
- Potoroko I.U. et al. Possibilities of Regulating Antioxidant Activity of Medicinal Plant Extracts // Человек. Спорт. Медицина. 2017. Т. 17, № 4. Р. 77-90. DOI: 10.14529/hsm170409
- Walle T. Methoxylated flavones, a superior cancer chemopreventive flavonoid subclass? // Semin. Cancer Biol. 2007. V. 17 (5). P. 354-362. DOI: 10.1016/j.semcancer.2007.05.002
- Yang J., Guo, J., Yuan, J. In vitro antioxidant properties of rutin // LWT Food Sci. Technol. 2008. V. 41. DOI: 10.1016/j.lwt.2007.06.010


