Получение жидкого фермента сычуга маралов
Автор: Гришаева И.Н.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Технология продовольственных продуктов
Статья в выпуске: 5, 2019 года.
Бесплатный доступ
Цель исследования - разработать способ получения жидкого фермента сычугов маралов (ФСМ) для эффективной переработки побочной продукции пантового оленеводства. Для проведения экспериментов забор сычугов маралов осуществляли в мараловодческом предприятии ФГУП «Новоталицкое» (Чарышский район, Алтайский край). Сычуг очищали от содержимого, жировой ткани, промывали холодной водой, измельчали в промышленной мясорубке МИМ 300 и хранили при температуре минус 18 ˚С. Опыты проводили в лаборатории переработки и сертификации пантовой продукции (отдела Всероссийского научноисследовательского института пантового оленеводства (ВНИИПО)). В ходе определения оптимальной продолжительности экстракции сычуги маралов настаивали в термостате, гидромодуль 1 : 125, в течение 3, 6, 12, 24, 48,72 ч, активность ферментов оценивали по обесцвечиваю окрашенного фибрина. С целью активизации пепсина в жидком экстракте применяли 10 %-й раствор соляной кислоты рН 1,0; 2,0; 3,0. Оптимальную температуру экспозиции определяли в точках 35, 37, 39, 41 ˚С...
Желудочно-кишечный тракт, марал, сычуг, жидкий фермент сычуга
Короткий адрес: https://sciup.org/140243443
IDR: 140243443 | УДК: 636.294:637
Obtaining liquid maral rennet enzyme
The research objective was to develop the way of receiving liquid maral rennet enzyme (MRE) for effective processing of by-products of maral farming. For carrying out the experiments the intake of maral rennet was carried out on maral farm FSUE “Novotalitskoye” (Charyshsky area, Altai Region). The rennets were cleaned of their contents and fat tissue, rinsed in cold water, minced in an industrial mincing machine MIM 300 and stored at the temperature of -18˚С. The experiments were conducted in the Laboratory for Processing and Certification of Velvet Antler Products (the Department of All-Russia Research and Development Institute of Reindeer Breeding for Velvet Antlers). In the course of determining the optimum extraction time, maral rennets were being infused in the thermostat the hydromodule 1 : 125 for 3, 6, 12, 24, 48, 72 hours, the activity of enzymes was assessed based on the bleaching of the colored fibrin. 10 % solution of hydrochloric acid with рН 1.0; 2.0; 3.0 was used in order to activate pepsin...
Текст научной статьи Получение жидкого фермента сычуга маралов
Введение . Создание и разработка новых технологических подходов по глубокой переработке как основной, так и побочной продукции пантового оленеводства являются основополагающим этапом развития данной отрасли. Вовлечение в производство вторичного сырья способствует повышению эффективности использования продукции мараловодства. Расширяя технологии переработки и включая биосубстанции с новыми свойствами в различные продукты, можно достичь высокой рентабельности отрасли [1]. В связи с этим разработка способов переработки желудочно-кишечного тракта маралов может обеспечить мараловодство не только новым видом сырья, но и использовать ранее не применяемые катализаторы для производства гидролизатов и концентратов из сырья маралов, что значительно сократит себестоимость готовых продуктов.
Л.А. Каймбаевой разработан способ получения сухого фермента сычугов маралов, который включает многоэтапную экстракцию с применением органических растворителей, которые не рекомендуется применять при производстве экологически чистых функциональных продуктов. На данный момент на территории России сычуги маралов не применяются в производстве и утилизируются мараловодческими хозяйствами еще на боенских пунктах, что ежегодно ведет к недополучению существенной прибыли [2].
Применяемые ранее способы получения гидролизатов и концентратов включали ферменты животного (пепсин говяжий), растительного (папаин) и микробного происхождения [3, 4]. Комплексы ферментов обеспечивали достаточно высокий выход биосубстанций, но зна- чительно увеличивали себестоимость готовых продуктов на их основе. В связи с этим разработка простого в технологическом исполнении способа переработки сычугов маралов без применения специализированного оборудования и органических растворителей позволит многим предприятиям малой мощности получать качественные биосубстанции для производства функциональных продуктов из сырья маралов.
Цель исследования: разработать способ получения жидкого фермента сычугов маралов для эффективной переработки побочной продукции пантового оленеводства.
Объекты и методы исследования. Научноисследовательская работа была проведена во Всероссийском научно-исследовательском институте пантового оленеводства ФГБНУ ФАНЦА в период 2017–2018 гг.
Для осуществления эксперимента заготовку сырья маралов осуществляли в ФГУП «Новота-лицкое» (Чарышский район, Алтайский край). В соответствии с принятыми нормами в процессе убоя маралов извлекали внутренние органы, в том числе желудочно-кишечный тракт, который разделывали на специальном столе. От желудочно-кишечного тракта отделяли кишечник и разделяли многокамерный желудок на отдельные части: книжку, сетку, рубец и сычуг. Сычуг освобождали от содержимого и жировой ткани, промывали проточной холодной водой, замораживали при температуре минус 18 °С. Замороженные сычуги для проведения экспериментальных исследований отправляли в лабораторию переработки и сертификации пантовой продукции отдела ВНИИПО.
В ходе исследования для получения жидкого фермента сычуга маралов (ФСМ) проведены эксперименты по приготовлению раствора из размороженного, измельченного на мясорубке МИМ 300 сычуга с размерами частиц 2–5 мм, время экспозии смеси в термостате 3, 6, 12, 24, 48, 72 ч, гидромодуль 1:125. Оптимальную температуру экспозиции определяли в точках 35, 37, 39, 41˚С.
Время экстракции оценивали по скорости обесцвечивания окрашенного фибрина. Окраску фибрина производили кармином, объединив его с едким натрием. Для определения работы фермента в экстрактах добавляли экстракт в количестве 2 мл в пробирку, а затем вносили окрашенный фибрин, после чего оценивали время обесцвечивания фибрина [5].
Для активизации пепсина в реакционной смеси использовали 10 %-й раствор соляной кислоты, количество которой регулировали с учетом величины кислотности, которая составляла 1,0; 2,0; 3,0.
Таким образом, технология получения жидкого фермента сычуга маралов заключалась в следующем: 50 г измельченного сычуга маралов выдерживали в реакционной смеси (1:126), состоящей из 6,3 л воды, подкисленной до нужной рН при температуре 37 °С. После фильтра-
Вестник КрасГАУ. 2019. № 5 ции жидкого ФСМ оценивали его протеолитическую активность.
Протеолитическую активность изучали по степени гидролиза (аминному азоту) жидкого фермента сычуга маралов с использованием в качестве субстрата побочного сырья пантового оленеводства – хвостов маралов [6].
Эксперименты проведены в трехкратной повторности.
Результаты исследования. С целью изучения возможности получения жидкого фермента сычуга маралов из измельченных слизистых оболочек были получены экстракты с разным временем экспозии, результаты исследования которых представлены в таблице 1.
Таблица 1
Определение оптимального времени экстракции жидкого ФСМ
|
Показатель |
Время экстракции, ч |
|||||
|
3 |
6 |
12 |
24 |
48 |
72 |
|
|
Время, затраченное на обесцвечивание фибрина, мин |
250 |
160 |
43 |
18 |
17 |
Испорчен |
Как показывают данные таблицы 1, расщепление белка фибрина быстрее всего происходит при воздействии экстрактов с экспозицией 24– 48 ч. Незначительное изменение времени обесцвечивая фибрина через 48 ч экстракции, вероятно, свидетельствует при заданных параметрах о полном извлечении ферментов из ткани сычуга. Увеличение времени до 72 ч приводит к закисанию жидкого экстракта.
При разных значениях рН получены реакционные смеси, в которых исследована протеолитическая активность на хвостах маралах, представленная на рисунке 1.
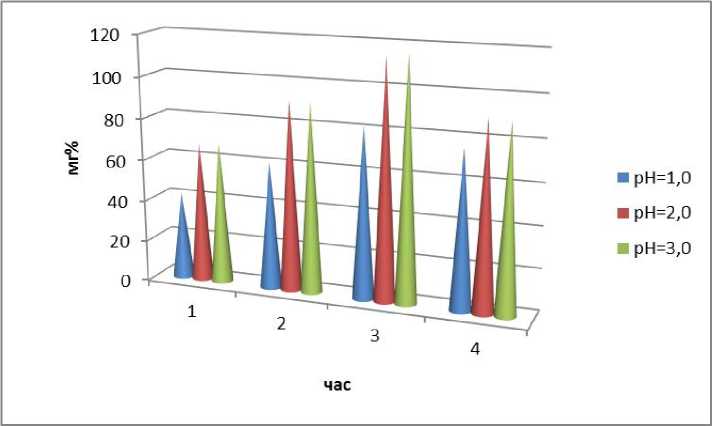
Рис. 1. Протеолитическая активность экстрактов из хвостов при разных рН
Содержание аминного азота позволяет судить о глубине расщепления белка до растворимых молекул: пептонов, пептидов (высоко-, средне-, низкомолекурных), аминокислот и, следовательно, о более высокой протеолитической активности ферментных препаратов. Так, при гидролизе хвостов раствором жидкого ФСМ с рН = 2,0 получены более высокие показатели аминного азота по сравнению с раствором рН=1,0 – на 15,5–37,9 %, растворы с рН = 3,0 имеют малозначимое недостоверное отличие показателя. В связи с чем оптимальным уровнем рН для получения жидкого ФСМ является величина 2,0.
Температурный оптимум определяли в экстрактах с рН=2,0, время – 24 ч, в разных точках. На рисунке 2 показано влияние температуры на протеолитическую активность жидкого ФСМ.
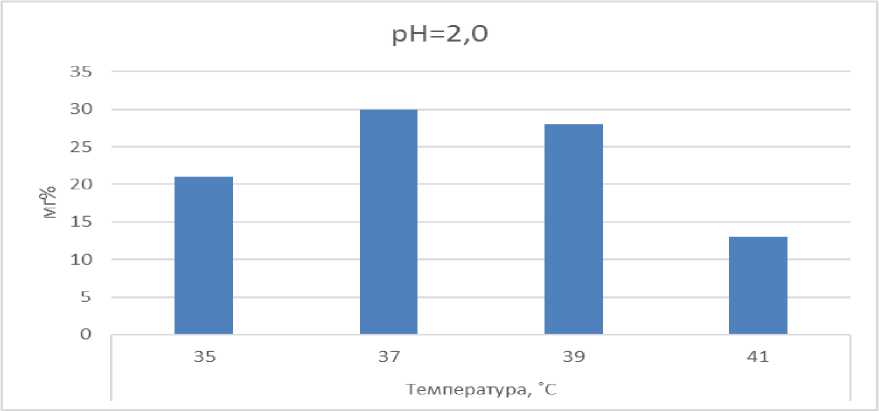
Рис. 2. Протеолитическая активность экстрактов из хвостов при рН = 2,0 в зависимости от температуры
Анализируя полученные данные, можно сказать, что оптимальными параметрами температуры для ферментации являются 37–39 °С. Увеличение температуры экстракции измельченных сычугов свыше 39 °С приводит к снижению протеолитической активности в 2,2 раза.
В результате проведенного исследования можно заключить, что оптимальными параметрами для получения жидкого фермента сычуга маралов является время экспозиции в термостате 24 ч, температура – 37 °С, рН = 2,0.
Список литературы Получение жидкого фермента сычуга маралов
- Хижняк С.В., Пучкова Е.П., Невзоров В.Н. и др. Влияние температуры на скорость роста амилолитических штаммов Geomyces pannorum // Вестн. КрасГАУ. - 2018. - № 1. - С. 214-221.
- Каймбаева Л.А. Научно-практические аспекты комплексной переработки и оценки качества мяса и продуктов убоя маралов: дис. … д-ра техн. наук. - Улан-Удэ: КИТА, 2014. - 318 с.
- Белозерских И.С., Луницын В.Г. Сравнение биохимического состава биосубстанций из пантов и второстепенной продукции пантового оленеводства, полученных разными технологиями // Вестн. Алтайского ГАУ. - 2015. - № 8 (130). - С. 125-128.
- Кротова М.Г., Луницын В.Г. Эффективность использования ферментов микробного происхождения при переработке сырья маралов // Сиб. вестн. с.-х. науки. - 2017. - № 5. - С. 97-102.
- ОСТ 10 288-2001. Препараты ферментные молокосвертывающие. Технические условия. - М., 2002.
- МУК 4.2.2316-08. Методы контроля бактериологических питательных сред. Определение аминного азота формольным титрованием по упрощенному методу Зеренса - Гаврилова. - М., 2008.


