Влияние катехоламинов на осмотическую хрупкость эритроцитов рыб в условиях индуцированного стресса
Автор: Фомина Любовь Леонидовна, Березина Дарья Игоревна, Моданова Карина Эдуардовна, Моисеев Александр Рустамович
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Рубрика: Сельскохозяйственные и ветеринарные науки
Статья в выпуске: 1 (45), 2022 года.
Бесплатный доступ
В современной ветеринарии ведется активный поиск чувствительных и дешевых инструментов для лабораторной диагностики стрессового состояния рыб, поэтому актуальной является работа по оценке влияния катехоламинового ответа на осмотическую резистентность эритроцитов тиляпий в условиях индуцированного стресса. Установлено, что катехоламиновый ответ тиляпий на модуляцию стресса был неоднозначным, а вариативность показателей у разных рыб была слишком высокая за счет чувствительности этих гормонов. В то же время, изменения в осмотической резистентности эритроцитов (ОРЭ) при воздействии кортизола достаточно заметны и достоверны, а также тесно связаны с уровнем адреналина в крови тиляпий, и этот показатель возможно использовать для диагностики стрессового состояния рыб как дешевый и наиболее доступный в лабораторной диагностике болезней рыб. В работе использовались гематологические, биохимические и статистические методы исследования.
Рыбы, тиляпия, стресс, катехоламины, эритроциты, осмотическая резистентность
Короткий адрес: https://sciup.org/149140621
IDR: 149140621 | УДК: 639.3:612.1 | DOI: 10.52231/2225-4269_2021_3_128
The effect of catecholamines on the osmotic fragility of fish erythrocytes under induced stress
There is an active search for sensitive and cheap ways for laboratory diagnostics of fish stress in modern veterinary medicine. Because of this assessing effects of catecholamine response on osmotic resistance of tilapia erythrocytes under induced stress is relevant. It has been found that the catecholamine response of tilapia to stress modulation is ambiguous and indicators variability in different fish is too high due to sensitivity of these hormones. Changes in osmotic resistance of erythrocytes (RE) when exposed to cortisol are quite noticeable and reliable and are also closely related to the level of adrenaline in tilapia blood. The indicator can be used to diagnose fish stress, as the cheapest and most suitable in laboratory diagnostics of fish diseases. Hematological, biochemical and statistical research methods have been used in the work.
Текст научной статьи Влияние катехоламинов на осмотическую хрупкость эритроцитов рыб в условиях индуцированного стресса
Гематологические методы диагностики традиционно являются самыми массовыми видами лабораторных исследований в ветеринарии. Состав крови изменяется при некоторых физиологических состояниях, позволяет получить лабораторную информацию о состоянии организма, применять её в интересах диагностики заболеваний, контроля за лечением больных животных. Почти всякий патологический процесс вызывает в картине периферической крови (гемограмме) изменения – сдвиги показателей [1].
Определение осмотической резистентности эритроцитов (ОРЭ) является одним из наиболее доступных в лабораторной диагностике методом оценки физико-химических свойств мембран эритроцитов. Изменения ОРЭ наблюдаются при ряде заболеваний у млекопитающих, так при гемолитических анемиях значения этого показателя снижаются, при гемоглобинопатиях, механической желтухе – повышаются [2].
На осмотическую устойчивость эритроцитов рыб влияет множество факторов: стадия их зрелости, температура, питание, состав корма, наличие токсинов в воде [3 ‒ 6], в том числе и стрессовое состояние [7, 8].
Первичной реакцией на воздействие стрессора у рыб являются эндокринные изменения, включающие, прежде всего, выработку катехоламинов (адреналин и норадреналин) и глюкокортикоидов [9, 10, 11].
При этом предполагается существование четырех степеней стрес-сорной реакции: полная стрессорная реакция, включающая повышенное образование катехоламинов и кортизола; частичная с повышенным образованием либо катехоламинов, либо кортизола, и реакции нарушения гомеостаза, которые рыба не воспринимает как стресс и не связанные ни с катехоламинами, ни с кортизолом [11]. В результате возникают вторичные метаболические, осмотические и другие изменения [12, 13, 14].
Ввиду большой трудоемкости процесса определения уровня катехоламинов крови у рыб, изучение механизма осмотических изменений при воздействии стресс-факторов и взаимосвязь этих изменений с содержанием адреналина и норадреналина в крови может дать чувствительный и дешевый инструмент для лабораторной диагностики стрессового состояния рыб.
Цель работы состоит в оценке влияния катехоламинового ответа на осмотическую резистентность эритроцитов тиляпий в условиях индуцированного стресса.
Материалы и методы исследования
Работа выполнена на кафедре ВНБ, хирургии и акушерства факультета ветеринарной медицины и биотехнологий Вологодской ГМХА имени Н. В. Верещагина.
Опыты проводили в аквариумных условиях на 18 нильских тиляпиях (Oreochromis niloticus L.), выращенных в условиях «АкваБиоЦентра» Вологодской ГМХА, которых предварительно разделили на три группы по 6 особей (табл. 1).
Таблица 1 ‒ Характеристика групп рыб в эксперименте .
|
Группа |
Воздействие |
Модель |
|
Контрольная (n=6) |
интактная |
контроль |
|
I экспериментальная (n=6) |
инъекция раствора дексаметазон-фосфата (4 мг/мл) в дозе 0,2 мл/ особь однократно |
острый стресс |
|
II экспериментальная (n=6) |
инъекция суспензии бетаметазона (2,63 мг+6,43 мг/мл) в дозе 0,5 мл/ особь однократно |
хронический стресс |
Животных I экспериментальной группы однократно обрабатывали дексаметазоном (Эллара, Россия), который метаболизируется в течение 4 часов, путем парентеральных инъекций в дозе 0,2 или 0,8 мг активного вещества дексаметазон фосфата на особь.
Рыбы II экспериментальной группы после адаптации подвергались хроническому стрессу (применяли суспензию бетаметазона (2,63 мг бетаметазона натрия фосфата + 6,43 мг бетаметазона дипропиона-та/мл), период выведения которого более 10 дней. Рыбам инъецирова- ли Дипроспан (Schering-Plough Labo N.V., Бельгия) по 0,5 мл на особь, что соответствует 3,5 мг активного вещества.
Данные синтетические гормоны обладают аналогичным кортикостероидам эффектом [12, 15].
Контрольная группа оставалась интактной.
Рыбы содержались в условиях с обеспечением непрерывной циркуляции воды между аквариумами с принудительной аэрацией при температуре 27 - 30°C (рис. 1) . Для кормления использовали гранулированный корм (режим – 1 раз в сутки).

Рисунок 1 — Экспериментальная установка с обеспечением непрерывной циркуляции воды
Забор крови для определения осмотической устойчивости эритроцитов проводили у рыб с разницей в 21 день шприцом из хвостовой вены в стеклянные пробирки, содержащие 3,8% раствор цитрата натрия в соотношении 1:9, для анализа катехоламинов ‒ в пластиковые пробирки с гепарином и пластиковые пробирки с активатором свертывания и разделительным гелем. Перед отбором проб крови рыб анестезировали при помощи добавления в воду гвоздичного масла в дозе 0,033 мл/л [16] с последующей выдержкой в ней 15 минут.
Оценку состояния функциональных сдвигов в состояние мембран эритроцитов проводили, используя модификацию метода определения осмотической резистентности эритроцитов М.А. Горшковой, Д.А Миллер, Е.Н. Егоровой, Т.А. Федотовой [2].
При исследовании ОРЭ в первую пробирку помещали 2,5 мл дистиллированной воды, во вторую - 2,5 мл изотонического (0,9%) рас- твора натрия хлорида, в третью – по 1,25 дистиллированной воды и изотонического раствора натрия хлорида (для получения 0,45 % раствора NaCl).
Затем во все пробирки добавляли по 0,01 мл крови. Перемешивали и центрифугировали в течение 10 минут при 2000 оборотов в минуту. Измеряли оптическую плотность надосадочных жидкостей трех проб на спектрофотометре при длине волны 414 нм в кювете с длиной поглощающего слоя 1 см против дистиллированной воды. ОРЭ оценивали по степени гемолиза эритроцитов в растворах с разной концентрацией натрия хлорида по сравнению со степенью гемолиза в образце с дистиллированной водой, который принимали за 100%. Степень гемолиза рассчитывали дважды в образцах с 0,9 и 0,45% растворами натрия хлорида по формуле:
H = 100 X Еоп. /Ек. , где H – степень гемолиза (%),
100 – степень гемолиза в образце с дистиллированной водой,
Еоп. - оптическая плотность надосадочной жидкости в образце,
Ек. - оптическая плотность надосадочной жидкости в пробирке с дистиллированной водой [2, 17, 18].
Концентрацию катехоламинов в сыворотке крови устанавливали методом высокоэффективной жидкостной хроматографии в лаборатории ООО «Центр лабораторных исследований».
Полученный в ходе исследования цифровой материал обрабатывался с помощью програмного обеспечения Microsoft Excel и STATISTICA 6.0. Результаты представлены в виде средней величины и стандартной ошибки средней. Сравнение данных проводилось с применением U-критерия Манна-Уитни для независимых групп. Для оценки различий в зависимых выборках с нормальным распределением использовали t-критерий Стьюдента для зависимых выборок.
Результаты исследования
Стресс приводит к массивному высвобождению катехоламинов из хромаффинных клеток, за которым следуют быстрое изменение некоторых функций основных физиологических систем: дыхательной и сердечно-сосудистой [19]. Необходимое количество катехоламинов для проявления этих воздействий редко известно, поскольку химическое определение количеств адреналина и норадреналина затруднительно и требует больших объемов плазмы крови из-за их низкой концентрации [20] .
Количественное содержание адреналина и норадреналина в крови рыб представлено в таблице 2 .
Таблица 2 ‒ Катехоламины тиляпий в ходе эксперимента.
|
До обработки |
21-й день |
|||||
|
Наименование показателя |
га с о. |_ га ® X II л с *--о о. i-X о 2 |
К га га А 1-1 |
га га X с а *—- m i-i |
с га 2 |
га га m i-i |
к га га Е II X с а - V m i-i |
|
Адреналин, |
11315,5± |
3149,33± |
7117,0± |
83,50± |
65,25± |
92,50± |
|
пг/мл |
11097,5 |
3066,87 |
6041,44 |
23,50 |
4,23* |
14,50 |
|
Норадреналин, |
1628,5± |
728,0± |
2219,0± |
132,50± |
140,25± |
172,50± |
|
пг/мл |
1486,5 |
603,03 |
1723,65 |
17,50 |
15,91 |
57,50 |
|
* Различия с показателем второй экспериментальной группы достоверны (p ≤ 0,05). |
||||||
Содержание адреналина и норадреналина между рыбами одной группы очень сильно варьировалось (для адреналина 65 ‒ 22500 пг/ мл, для норадреналина 115 ‒ 5500 пг/мл), однако их уровни претерпели резкое снижение: адреналина ‒ на 97,9 ‒ 99%, норадреналина ‒ на 80 ‒ 92,2% у всех групп рыб к 21 дню эксперимента. Возможно, в результате анестезии и кратковременного хэндлинг-стресса (венепункция) произошел всплеск катехоламинов у исследованных нами тиляпий, о чем говорит динамика к последнему дню эксперимента не только экспериментальных, но и контрольных значений. В связи с этим можно также предположить, что к концу эксперимента организм исследуемых животных адаптировался к кратковременным стрессовым условиям, или по каким-либо другим причинам, на что указывает падение уровня основных катехоламинов (адреналина и норадреналина) относительно первоначального у всех групп рыб [20].
У всех позвоночных имеет место разнокачественность эритроцитов по резистентным характеристикам (осмотической и кислотной), которая формируется в результате действия на организм внешних и внутренних факторов. У человека в норме гемолиз эритроцитов на- чинает происходить в 0,46–0,42%-ном растворе NaCl, полный гемолиз ‒ в 0,32–0,3%-ном NaCl. Снижение осмотической резистентности эритроцитов происходит вследствие изменений структурных и функциональных свойств мембран эритроцитов, возникающих при старении организма, заболеваниях, обусловленных накоплением скрытых структурных повреждений в белково-липидном каркасе мембран низко- и высокостойких эритроцитов [21, 22].
Степень гемолиза эритроцитов человека, полученная с использованием унифицированного метода М.А. Горшковой, составила в норме 1,61±0,23% в 0,9% растворе натрия хлорида и 25,16±1,83% в 0,45% растворе натрия хлорида [2].
Степень гемолиза эритроцитов рыб, полученная с помощью этого же метода, оказалась значительно ниже, чем эритроцитов человека (табл. 3) , хотя, по данным некоторых авторов, эритроциты рыб по осмотической резистентности уступают таковым у млекопитающих: признаки гемолиза у них могут появляться уже при небольших разведениях физиологического раствора (0,9–0,81%-ный NaCl), массовый гемолиз эритроцитов половозрелых рыб происходит, как правило, при 0,63–0,54%-ном NaCl [23].
Таблица 3 ‒ Степень гемолиза эритроцитов рыб в изотоническом и гипотоническом растворах до стресса, %.
|
Концентрация раствора |
Контрольная группа (n=6) |
I эксперимен тальная (n=6) |
II эксперимен тальная (n=6) |
|
|
0,9%-ный натрия |
хлорид |
0,22±0,06 |
0,19±0,06 |
0,13±0,02 |
|
0,45%-ный натрия |
хлорид |
0,30±0,01 |
0,40±0,04 |
0,32±0,06 |
В 0,45%-ном (гипотоническом) растворе хлорида натрия гемолиз происходил значительно интенсивнее, чем в 0,9-ном (изотоническом). Различия в осмотической устойчивости эритроцитов рыб в группах-аналогах не были достоверными.
Острый стресс у рыб обеспечивает адаптацию организма к стрессовым условиям, что сопровождается активацией многих систем организма. Это требует активной работы всех клеток организма и их мембран соответственно [24]. Хронический стресс в свою очередь отрицательно влияет на здоровье организма и снижает устойчивость клеток эритроцитарного ряда к гемолизу [25], но полученные нами результаты оценки ОРЭ рыб спустя 21 день после воздействия гормонов, инду- цирующих острый и хронический стресс, отличаются от данных, полученных у человека (табл. 4).
Таблица 4 ‒ Степень гемолиза эритроцитов рыб в изотоническом и гипотоническом растворах после индуцированного стресса, %.
|
Концентрация раствора |
Контрольная группа (n=6) |
I эксперимен тальная (n=6) |
II эксперимен тальная (n=6) |
|
0,9%-ный хлорид натрия |
0,06±0,01 |
0,04±0,01 |
0,02±0,001 |
|
0,45%-ный хлорид натрия |
0,88±0,38* |
0,78±0,39* |
0,44±0,04 |
|
* Различия с показателем второй экспериментальной группы достоверны (p≤0,05). |
|||
Анализируя данные исследования, можно отметить значительное превышение степени гемолиза эритроцитов в 0,45%-ном растворе хлорида натрия у рыб контрольной и I экспериментальной групп над эритроцитами рыб II экспериментальной группы, что можно связать с продолжающимся воздействием хронического стресса у рыб этой группы. В изотоническом растворе натрия хлорида достоверных различий в ОРЭ эритроцитов выявлено не было.
Изучая динамику показателей осмотической устойчивости эритроцитов рыб в гипотоническом растворе, мы получили результаты, представленные на рисунке 2 .
Гемолиз эритроцитов рыб в 0,45% растворе натрия хлорида, %
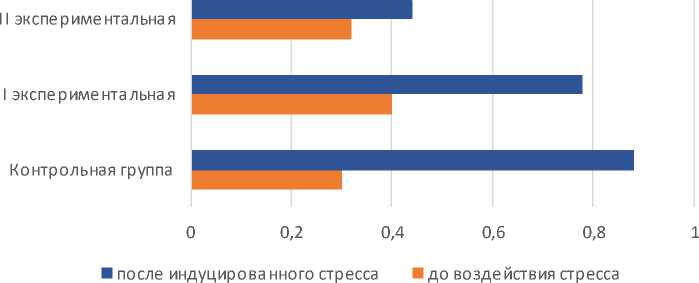
Рисунок 2 — Динамика степени гемолиза эритроцитов рыб в гипотоническом растворе хлорида натрия до и после гормониндуцированного стресса.
Во всех группах исследуемых рыб эритроциты снизили устойчивость к гемолизу, но наиболее выражен гемолиз в крови рыб контрольной группы. Осмотическая устойчивость эритроцитов рыб, находящихся под воздействием хронического стресса, оказалась в два раза выше таковой рыб контрольной группы. Таким образом, можно заключить, что кортизол влияет на эритроциты рыб, повышая их устойчивость к гемолизу, что возможно связано с нарушением функции их мембран и требует дальнейшего изучения с помощью атомно силовой микроскопии.
Оценивая влияние катехоламинов на осмотическую устойчивость эритроцитов рыб по шкале Чеддока, можно отметить заметную связь между содержанием адреналина и степенью гемолиза эритроцитов, причем до воздействия гормониндуцированного стресса эта связь была отрицательная, а после воздействия - положительная (рис. 3).
Корреляционная зависимость ОРЭ тиляпий от содержания катехоламинов
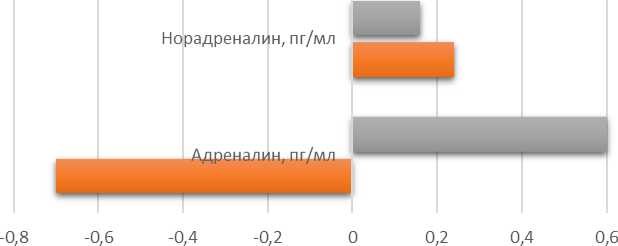
■ после индуцированного стресса ■ до воздействия стресса
Рисунок 3 — Динамика степени гемолиза эритроцитов рыб в гипотоническом растворе хлорида натрия до и после гормониндуцированного стресса
Заключение
Катехоламиновый ответ тиляпий на модуляцию стресса был неоднозначным, а вариативность показателей у разных рыб была слишком высокая за счет чувствительности этих гормонов, в связи с чем установление интенсивности стресса по данным показателям в рыбоводстве сомнительно и экономически не целесообразно. Поскольку изменения в ОРЭ при воздействии кортизола достаточно заметны и достоверны, а также тесно связаны с уровнем адреналина в крови тиляпий, этот показатель возможно использовать для диагностики стрессового состояния рыб, как дешевый и наиболее доступный в лабораторной диагностике болезней рыб.
Список литературы Влияние катехоламинов на осмотическую хрупкость эритроцитов рыб в условиях индуцированного стресса
- Амиров, Д.Р. Клиническая гематология животных: учебное пособие / Д.Р. Амиров, Б.Ф. Тамимдаров, А.Р. Шагеева. - Казань: Центр информационных технологий КГАВМ, 2020. - 134 с.
- Патент № 2328741 Рос. Федерация, МПК G01N 33/49. Способ определения осмотической резистентности эритроцитов / М.А. Горшкова, Д.А. Миллер, Е.Н. Егорова, Т.А. Федотова; патентообладатель Государственное бюджетное образовательное учреждение высшего профессионального образования «Тверская государственная медицинская академия» Министерства здравоохранения и социального развития Российской Федерации (RU)- № 2007116258/15; заявл. 28.04.2007; опубл. 10.07.2008, Бюл. № 19
- Иванов, А. А. Физиология рыб: учеб. пособ. / А. А. Иванов. -2-е изд., стер. - СПб.: Лань, 2021. - 288 с.
- Serpunin, G.G. Use of the ichthyohaematological studies in ecological monitoring of the reservoirs / G.G. Gorissen, O.A. Likhatchyova // Acta Vet. Brno, 1998. - Vol. 67. - P. 339-345
- Messager, J. L. Effects of dietary oxidized fish oil and antioxidant deficiency on histopathology, haematology, tissue and plasma biochemistry of sea bass Dicentrarchus labrax / J. L. Messager, G.Stephan, C. Quentel, F. Baudin-Laurencin // Aquat. Living Resour. Vivantes Aquat, 1992. -Vol. 5. - P. 205-214.
- Obach, A. Eff ect of alpha-tocopherol and dietary oxidized fi sh oil on the immune response of sea bass / A. Obach, C. Quentel, F. B Lau-rencin // Dis. Aquat. Org, 1993. - Vol. 15. - P. 175-185.
- Pages, T. Eff ects of daily managements stress on haematology and blood rheology of the gilthead seabream / T. Pages, E. Gomez, O. Sun-er, G. Viscor, L. Tort // J. Fish Biol, 1995. - Vol. 46. - P. 775-786.
- Микряков, Д.В. Изменение морфофизиологических показателей иммунокомпетентных органов карпа Cyprinus carpio под влиянием гормона стресса / Д.В. Микряков, В.Р. Микряков, Н.И. Силкина // Вопросы ихтиологии. - 2007. - Т. 47. - № 2. - С. 418-424.
- Gorissen, M. The endocrinology of the stress response in fish: an adaptation-physiological view / M. Gorissen, G. Flik // Fish physiology. -Academic Press, 2016. - Vol. 35. - P. 75-111.
- Schreck, C.B. The concept of stress in fish / C.B. Schreck, L. Tort // Fish physiology. - Academic Press, 2016. - Vol. 35. - P. 1-34.
- Smith, L. S. Introduction to fish physiology [Текст] / L. S. Smith. - TFH, 1982. - 352 p.
- Barton, B.A. Physiological changes in fish from st ress in aquaculture with emphasis on the response and effects of corticosteroids / B.A. Barton, G.K. Iwama // Annual Review of fish diseases. - 1991. - Vol. 1. -P. 3-26.
- Mazeaud, M.M. Primary and secondary effects of stress in fish: some new data with a general review / M.M. Mazeaud, F. Mazeaud, E.M. Donaldson // Transactions of the American Fisheries Society. - 1977. -Vol. 106. - № 3. - P. 201-212.
- Pickering, A. D. Stress and fish / A.D. Pickering. - London: Academic Press, 1981. - Pp. 367.
- Gamperl, A.K. Experimental control of stress hormone levels in fishes: techniques and applications / A.K. Gamperl, M.M. Vijayan, R.G. Boutilier // Reviews in Fish Biology and Fisheries. - 1994. - Vol. 4. - № 2. - P. 215-255.
- Hamackova, J. Clove oil as an anaesthetic for different freshwater fish species [Текст] / J. Hamackova, J. Kouril, P. Kozak, Z. Stupka // Bulgarian Journal of Agricultural Science. - 2006. - Vol. 12. - № 2. - P. 185-194.
- Моданова, К.Э. Изучение осмотической резистентности рыб при остром стрессе / К.Э. Моданова, Л.Л. Фомина // Молодые исследователи агропромышленного и лесного комплексов - регионам. Т. 3. Ч. 2. Биологические науки. - Вологда-Молочное: ФГБОУ ВО Вологодская ГМХА, 2021. - С. 64-67. - URL: https://molochnoe.ru/resources/files/nauka/sborniki/sbornik_332_2021. pdf
- Моисеев А.Р. Влияние хронического стресса на осмотическую резистентность эритроцитов рыб / А.Р. Мрисеев, Л.Л. Фомина // Молодые исследователи агропромышленного и лесного комплексов - регионам. Т. 3. Ч. 2. Биологические науки.-Вологда-Молочное: ФГБОУ ВО Вологодская ГМХА,2021. - С. 68-71. - URL: https://molochnoe.ru/ resources/files/nauka/sborniki/sbornik_332_2021.pdf
- Perry, S. F. The acute humoral adrenergic stress response in fish: facts and fiction / S. F. Perry, N. J. Bernier// Aquaculture. - 1999. -Vol. 177. - №1-4. - P. 285-295.
- Березина, Д.И. Изменение концентрации катехоламинов в крови в условиях экспериментальной модели стресса как биомаркер у тиляпий / Д. И. Березина, Л.Л. Фомина // Актуальные вопросы вет. биологии. - 2021. - Т. 51. - № 3. - С. 9-13
- Сравнительный анализ осмотической резистентности эритроцитов у различных по экологии teleostei / А.М. Андреева, И. П. Рябцева, И. И. Руднева, В. Г. Шайда, Н. Е. Ламаш, А. Э. Дмитриева// Вестник Санкт-Петербургского университета. - 2013. - Сер. 3. - Вып. 4. - С. 3-13.
- Попова, И.Е. Изучение структурных свойств эритроцитов крови новорожденных при оксидативном стрессе, вызванном гипоксией: специальность 03.00.02: диссертация на соискание ученой степени кандидата биол. наук / И.Е. Попова. - Воронеж, 2007. - 250 с.
- Андреева, А.М. Адаптации дыхательной функции крови у пресноводных костистых рыб / А.М. Андреева, И.П. Рябцева, В.В. Лукьяненко // Матер. 28-й Междунар. конф. «Биол. рес. Белого моря и внутренних водоемов европейского Севера». - Петрозаводск: КарНЦ РАН. -2009. - С. 33-39.
- Фомина, Л.Л. Влияние кортизола на некоторые иммунологические показатели карпов / Л.Л. Фомина, Д.И. Березина, Е.А. Пересто-ронина // Молочнохозяйственный Вестник. - 2019. - № 2. - С. 41-52.
- Гасасаева, Р.М. Изменения состояния мембран эритроцитов у студентов, переживающих экзаменационный стресс / Р.М. Гасасаева // Успехи современного естествознания. - 2019. - № 8. - С. 15-17.


