Влияние гипо- и гипертермии на коагуляционный гемостаз коров и кур in vitro
Автор: Фомина Л.Л., Рычкова Е.А., Киселева С.Д., Цыганок А.А.
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Рубрика: Сельскохозяйственные и ветеринарные науки
Статья в выпуске: 1 (53), 2024 года.
Бесплатный доступ
Коагулограмма относится к важнейшим диагностическим методам оценки физиологического состояния животных. Установлено, что при гипертермии in vitro в плазме крови коров происходит гиперкоагуляция, сопровождающаяся укорочение тромбинового (ТВ) и протромбинового времени (ПВ), а при гипотермии активируется противосвертывающая система. У кур активация свертывания крови и снижение активности антитромбина выявлены как при гипертермии (46°С), так и при гипотермии (18°С). Между показателями коагуляционного гемостаза и температурой инкубации плазмы коров обнаружена отрицательная корреляция от умеренной до заметной. У кур отметили высокую зависимость от температуры только тромбинового времени. Сравнивая реакцию показателей коагулограммы коров и кур на изменение температуры инкубации плазмы, можно отметить однотипность реакций тромбинового и активированного частичного тромбопластинового времени и совершенно разные реакции протромбинового времени, активности фибриногена и антитромбина у этих животных.
Коровы, куры, кровь, температура инкубации плазмы крови, гемостаз
Короткий адрес: https://sciup.org/149145818
IDR: 149145818 | УДК: 636:612.115:619 | DOI: 10.52231/2225-4269_2024_1_107
Effect of hypo-and hyperthermia on coagulation haemostasis of cows and hens in vitro
A coagulogram is the most important diagnostic method for assessing the physiological state of animals. Hyperthermia in blood plasma of cows results in hypercoagulation accompanied by shortening of the thrombin (TT) and prothrombin times (PT). Hypothermia activates the anticoagulation system. In chickens activation of blood clotting and a decrease in antithrombin activity were detected in both hyperthermia (46 °C) and hypothermia (18 °C). There is a negative correlation between coagulation parameters and incubation temperature in cow plasma, and only thrombin time is highly dependent on the temperature in chickens Comparing the reaction of coagulogram parameters of cows and chickens to changes in plasma incubation temperature, it is possible to note the uniformity of reactions of thrombin and activated partial thromboplastin time and completely different reactions of prothrombin time, fibrinogen and antithrombin activity in these animals.
Текст научной статьи Влияние гипо- и гипертермии на коагуляционный гемостаз коров и кур in vitro
Нарушение гемостаза является патогенетической основой многих болезней [1] и летальных исходов у кур и крупного рогатого скота, а также других животных, в связи с чем актуальна разработка диагностических, профилактических и терапевтических методов нормализации гемостаза у животных. Температура тела является одним из важнейших параметров гомеостаза, а также фактором регуляции функционирования живых систем [2]. Изменения системы гемостаза при гипертермическом воздействии широко изучается фундаментальной медициной в связи с успешным применением данного воздействия при лечении онкологических, аллергических, аутоиммунных и инфекционных заболеваний [3].
В связи с тем, что продуктивные животные и птицы имеют температуру тела, сильно отличающуюся от человеческой, методы оценки гемостаза, принятые в гуманной медицине могут не подходить для оценки гемостаза животных, но поскольку гемостазиологические оценки постепенно становятся важными для диагностики здоровья животных и для углубления существующих представлений о клеточных механизмах адаптации организма к температурным режимам, адаптированная и стандартизированная методология анализа свертывания крови продуктивных животных важна и срочно необходима [4].
Цель работы – определение зависимости скорости коагулологических реакций крови продуктивных животных от температуры инкубации плазмы.
Задачи исследования:
определить показатели коагуляционной активности крови коров in vitro при гипо- и гипертермии;
оценить показатели коагуляционной активности крови кур in vitro при гипо- и гипертермии;
провести корреляционно-регрессионный анализ полученных данных.
Материалы и методы
Работа выполнена в 2023 г. в Вологодской ГМХА имени Н.В. Верещагина при финансовой поддержке Российского научного фонда № 23-26-00115,
В исследовании использовали кровь 15 здоровых коров айрширской породы ( Bostaurus L., 1758) с привязным содержанием, в возрасте от 4 до 6 лет, разных стадий лактации и живой массой 400–480 кг, принадлежащих СПК «Агрофирма Красная Звезда» Вологодского района, и 19 здоровых кур-несушек ( Gallusgallus L., 1758), породы Род-Айленд красная, кросс Хайсекс Браун, принадлежащих СХПК «Племптица-Можайское», возрастом 2 года и весом 1900 г. Птица содержалась в четырехъярусных клетках производства компании «VALLI».
У птиц кровь получали в стеклянные пробирки, содержащие 3,8%-ный раствор цитрата натрия в соотношении 1:9 пункцией подкрыльцовой вены.
Отбор проб крови у коров проводился в вакуумные пробирки IMPROVACUTER, содержащие 3,8%-ный раствор цитрата натрия в соотношении 1:9 из хвостовой вены.
Объектом исследования являлась бедная тромбоцитами плазма, полученная в результате центрифугирования крови при 3000 оборотов в минуту в течение 20 мин [5, 6].
Для оценки состояния плазменно-коагуляционного гемостаза определяли следующие показатели: АЧТВ (активированное частичное тромбопластиновоевремя),ПВ(протромбиновоевремя),ТВ(тромбиновое время) и анализ активности фибриногена [7, 8]. Эти тесты основаны на триггерных реагентах, вызывающих образование фибринового сгустка в образце в присутствии фосфолипидов и кальция. Тромб обнаруживали механическим способом, основанным на измерении времени с момента внесения реагента, запускающего ферментативный процесс свертывания, до момента коагуляции (клоттинговыми методами) при температуре 37°С на коагулометре «Thrombostat» производства BehnkElektronik (Германия) и мануально (при периодическом покачивании пробирки) с использованием термостата медицинского водяного, серии TW: TW-2 (ELMI TW-2) при температуре 43°C, 40°C, 28°C, 24°C и 18°C . Были использованы медицинские наборы: «Тромбо-тест», «Техпластин-тест», «АПТВ-тест», «РФМК-тест планшетный вариант» и активность фибриногена (НПО РЕНАМ, Россия). Все исследования проводились в соответствии с инструкциями к реагентам [7, 8].
Антикоагуляционные свойства крови оценивали по активности Антитромбина III в плазме с помощью Тех-Антитромбин-теста при 18°C, 24, 28, 37, 40, 43°C. Принцип метода состоял в том, что Антитромбин III из плазмы, подвергнутой тепловому дефибринированию, инактивировал α-тромбин. Тестировали остаточную активность тромбина через 2 мин от начала инкубации дефибринированной плазмы с тромбином при разных температурах. По времени свёртывания оценивали активность Антитромбина III образца (принцип U.Abildgaard в модификации А.П. Момота и А.Н. Мамаева) [8].
Нормальность распределения данных оценивали при помощи критерия Шапиро-Уилка и Колмогорова-Смирнова. Для оценки достоверности различий параметров между видами в парных независимых выборках использовали критерий Манна-Уитни, для различий параметров при разных температурах в множественных зависимых выборках использовали критерий Вилкоксона. Силу парной линейной связи между переменными оценивали при помощи непараметрического коэффициента корреляции Спирмана (R). Качественную интерпретацию силы связи между показателями коагулограммы и температурой инкубации плазмы выполняли на основе шкалы Чеддока. Влияние температурного фактора оценивали с помощью теоретического коэффициента детерминации (R 2 ). Проверка статистической значимости коэффициентов корреляции осуществлялась с помощью статистического критерия Фишера (однофакторный дисперсионный анализ, One-way ANOVA) [9].
Результаты исследований
Исследования in vitro плазмы коров показали, что гипо- и гипертермия приводили к изменению каскада коагуляции (табл. 1).
Таблица 1 - Сравнительный анализ показателей гемостаза коров при разных температурах
|
Показатель (n=15) |
18 |
Температура, °С |
||
|
37 |
40 |
43 |
||
|
ТВ, с |
50,09±6,22dg |
26,54±1,74afg |
45,17±4,63dg |
18,01±2,11adf |
|
ПВ, с |
89,51±12,79dfg |
55,13±13,68ag |
34,57±1,68ag |
24,88±2,58adf |
|
АЧТВ, с |
353,09±14,89dfg |
62,83±2,34a |
64,31±6,85a |
88,91±29,19a |
|
Активность фибриногена, с |
130,15±27,00 dfg |
12,46±1,20 afg |
23,90±5,67 ad |
24,77±5,45 ad |
|
Антитромбин, с |
65,99±6,79df |
10,53±0,44ab |
10,11±0,22ab |
4,95±1,35 |
|
aРазличия с аналогичным параметром при 18°С достоверны (p≤0,05) dРазличия с аналогичным параметром при 37°С достоверны (p≤0,05) fРазличия с аналогичным параметром при 40°С достоверны (p≤0,05) gРазличия с анал огичным параметром при 43°С достоверны (p≤0 ,05) |
||||
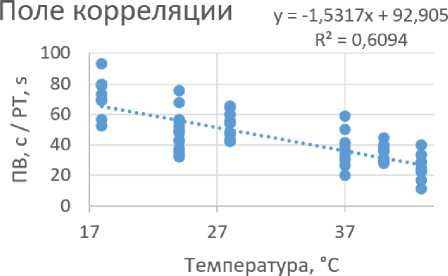
Корреляционно-регрессионный и однофакторный дисперсионный анализ (One-way ANOVA) выявили высокую зависимость от температуры ПВ и АЧТВ, коэффициент детерминации которых составил 60 и 44% соответственно (рис. 1).
Поле корреляции у = _8Л64х + 374,92 R2 = 0,4401
|
V) t |
500,00 400,00 |
|
1 1 CL < |
300,00 |
|
■^ |
200,00 |
|
со |
100,00 |
|
zr < |
0,00 |
Температура, °C
Рисунок 1 - Корреляционно-регрессионная зависимость ПВ и АЧТВ плазмы коров от температуры инкубации
В соответствии со шкалой Чеддока корреляционную связь между показателями гемостаза коров и температурным фактором можно охарактеризовать как отрицательную умеренную (АЧТВ; r=-0,44), заметную (ТВ, фибриноген; r=-0,51) и тесную (ПВ, АТ-III; r=-0,80)
У кур в результате изменения температуры инкубации плазмы были получены показатели активности свертывающего и противосвертывающего звена гемостаза представленные в таблице 2.
Таблица 2 - Сравнительный анализ показателей гемостаза кур при разных температурах
|
Показатель (n=19) |
18 |
Температура, °С 37 43 |
46 |
|
|
ТВ, с |
149,97±11,32cdf |
46,39±1,74a |
45,52±1,64a |
32,43±3,65a |
|
ПВ, с |
29,33±6,37cd |
83,13±15,36adf |
154,64±41,71aсf |
43,71±13,99cd |
|
АЧТВ, с |
84,72±15,23 |
64,56±7,67 |
78,82±12,41 |
86,86±17,56 |
|
Активность фибриногена, с |
25,35±4,99cdf |
93,88±9,75af |
109,15±11,27af |
395,60±32,99acd |
|
Антитромбин, с |
11,81±2,62cdf |
30,70±2,48a |
26,02±1,70a |
24,46±2,08a |
|
aРазличия с аналогичным параметром при 18°С достоверны (p≤0,05) cРазличия с аналогичным параметром при 37°С достоверны (p≤0,05) dРазличия с аналогичным параметром при 43°С достоверны (p≤0,05) f Различия с аналогичным параметром при 46°С достоверны (p≤0,05). |
||||
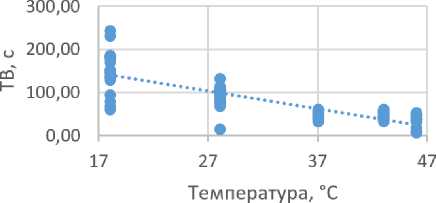
Корреляционно-регрессионный и однофакторный дисперсионный анализ (One-way ANOVA) у кур выявили высокую зависимость от тем- пературы ТВ и активности фибриногена, коэффициент детерминации которых составил 71 и 39% соответственно (рис. 2).
Поле корреляции v = -4,i238x + 2i5,i
R2 = 0,7057
Поле корреляции у = 8,87эзх-1бо,б4
R2 = 0,3934
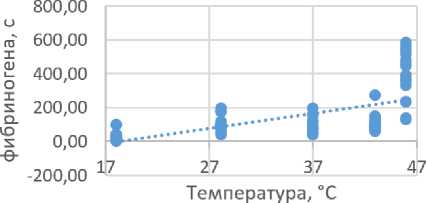
Рисунок 2 - Корреляционно-регрессионная зависимость ТВ и активности фибриногена плазмы кур от температуры инкубации
В соответствии со шкалой Чеддока корреляционную связь между показателями гемостаза кур и температурным фактором можно охарактеризовать как отрицательную высокую (ТВ; r=-0,8) и положительную высокую (фибриноген; r=0,8).
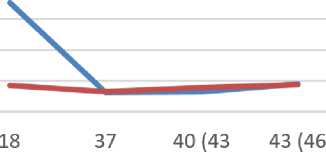
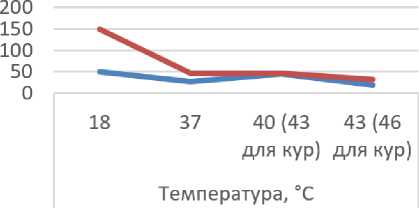
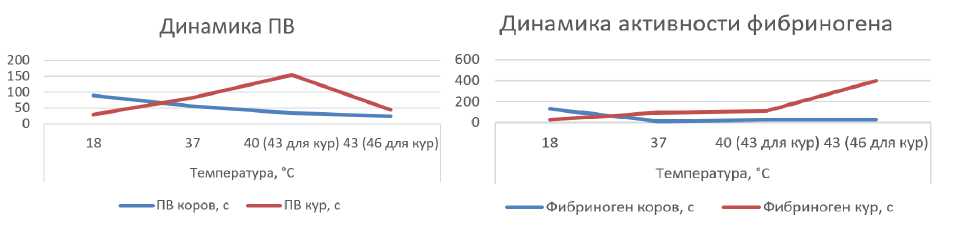
Сравнивая динамику показателей гемостаза кур и коров, можно отметить однотипность реакций тромбинового и активированного частичного тромбопластинового времени на изменение температуры инкубации плазмы и совершенно разные реакции протромбинового времени, активности фибриногена и антитромбина у этих животных (рис. 3, 4).
Динамика ТВ
Динамика АЧТВ
О
для кур) для кур)
Температура, °C
^—ТВ коров, с ^—ТВ кур, с
Рисунок 3 - Реакция ТВ и АЧТВ коров и кур на изменение температуры
Динамика активности ^ антитромбина
18 37 40 (43 для кур) 43 (46 для кур)
Температура, °C
^^—Антитромбин коров, с ^^—Антитромбин кур, с
Рисунок 4 - Реакция ПВ, активности фибриногена и антитромбина коров и кур на изменение температуры
Обсуждение
Повышение температуры инкубации плазмы крови коров приводит к гиперкоагуляции крови in vitro, активируя каскад свертывания и угнетая активность противосвертывающей системы, гипотермия оказывает обратный эффект на эти два звена системы гемостаза. Полученные результаты согласуются с результатами зарубежных авторов, которые делают вывод, что гиперкоагуляции во время теплового удара вызывает локальную гипоперфузию, тканевую гипоксию и последующую органную дисфункцию [10], а гипотермия на модельных организмах может служить защитой от повышенного тромбообразования [11].
Анализируя полученные результаты можно заключить, что большая часть показателей, характеризующих плазменный гемостаз кур, ярко реагирует на изменение температуры инкубации, особенно на гипотермию, поэтому оптимизация диагностических процедур и определение референтных значений показателей свертываемости крови у птиц при температуре, свойственной этим позвоночным, могут улучшить диагностику нарушений гемостаза. Мы согласны с M. Buzala с соавторами, что процессы свертывания крови глубоко заложены в геноме современной домашней птицы, и поэтому признание механизмов гемостаза и улучшение диагностических процедур могут стать очень мощным инструментом генетического отбора [12].
Выводы
В результате проведенных исследований определено, что в плазме крови коров при гипертермии in vitro происходит укорочение тромбинового (ТВ) и протромбинового времени (ПВ), что свидетельствует о риске тромбообразования и может наблюдаться при первой фазе ДВС-синдрома (гиперкоагуляции) [13–16].
Выявлено, что активность антитромбина III при охлаждении плазмы коров до 18 oC выросла на 85% по сравнению с нормотермией (40oC), что согласуется с данными других исследователей, которые заключают, что легкая гипотермия оказывает антикоагулянтное действие при охлаждении и это может оказывать ингибирующее действие на образование микротромбов [11,17, 18, 19].
У кур ответ плазменного гемостаза сопровождался активацией свертывания крови и снижением активности антитромбина как при гипертермии (46°С), так и при гипотермии (18°С). Корреляционнорегрессионный и однофакторный дисперсионный анализ выявили высокую зависимость от температуры тромбинового времени птиц, коэффициент детерминации которого составил 71%.
Сравнивая реакцию показателей коагулограммы коров и кур на изменение температуры инкубации плазмы, можно отметить однотипность реакций тромбинового и активированного частичного тромбопластинового времени и совершенно разные реакции протромбинового времени, активности фибриногена и антитромбина у этих животных.
Исследование выполнено при финансовой поддержке Российского научного фонда № 23-26-00115,
Список литературы Влияние гипо- и гипертермии на коагуляционный гемостаз коров и кур in vitro
- Maden M., £ol R., Arican M., Ider M., Garip M., Tras B. The evaluation of hemostatic dysfunctionand disseminated intravascular coagula-tionin dairy cows with abomasal displacement. Polish Journal of Veterinary Sciences. 2018. Vol. 21, no. 4, pp. 769 -778. - Text: direct.
- Suvernev A.V., Ivanov G.V., Novozhilov S.Yu., Yefremov A.V. Intensive Hyperthermia Therapy. Siberian Research Institute of Hyperthermia. 2011. Р. 96. - Text: direct.
- Ostberg J.R. Regulation of immune activity by mild (fever-range) whole body hyperthermia: effects on epidermal Langerhans cells. Cell Stress Chaperones. 2000. Vol. 5, no. 5, pp. 458-461. - Text: direct.
- Tavares-Dias M., Oliveira S.R. A review of the blood coagulation system of fish. RevistaBrasileira de Biociencias. 2009. Vol. 7, no. 2, pp. 205-224. - Text: direct.
- Зависимость коагуляционной активности крови кур in vitro от температуры / Л.Л. Фомина, Д.И. Березина, Т.С. Кулакова, К.Э. Моданова. - Текст: непосредственный // Международный вестник ветеринарии. - 2023. - № 4. - С. 327-334.
- Зависимость коагуляционной активности крови коров in vitro от температуры / Л.Л. Фомина, Д.И. Березина, Т.С. Кулакова, К.Э. Моданова. // Аграраная наука Евро-Северо-Востока. - 2024. - Т. 25. № 1. - С. 90-97.
- Берковский. А.Л. Диагностика нарушений гемостаза у животных / А.Л. Берковский, Е.В. Сергеева, А.В. Суворов // Ветеринария. - 2018. - № 5. - С. 54-57.
- Баркаган, З.С. Диагностика и контролируемая терапия нарушений гемостаза / З.С. Баркаган, А.П. Момот. - М.: Ньюдиамед-АО, 2008. - 292 с. - URL:https://elibrary.ru/item.asp?id = 19050159
- Шихова, О.А. Математическая биостатистика: методические указания и индивидуальные задания / О.А. Шихова. - Вологда-Молочное: ФГБОУ ВО Вологодская ГМХА, 2017. - 44 с.
- Burhans W.S., Rossiter Burhans C.A., Baumgard L.H. Invited review: Lethal heat stress: The putative pathophysiology of a deadly disorder in dairy cattle. Journal of Dairy Science. 2022. Vol.105. I. 5. P. 3716-3735. DOI: 10.3168/jds.2021-21080. - Text: direct.
- Wu J., Yuan W., Li J. etal. Effects of Mild Hypothermia on Cerebral Large and Small Microvessels Blood Flow in a Porcine Model of Cardiac Arrest. Neurocrit Care. 2017. Vol.27. Р. 297-303. https://doi.org/10.1007/ s12028-017-0395-6. - Text: direct.
- Buzala M. et al. The mechanism of blood coagulation, its disorders and measurement in poultry. Livestock Science. 2017. Т.195, pp. 1-8. DOI http://dx.doi.org/10.1016/j.livsci.2016.11.009. - Text: direct.
- Min L, Cheng J, Zhao S, Tian H, Zhang Y, Li S, Yang H, Zheng N, Wang J. Plasma-based proteomics reveals immune response, complement and coagulation cascades pathway shifts in heat-stressed lactating dairy cows. Journal of Proteomics. 2016. Vol.146, pp. 99-108. DOI: 10.1016/j. jprot.2016.06.008
- Николаев В.Ю.,ШахматовИ.И., КиселевВ.И., Вдовин В.М. Система гемостаза крыс при разных режимах одиночной гипертермической нагрузки // Современные проблемы науки и образования. - 2014. № 4. - С. 509-509. URL: https://science-education.ru/en/article/view?id = 14114
- Bruchim Y., Kelmer E., Cohen A., Codner C., Segev G., Aroch I. Hemostatic abnormalities in dogs with naturally occurring heatstroke. J Vet Emerg Crit Care (San Antonio). 2017. V.27(3), pp.315-324. DOI: 10.1111/ vec.12590. - Text: direct.
- Proctor E A, Dineen SM, Van Nostrand SC, Kuhn MK, Barrett CD, Brubaker DK, Yaffe MB, Lauffenburger DA, Leon LR. Coagulopathy signature precedes and predicts severity of end-organ heat stroke pathology in a mouse model. Journal of thrombosis and haemostasis. 2020. V.18, no.8, pp. 1900-1910. DOI: 10.1111/jth.14875. - Text: direct.
- Xu S, Miao H, Gong L, Feng L, Hou X, Zhou M, Shen H, Chen W. Effects of Different Hypothermia on the Results of Cardiopulmonary Resuscitation in a Cardiac Arrest Rat Model. Dis Markers. 2022. Vol.1-2, pp. 1-11. DOI: 10.1155/2022/2005616. - Text: direct.
- Thienel M., Müller-Reif J. B., Zhang Z., Ehreiser V., Huth J., Shchu-rovska K., Kilani B еt al. Immobility-associated thromboprotection is conserved across mammalian species from bear to human. Science. 2023. 380(6641):178-187. DOI: https://doi.org/10.1126/science.abo5044. -Text: direct.
- Gong, P. Effect of mild hypothermia on the coagulation-fibrinolysis system and physiological anticoagulants after cardiopulmonary resuscitation in a porcine model / P. Gong, M.Y. Zhang, H. Zhao, Z.R. Tang, R. Hua, X. Mei, J. Cui, C.S. Li. PLoS One. 2013. Vol.20, no.8(6). DOI: https://doi. org/10.1371/journal.pone.0067476. - Text: direct.


