Анализ и развитие известных теорий кристаллообразования
Автор: Гнездилова А.И., Шохалов В.А., Шохалова В.Н.
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Рубрика: Технические науки
Статья в выпуске: 1 (53), 2024 года.
Бесплатный доступ
В работе проведен сравнительный анализ различных механизмов зародышеобразования для дальнейшего развития и совершенствования процесса кристаллизации. Получено уравнение для расчета продолжительности индукционных периодов, которое удовлетворительно описывает процесс зародышеобразования в пересыщенных водных растворах лактозы. Среднее относительное отклонение вычисленных данных от опытных составило ±6,85%.
Молочный, кристаллизация, зародышеобразование, пересыщение
Короткий адрес: https://sciup.org/149145822
IDR: 149145822 | УДК: 637.345 | DOI: 10.52231/2225-4269_2024_1_173
Analysis and development of well-known theories of crystal formation
The work presents a comparative analysis of different nucleation mechanisms for further development and improvement of the crystallization process. The authors have developed an equation for calculating the duration of induction periods, which satisfactorily describes the process of nucleation in supersaturated water solutions of lactose. The average relative deviation of the calculated data from the experimental data is ± 6,85%.
Текст научной статьи Анализ и развитие известных теорий кристаллообразования
Кристаллизация – это сложный процесс, включающий следующие этапы: зародышеобразование, последующий рост образовавшихся кристаллических центров, коагуляцию, перекристаллизацию и др. [1,
2, 3]. Зародышеобразование (кристаллообразование) является первой стадией процесса, лишь после достижения зародышем определенного критического размера этот зародыш способен к росту, т. е. переходу во второй этап. Все зародыши, не достигшие этого размера, растворяются и являются ростовым материалом.
Первая стадия трудно отделима от собственно роста образовавшихся центров, поэтому наряду с этапом роста почти всегда продолжается параллельный процесс образования и растворения новых центров. Этот процесс постоянно сопровождает и предопределяет рост кристаллов. Исключить этот процесс практически невозможно, поэтому речь идет лишь о преобладании того или иного этапа в зависимости от скорости.
При высоких пересыщениях, когда преобладает скорость зародышеобразования, образуется достаточно много мелких органолептически не ощущаемых кристаллов. Именно этот режим следует реализовывать в производстве сгущенного молока с сахаром, в производстве сухой молочной сыворотки, в производстве молочного сахара по интенсивной технологии.
Для выращивания достаточно крупных кристаллов целесообразно интенсифицировать скорость роста. Для этого необходимо снизить пересыщение до определенного значения.
Таким образом, основным параметром, определяющим процесс кристаллизации, является коэффициент пересыщения, который определяется как отношение концентрации пересыщенного раствора к насыщенному при той же температуре.
В зависимости от величины коэффициента пересыщения раствор может находится в трех состояниях: стабильном, метастабильном и лабильном.
Стабильная область характеризует состояние раствора, при котором его концентрация равна или ниже равновесной. Метастабильное состояние можно разделить на две области. Первая метастабильная область находится между равновесной концентрацией и некой предельной концентрацией, ниже которой гомогенное зародышеобразование новых центров кристаллизации невозможно. Во второй метастабиль-ной области зародышеобразование происходит спонтанно, но через некоторый промежуток времени, названный индукционным периодом кристаллизации ( τind ) [4].
В лабильной области, которая характеризуется высоким пересыщением, зародышеобразование происходит спонтанно и продолжительность индукционного периода близка к нулю.
Возникновение центров кристаллизации происходит в течение определенного времени с определенной вероятностью, поэтому для описания процесса зародышеобразования используют уравнения вероятности в полях температур, пересыщений и скоростей циркуляции.
Выделив первую фазу процесса, необходимо понять условия, обеспечивающие требуемую вероятность образования кристаллов для оптимизации процесса кристаллизации в целом.
Оценку вероятности кристаллообразования следует осуществлять с помощью энергетического состояния объектов (рисунок).
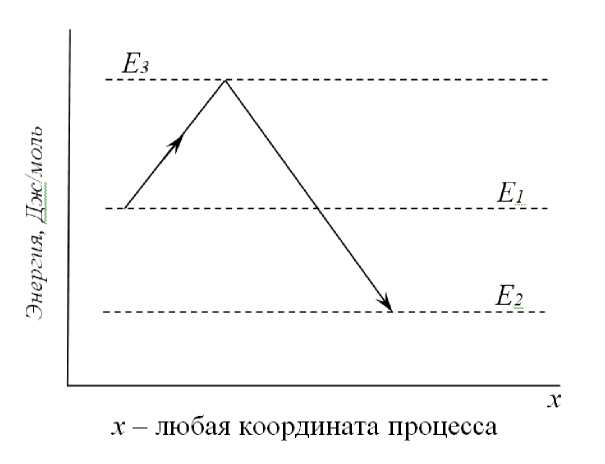
Рисунок 1 – Схема уровней энергии процесса кристаллизации
Как известно, кристаллизация возможна из пересыщенных растворов, которые характеризуются уровнем энергии Е1 . Энергетический уровень вещества в кристалле составляет Е2 . Таким образом, энергетическое состояние вещества в кристаллическом состоянии более выгодно, однако переход из состояния Е1 в состояние Е2 возможно при определенных условиях. Частицы (молекулы) в жидкости, кристалле или на его поверхности связаны с окружающими частицами и находятся в «потенциальных ямах». Чтобы перейти в другое равновесное состояние, частице требуется разорвать часть своих связей с соседними частицами, т. е. преодолеть энергетический барьер, высота которого составляет Е3-Е1 , где Е3 – энергия активации.
Из рисунка 1 следует, что чем выше пересыщение и выше уровень Е1 , тем ниже высота энергетического барьера и больше вероятность кристаллообразования. Именно поэтому в лабильной области имеет место самопроизвольное мгновенное образование центров кристаллизации и практически отсутствует кристаллизация в стабильной области.
Среднее значение энергии всех частиц определяет пересыщение и температуру процесса. Однако энергия разных частиц неодинакова, за счет этого образуются флуктуации и отдельные частицы приобре- тают энергию, достаточную для преодоления барьера. Но образование устойчивых зародышей возможно только в метастабильной области.
Идеи классической теории зародышеобразования были развиты в работах исследователей [5–9].
Открытия последних лет в области изучения структуры кристаллообразующих сред послужили основой для развития неклассических концепций образования кристаллов [10–15].
Исследователями была показана возможность спонтанного образования и сравнительно стабильного существования в пересыщенной среде (растворе, паровой фазе) и переохлажденных расплавах дополнительных наноразмерных кластеров. Они интерпретировались как предзародышевые частицы и были названы кватаронами. На этой основе была сформулирована специальная кватаронная концепция кластерной самоорганизации вещества, в рамках которой решался ряд спорных вопросов теории зародышеобразования, формирования кристаллических и некристаллических материалов.
Некоторые исследователи дали им названия «доллопы». И ква-тароны, и доллопы и другие подобные частицы можно рассматривать в качестве основных структурных элементов роста кристаллов. В результате была сформулирована принципиально новая кватаронная концепция роста кристаллов, отличающаяся от известных представлений микроблочного и атомарного роста кристаллов. Рассматриваемая кватаронная концепция лежит в основе популярных в настоящее время идей неклассического зарождения и роста кристаллов и формирования наноструктурированных материалов.
Кватароны образуются и могут существовать в неравновесных условиях. Нижняя геометрическая граница существует при r = δ, верхняя при r = 4δ, где r – радиус зародыша, δ – минимальное расстояние, на которое могут приблизиться молекулы кластера и окружающей среды без установления связи.
В качестве наноструктурированных частиц можно выделить также кластеры-прекуреоры, а кристаллизация сводится к сборке этих частиц. Кластер-прекуреор представляет собой 3-D фрагмент макрокри-сталлической структуры. Таким образом, кватаронная модель предполагает образование предзародышевых кластеров.
Целью нашей работы явился анализ различных механизмов зародышеобразования для дальнейшего развития и совершенствования процесса кристаллизации лактозы в производстве молочного сахара.
Теория
Как показано в работах [16, 17, 18], образованию кристаллических зародышей предшествует образование дозародышевых докри-сталлических ассоциатов, что не противоречит образованию нанораз- мерных кластеров.
Частицы новой фазы образуются постепенно путем укрупнения дозародышевых ассоциатов до размеров зародышей. Поскольку число крупных ассоциатов, способных стать зародышами, составляет незначительную долю, это свидетельствует о том, что на укрупнение ассоциатов до размеров критических зародышей необходимо время. Именно это время и обусловливает наличие индукционных периодов.
Таким образом, только ассоциаты, достигшие некоторого максимального значения ν max , способны стать зародышами.
Поскольку число ассоциатов с v max невелико, их увеличение определяется ростом вероятности взаимодействия ассоциата с мономерными молекулами. Для расчета v max воспользуемся уравнением Больцмана:
νmax = А∙m∙exp (- ε/k∙T), (1)
где е - энергия взаимодействия ассоциата с молекулой кристаллизующего вещества;
m – концентрация кристаллизующего вещества в растворе, моль/1000 г Н2О;
А – постоянная;
k – константа Больцмана.
Тогда с учетом уравнения Больцмана получим:
νmax = А∙m∙exp (- E/R∙T), (2)
где Е - энергия взаимодействия ассоциата с мономерными молекулами, Дж/моль;
m – концентрация пересыщенного раствора, моль/1000 г Н2О;
А – постоянная;
R – универсальная газовая постоянная, Дж/моль∙К;
T – температура, К.
Число молекул кристаллизующегося вещества, которое необходимо присоединить для получения критического зародыша, составит:
∆νmax = ν μmax - ν нmax = А∙(mμ - mн)∙exp (- E/R∙T), (3)
где т ^ и т н - концентрация растворов по линии первой границы метастабильности и по линии насыщения соответственно, моль/1000 г Н2О;
νнmax и νμmax – максимальное число молекул кристаллизующегося вещества в ассоциате по линии насыщения и по линии первой границы метастабильности.
Скорость роста ассоциата при условии m > т н составит:
dνmax /dτ = z∙exp (-Ea/RT)·(m - mн )n, (4)
где z – постоянная величина;
Еа – энергия активации процесса роста ассоциата, Дж/моль;
n – порядок роста.
После замены дифференциалов в уравнении (4) их частными приращениями было получено уравнение для расчета продолжительности индукционных периодов:
τind = В· (mμ- mн) ∙(m - mн )-n · exp (ΔЕ/RT),(5)
где В = А/Z; ΔЕ =Еа-Е.
При Т = const :
τind = D∙(m - mн )-n,(6)
где D=В·(mμ - mн)∙exp (ΔЕ /RT)(7)
Уравнения (5) и (6) были использованы для расчета индукционных периодов при кристаллизации лактозы в пересыщенных водных растворах. Значения n, D, В, ΔЕ определялись по экспериментальным данным о значениях Tind, т н , im [16]. Значения т н рассчитывались по данным о растворимости лактозы в воде, значения тц были определены путем экстраполяции кривых τind=f (m/ mH) в область τind —> ∞ и приведены в таблице 1.
Методы исследований
Продолжительность индукционных периодов Tnd экспериментально определялась нефелометрическим методом [17]. Методика экспериментального определения продолжительности индукционных периодов заключалась в следующем [18]. Пересыщенный раствор в количестве 400 мл раствора лактозы переносился в стеклянный термостатируемый кристаллизатор. После достижения раствором температуры опыта осуществлялось перемешивание раствора на лабораторной установке ER-10 с помощью стеклянной пропеллерной мешалки с частотой вращения n=1c-1 .
В ходе опытов через определенные интервалы времени с помощью термостатируемой пипетки отбирался пересыщенный раствор и в нем определялась мутность нефелометром. Продолжительность индукционных периодов фиксировалась по началу возрастания мутности.
Методика расчета Tind заключалась в следующем. На основе экспериментальных данных τ ind и в соответствии с уравнением (6) были найдены значения ln D и n при T=const . Затем было рассчитано значение ln[D/(mμ -mH)] при различных температурах и определены В и ΔЕ. Результаты расчетов приведены в таблице 1.
Результаты исследований и их обсуждение
Таблица 1 – Значение постоянных величин в уравнениях (4) и (5) при кристаллизации лактозы
|
Показатель |
Пересыщенный раствор лактозы при Т, К 293 333 |
|
|
n |
4,60 |
4,65 |
|
D |
347,2 |
290,0 |
|
mμ, моль/1000 г Н2О |
0,959 |
2,022 |
|
mн, моль/1000 г Н2О |
0,533 |
1,631 |
|
(mμ- mн), моль/1000 г Н2О |
0,426 |
0,391 |
|
ln Д/ (mμ- mн), |
6,703 |
6,609 |
|
В |
335 |
|
|
ΔЕ, Дж/моль |
2078 |
|
На основе этих данных по уравнению (5) были рассчитаны индукционные периоды и приведены в таблице 2.
Таблица 2 - Расчетные значения продолжительности индукционных периодов Tjnd мин. при кристаллизации лактозы
Пересыщенный раствор лактозы при Т, К
|
293 |
333 |
||
|
m/mH |
τ ind , мин. |
m/mH |
τ ind , мин. |
|
3,06 |
218,0 |
1,85 |
62,3 |
|
3,77 |
55,6 |
2,17 |
16,7 |
|
4,62 |
16,3 |
2,55 |
4,4 |
|
5,65 |
5,2 |
3,06 |
1,2 |
Среднее относительное отклонение вычисленных данных от опытных составило ±6,85%.
Заключение
-
1. С учетом современных представлений об образовании нанораз-мерных кластеров при кристаллизации предложена модель, согласно которой рост кристаллических зародышей определяется ростом доза-родышевых ассоциатов.
-
2. Получено уравнение для расчета продолжительности индукционных периодов в пересыщенных водных растворах лактозы, которое удовлетворительно описывает процесс. Среднее относительное отклонение вычисленных данных от опытных составило ±6,85%.
Список литературы Анализ и развитие известных теорий кристаллообразования
- Фольмер, М. Кинетика образования новой фазы / М. Фольмер. -М.: Наука, 1986. - 208 с.
- Странский, И.Н. К теории роста кристаллов и образование кристаллических зародышей / И.Н. Странский, Р.К. Каишев // Успехи химии. - 1939. - Т. XXI. - Вып. 4. - С. 408-465.
- Стрикленд-Констэбл, Р.Ф. Кинетика и механизм кристаллизации / Р.Ф. Стрикленд-Констэбл. - Л.: Недра, 1971. - 310 с.
- Хамский, Е.В. Кристаллизация из растворов / Е.В. Хамский. -Л.: Наука, 1967. - 150 с.
- Харин, В.М. О кинетике массовой кристаллизации из пересыщенных растворов / В.М. Харин // Коллоидный журнал. - 1974. - Т. XXXIV. - № 2. - С. 313-317.
- Шумская, Э.Е. О влиянии готовой кристаллической поверхности на скорость кристаллообразования сахарозы / Э.Е. Шумская, В.Д. Попов, С.И. Сиренко // Известия ВУЗов, Пищевая технология. - 1972. - № 6. - С. 155-158.
- Траоре, М. Кинетика зародышеобразования в растворах сахарозы / М. Траоре, В.И. Тужилкин, А.Р. Сапронов // Сахарная промышленность. - 1981. - № 10. - С. 28-30.
- Харин, С.Е. Кинетика фазовых переходов в пересыщенных растворах сахарозы / С.Е. Харин, А.В. Зубченко, Ю.Н. Левин // Коллоидный журнал. - 1969. - Т. XXXI. - № 1. - С. 147-152.
- Зубченко, А.В. Нестационарный режим образования новой фазы в пересыщенных растворах сахарозы / А.В. Зубченко, С.Е. Харин, Ю.Н. Левин // Известия ВУЗов, Пищевая технология. - 1968. - № 1. - С. 136-139.
- Асхабов, А.М. Кватаронная концепция: основные идеи и некоторые приложения / А.М. Асхабов // Тез.Коми научного центра УрО РАН, 2011. - № 3 (7). -С. 70-77.
- Портнов, В.Н. Возникновение и рост кристаллов / В.Н. Портнов, Е.В. Чупрунов. - М.: Изд. физико-математической литературы, 2006. - 328с.
- Асхабов, А.М. Строительные единицы в кристаллогенезе / А.М. Асхабов // III Межд. конференция «Кристаллогенез и минералогия». -Новосибирск: СО РАН, 2013. - С. 8-9.
- Асхабов, А.М. Эволюция и конкуренция идей в теории роста кристаллов в XX веке / А.М. Асхабов // Вестник ИГ Коми НЦ УрО РАН. -2012. - № 6. -С. 24-25.
- Асхабов, А.М. Агрегация кватаронов как механизм образования аморфных сферических частиц / А.М. Асхабов // Доклады наук о Земле. - 2005. - Т. 400. - № 1. - С. 937-940.
- Асхабов, А.М. Новые идеи в теории образования кристаллических зародышей / А.М. Асхабов // Известия Коми НЦ УрО РАН. - 2019. - № 2(38). - С. 51-57.
- Гнездилова, А.И. Развитие научных основ кристаллизации лактозы и сахарозы в многокомпонентных водных растворах: автореф. дис. докт. техн. наук. / А.И. Гнездилова. - М., 2000. - 46 с.
- Червецов, В.В. Интенсификация процессов кристаллизации при производстве молочных продуктов / В.В. Червецов, А.И. Гнездилова. - М.: типография Россельхозакадемии, 2011. - 196с.
- Шохалов, В.А. Разработка технологии консервированного мо-локосодержащего продукта с сахаром: дис. ... канд. техн. наук: 05.18.04 / Шохалов Владимир Алексеевич. - Вологда, 2004. - 149 с.


