Сравнительная оценка способов и обоснование оперативного метода экспериментального определения доли изомеризации лактозы в лактулозу
Автор: Гнездилова Анна Ивановна, Шевчук Владимир Борисович, Новикова Татьяна Валентиновна, Виноградова Юлия Владимировна
Журнал: Молочнохозяйственный вестник @vestnik-molochnoe
Рубрика: Технические науки
Статья в выпуске: 1 (33), 2019 года.
Бесплатный доступ
В работе проведена сравнительная оценка способов экспериментального определения лактулозы. Обосновано, что поляриметрический метод анализа является наиболее приемлемым для оперативного метода экспериментального определения доли изомеризации лактозы в лактулозу.
Лактоза, лактулоза, поляриметрический, хромотографический, изомеризация
Короткий адрес: https://sciup.org/149126696
IDR: 149126696 | УДК: 637.345 | DOI: 10.24411/2225-4269-2019-00008
Comparative evaluation of methods and justification of the operational method for experimental determining the isomerization proportion of lactose into lactulose
The article gives a comparative assessment of methods for experimental determination of lactulose. It has been established, that the polarimetric method of analysis is the most appropriate one for the operational method of experimental determination of the lactose isomerization fraction into lactulose.
Текст научной статьи Сравнительная оценка способов и обоснование оперативного метода экспериментального определения доли изомеризации лактозы в лактулозу
Актуальность.
В настоящее время известны различные методы определения лактулозы [1-5], которые основаны:
-
- на химических реакциях углеводов, связанных с их редуцирующими свойствами и образованием окрашенных соединений;
-
- физических и физико-химических свойствах углеводов;
-
- биохимических реакциях.
Современная аналитическая химия располагает рядом методов количественного определения углеводов, основанных на химических реакциях с использованием редуцирующих свойств или образованием окрашенных соединений [1]. Однако определение лактулозы в реальном сырье этими методами затруднено из-за наличия в растворах и сиропах близких по строению и свойствам углеводов, минеральных и азотистых компонентов.
Ферментативный метод, описанный в работе [6], позволяет определить лактулозу в присутствии значительного количества лактозы. Основой метода вляется совместный гидролиз лактозы и лактулозы ß-Д-галактозидазой с образованием моносахаров: глюкозы, галактозы и фруктозы и дальнейшее преобразование фруктозы под действием никотинамидадениндинуклеотидфосфата (НАДФ) с использованием ряда ферментов. Содержание образующегося после добавления никотинамида-дениндинуклеотидфосфата НАДФН измеряют фотометрически при 340 нм [7]. По данным [2] ферментативный метод дает завышенные результаты, так как при этом измеряется и содержание свободной фруктозы. Чтобы устранить погрешность, необходимо проводить параллельное определение фруктозы. Однако метод требует дорогостоящих ферментов и реактивов, что затрудняет его использование в производственных условиях.
Анализ литературы показал, что наиболее широко в научных исследованиях применяются хроматографические методы определения углеводов. Хромотографический метод анализа включает бумажную хроматогафию, тонкослойную (ТСХ), газо-жидкостную.
В работе [8] предложено осаждать лактозу в смеси с лактулозой с помощью ацетона, а отделение оставшихся дисахаридов осуществлять тонкослойной хроматографией (ТСХ). Глюкоза, галактоза и сахароза, которые могут находиться в молочных продуктах, не мешают определению лактулозы. Для удаления белков и жира их осаждают с помощью сернокислой меди. Способ позволяет определять присутствие лактулозы в количествах ниже 0,02% от общего содержания углеводов.
При отработке методики ТСХ авторами [2] было достигнуто четкое разделение между лактозой и лактулозой. Проведенные исследования показали, что метод ТСХ можно использовать для селективного разделения углеводов в смеси и идентификации лактулозы в присутствии других сахаров. В то же время анализ ТСХ связан с применением целого ряда токсичных дорогостоящих реактивов (ацетонитрила, дифениламина, анилина, фосфорной кислоты, ацетона) и дает значительный разброс данных при количественном определении углеводов.
К современным методам определения углеводов относится высокоэффективная жидкостная хроматография (ВЭЖХ) [9]. Относительная ошибка определения лактулозы в промышленных образцах составила 0,5%. К сожалению, этот метод пока широко не применяется в нашей стране для определения углеводов молока.
Более доступным и освоенным является метод газожидкостной хроматографии
(ГЖХ). Он основан на переводе моно- и дисахаридов в летучие триметилсилильные производные с последующим их разделением на ГЖХ-колонке и определением с помощью пламенно-ионизационного детектора.
Автором [10] разработана усовершенствованная методика газо-хроматографического определения лактулозы. Особенностью метода является выбор насадки, вид колонки, принцип программирования температуры, а также природа реагента, используемого при получении триметилсилилпроизводных углеводов. Сущность метода заключается в следующем. Анализируемый образец, пердварительно высушенный и обезжиренный, обрабатывают N-триметилсилилимидазолом при температуре (60‒70)°С в течение 1-2 ч. Затем к смеси добавляется точный объем гексана, избыток которого гидролизуется водой, после чего аликвота гексановой фазы инжектируется в хроматограф. Разделение углеводов проводится на насадочной колонке с полярной фазой в изотермическом режиме. Моносахариды при этом выходят с фронтом растворителя, лактоза ‒ в виде двух пиков, соответствующим альфа- и бета-аномерам, а лактулоза ‒ в виде одного пика. Содержание лактулозы, лактозы, галактозы рассчитывали методом внутреннего стандарта с использованием предварительно проведенной калибровки.
Как показали результаты исследований, метод ГЖХ имеет высокую точность и разрешающую способность, позволяет качественно и количественно определять лактулозу в присутствии альфа- и бетаформ лактозы, галактозы, глюкозы, тага-тозы, фруктозы и других углеводов. Однако организация ГЖХ достаточно сложна, требует больших затрат, поэтому этот метод не может применяться для проведения массовых анализов и контроля в производственных условиях.
Более доступными для проведения производственного контроля являются спектрофотометрические методы определения лактулозы, которые основаны на измерении интенсивности окраски комплексов, которые образуются при реакции этого углевода с некоторыми веществами. Имеются данные о применении метиламина, дающего с лактулозой при определенных условиях соединения фиолетовокрасного цвета [11]. Определению мешают: лактоза, мальтоза и другие альдозы, поэтому автор предлагает окислять их гипоиодитом, а образовавшиеся альдоновые кислоты удалять с помощью ионообменных смол.
Во ВНИИМС разработан колориметрический метод определения лактулозы, основанный на реакции Иохансона [12]. В среде, состоящей из смеси фосфорной и уксусной кислот, лактулоза образует окрашенный комплекс, имеющий максимум поглощения при длине волны 427,4 нм. Для исключения влияния на результат анализа альдозы лактозу осаждают в 92%-ном этиловом спирте.
На начальных этапах исследования автором [2, 3] использовался именно этот метод определения лактулозы. Однако при отработке методики была отмечена его высокая чувствительность к температурным условиям проведения анализа и значительный разброс данных при построении калибровочного графика [13]. К недостаткам метода относится также сложный состав и нестойкость антронового реактива, который необходимо готовить непосредственно перед анализом.
В Литовском филиале ВНИИМС был разработан спектрофотометрический метод определения лактулозы в сиропах и молочных смесях для детского питания [14, 15]. Он основан на реакции лактулозы с серной кислотой. При нагревании реакционной смеси образуется сложная смесь различных продуктов (оксиметил-фурфурол, фуран, левулиновая кислота и др.), имеющих красно-коричневый цвет. Подбор концентрации кислоты и времени выдержки в кипящей водяной бане по- зволили определить условия, при которых альдозы (лактоза, галактоза и другие) не влияют на результаты определения лактулозы [16].
Как показали исследования, определение лактулозы с серной кислотой проще, чем с антроном, в исполнении, требует меньшего количества реактивов и затрат времени при той же достоверности результатов. При отработке спектрофотометрического метода и построении калибровочного графика было установлено, что зависимость оптической плотности от концентрации лактулозы имеет вид прямой в интервале (2-10) мг/см3 [2].
Спектрофотометрический метод был использован при проведении экспериментальных исследований и стал основой разработки методики выполнения измерений массовой доли лактулозы, рекомендованной НИИДП для контроля производства концентрата лактулозы для детского питания [17].
Поляриметрический метод основан на специфической оптической активности углеводов. Лактоза вращает плоскость поляризованного света вправо и имеет удельный угол вращения [α] = +52,5°, а лактулоза - влево, [α] = -51,5°. Измерение удельного вращения [α], которое является мерой оптической активности веществ, является одним из наиболее простых и надежных методов контроля их чистоты.
На основании измерений показателей удельного вращения исследуемых растворов и статистической обработки большого объема экспериментальных данных О.Н. Яковлевой [18] были составлены специальные таблицы, позволяющие по данным оптической активности определять содержание лактулозы.
При уточнении этого метода во ВНИИМС В.Я. Матвиевским [5] было получено уравнение зависимости удельного угла вращения [α] от содержания лактозы Х:
[α]=-7,3·Х+56,6, (1)
где Х ‒ содержание лактозы,%.
В результате было установлено, что снижение [α] на 7,3° соответствует увеличению содержания лактулозы на 1%.
При отработке метода авторами [2] было установлено, что на точность определения лактулозы поляриметрическим методом оказывает влияние содержание белка, минеральных солей, молочной кислоты и других компонентов раствора.
Авторами [2] на основе сопоставления большого количества данных измерений содержания лактулозы поляриметрическим, спектрофотометрическим и хроматографическим методами были получены эмпирические уравнения для расчета степени изомеризации S лактозы в лактулозу в разных видах сырья:
-
- для модельных растворов лактозы и рафинированного молочного сахара:
S = 51,5-0, 98 [α];(2)
-
- для растворов молочного сахара-сырца:
S = 45,2-0, 96 [α];(3)
-
- для подсырной сыворотки:
S = 44,1-1,12 [α];(4)
-
- для творожной сыворотки:
S = 31,0-1,32 [α].(5)
Сравнительные исследования показали, что при учете поправочных коэффициентов поляриметрический метод определения лактулозы дает достаточно хорошую сходимость с другими, более точными методами (спектрофотометрическим и хроматографическим).
Целью работы является сравнительная оценка способов экспериментального определения лактулозы для обоснования выбора оперативного метода экспери- ментального определения доли изомеризации лактозы в лактулозу.
Сравнительный анализ методов показывает, что поляриметрический метод определения лактулозы является наиболее приемлемым для оперативного контроля.
Для проведения исследований поляриметрическим методом проводилась предварительная очистка растворов от белка, минеральных солей, молочной кислоты и других компонентов. Методика заключалась в следующем. 33 г исследуемого продукта растворяют в стакане, вместимостью 250 см3 , и количественно переносили в мерную колбу, вместимостью 100 см3.
Добавляют 3 мл раствора уксусно-кислого цинка и 3 мл железистосинеродистого калия. После добавления реактивов содержимое колбы осторожно перемешивают во избежание образования пузырьков. Затем объем доводят до метки дистиллированной водой при температуре 20 ± 2°С, вновь перемешивают и спустя 20±2 минуты фильтруют через сухой складчатый фильтр. Фильтрат поляризуют в поляриметрической трубке, длиной 200 мм. Отсчет показаний поляриметра проводят не менее 5 раз, и из полученных результатов берут среднеарифметическое значение. В работе использовался поляриметр Atago AP-300 (Япония).
Для построения калибровочных зависимостей были использованы растворы лактозы, лактулозы и их смеси, приготовленные в различных соотношениях. Калибровочные растворы имели концентрацию сухих веществ, равную концентрации сухих веществ в рабочих растворах.
Значения удельного угла вращения при различных соотношениях лактоза : лактулоза приведены в таблице .
Таблица. Значение удельного угла вращения [α] D при различных соотношениях лактоза : лактулоза
|
Соотношение лактоза : лактулоза |
Удельный угол вращения, [α] D град |
|
1:0 |
+27,02 |
|
2:1 |
+13,44 |
|
1:1 |
+6,45 |
|
1:2 |
-0,38 |
|
0:1 |
-14,12 |
По полученным данным была построена графическая зависимость (рисунок) , с помощью которой можно определять долю изомеризации лактозы в лактулозу в 50-60%-ных водных растворах в зависимости от удельного угла вращения.
Доля изомеризации лактозы в лактулозу может быть определена также аналитически по уравнению:
L= [«]-7 ,0 0,4114 , % где [α] – показания удельного угла вращения раствора, град.
С помощью калибровочных графиков была определена доля изомеризации лактозы в лактулозу в образцах продукта после проведения изомеризации сгущенного концентрата нанофильтрата с массовой долей сухих веществ 57% и лактозы ‒ 49%. Удельный угол вращения раствора составил [α]=2,54 град. В результате было установлено, что доля изомеризации составляет 59,5%.
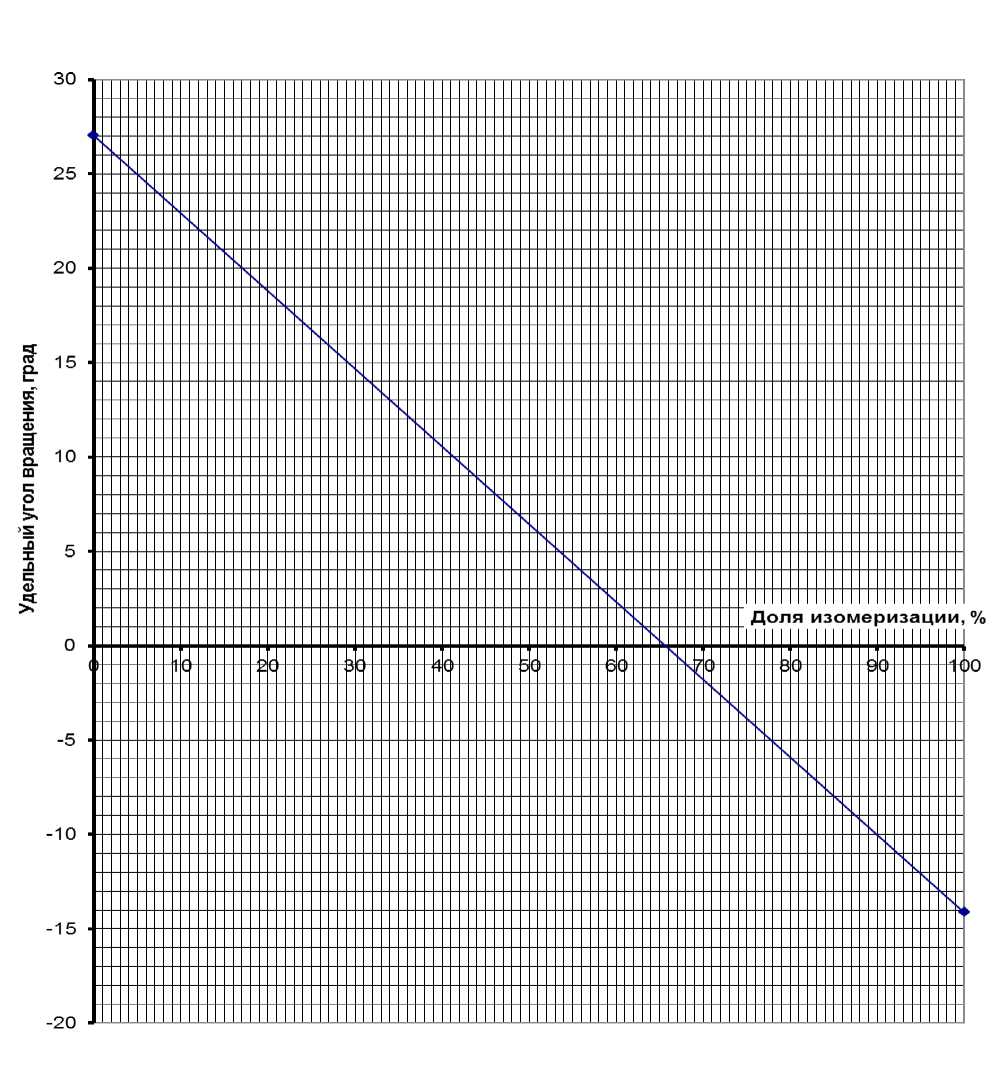
Рисунок. Зависимость удельного угла вращения от доли изомеризации
Вывод.
Поляриметрический способ экспериментального определения удельного угла вращения может быть использован для оперативного метода контроля доли изомеризации лактозы в лактулозу.
Список литературы Сравнительная оценка способов и обоснование оперативного метода экспериментального определения доли изомеризации лактозы в лактулозу
- Горбатова, К.К. Биохимия молока и молочных продуктов/К.К. Горбатова. -М.: Легкая и пищевая промышленность, 1984. -344 с.
- Рябцева, С.А. Развитие физико-химических основ технологии лактулозы: автореф. дис.. д-ра техн. наук/С.А. Рябцева. -Ставрополь, 2000. -42 с.
- Рябцева, С.А. Физико-химические основы технологии лактулозы: монография/С.А. Рябцева. -Ставрополь: СевКавГТУ, 2001. -138 с.
- Серов, А.В. Химия и физика лактозы и ее производных: монография/А.В. Серов. -Ставрополь: СевКавГТУ, 2003. -116 с.
- Матвиевский, В.Я. Исследование процесса получения сиропа лакто-лактолузы для продуктов детского питания: автореф. дис. … канд. техн. наук/В.Я. Матвиевский. -М.: 1979. -25 с.
- Гейер, Г. Ферментативный метод определения лактулозы/Г. Гейер, X. Клостермайер//XXI Межд.мол.конгресс. Краткие сообщения. Т. 1, кн. 2. -М.: 1982. -С. 293.
- ГОСТ Р 51939-2002. Метод определения лактулозы.
- Мартинес-Кастро, И. Обнаружение небольших количеств лактулозы в молочных продуктах методом тонкослойной хроматографии/И. Мартинес-Кастро, А. Алано//XXI Межд.мол.конгресс. Краткие сообщения. Т.2, кн.2. -М.: 1982. -С. 302-303.
- Рудаков, О.Б. Современная жидкостная хроматография углеводов/О.Б. Рудаков, К.К. Полянский//Молочная промышленность. -1999. -№4. -С. 25-27.
- Серов, В.А. Теоретическое обоснование и экспериментальные исследования химико-технологических проблем получения, определения и использования лактозы и ее производной лактулозы: автореф. дис.. д-ра техн. наук/В.А. Серов. -Ставрополь, 2004. -40 с.
- Adachi S. Spectrofotometric determination of lactulose with methylamine//Anal. Chem.,1965,v.37, N 7. -P.896-898.
- Кравченко, Э.Ф. Модификация методики количественного определения лактулозы в присутствии лактозы/Э.Ф. Кравченко, В.Я. Матвиевский, А.Г. Храмцов//Труды ВНИИМС. Т. 21. -1977. -С. 95-96.
- Василисин, С.В. Теория и практика определения лактулозы колориметрическим методом/С.В. Василисин, C.A. Рябцева, Р.Ф. Храмцова. -М., 1986. -5 с.
- Маргелите, Ю. Спектрофотометрический метод определения массовой доли лактулозы в сиропе лакто-лактулозы/Ю. Маргелите, Г. Качераускене//Методический сборник (Литовский филиал ВНИИМС). -М.: АгроНИИТЭИММП, 1988. -С.61-64.
- Качераускене, Г. Количественное определение лактулозы в детских молочных продуктах/Г. Качераускене, Ю. Маргелите//XXI Межд.мол.конгресс. Краткие сообщения. Т. 1, кн. 2. -М.: 1982. -С. 95.
- Маргелите, Ю. Исследование реакции карбогидратов с серной кислотой для их количественного определения/Ю. Маргелите//Сб. науч. трудов лит. фил. ВНИИМС. Т. 10, 1976. -С. 275-283.
- О разработке технологического процесса получения лактулозы/Л.Г. Андреенко, Г.А. Антипова, В.В. Тихонычев и др.//Труды участников Межд. конф. «Научные и практические аспекты совершенствования качества продуктов детского и геродиетического питания». -М.: Пищепромиздат, 1997. -С. 26-27.
- Яковлева, О.Н. Разработка методов получения углеводов для детского питания: автореф. дис.. к.т.н./О.Н. Яковлева. -Киев, 1963. -22 с.


